
2022-07-08 14:29:31来源:医药魔方info浏览量:657
近日,国家药品监督管理局药品审评中心(CDE)官网显示,默沙东MK-4830注射液临床申请已获受理。
免疫球蛋白样转录子4 (ILT4) 受体——也称为白细胞免疫球蛋白样受体B2 (LILRB2) - 是ILT家族的免疫抑制成员,通常在许多骨髓谱系表达,包括单核细胞、巨噬细胞、粒细胞和树突状细胞。在肿瘤微环境中,ILT4通常表达于单核骨髓源性抑制细胞(MDSC)和粒细胞性MDSC中。ILT4的典型配体是人类白细胞抗原G (HLA-G),这是一种在肿瘤细胞广泛表达的非经典MHC I类分子,其表达与预后不良有关。其他几种ILT4配体,包括经典的人类白细胞抗原(HLA)和血管生成素样蛋白,也可能与驱动ILT4介导的肿瘤微环境免疫抑制有关。
MK-4830是一款first-in-class全人源IG4亚型抗ILT4单抗,可特异性结合 ILT4并阻断其与HLA-G和其他配体的相互作用。MK-4830最初于Agenus公司发现,后来默沙东获得了该款产品的开发授权。
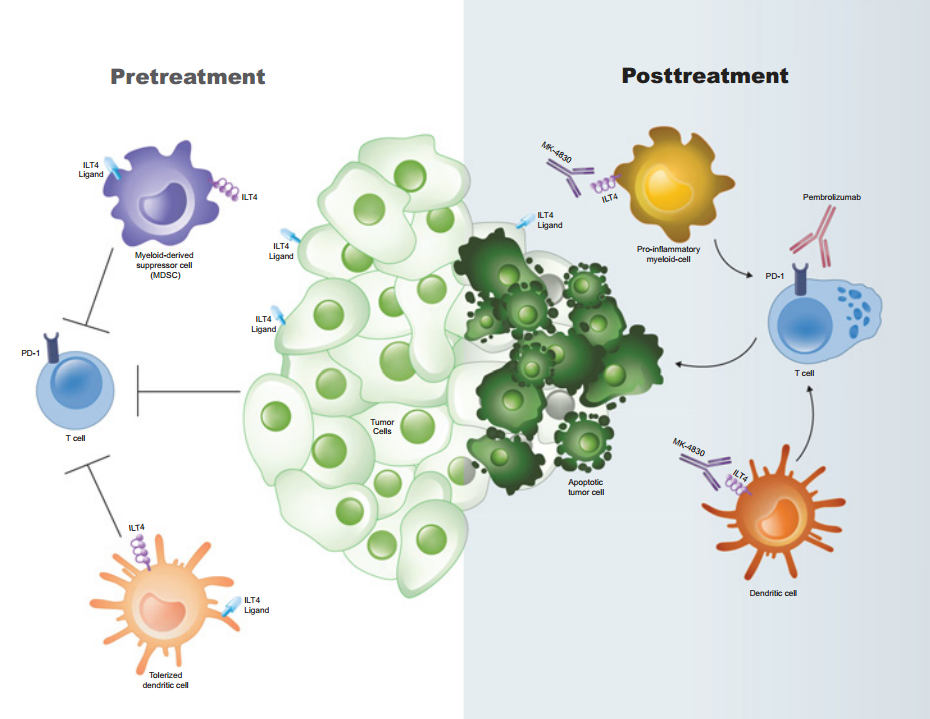
MK-4830联合Keytruda治疗实体瘤的首个人体I期研究数据显示,患者ORR为24%,在11例先前接受过PD-1治疗的患者中有5例患者产生应答(45%)。

在国内,早在今年3月以明生物医药已经申报了ILT4抑制剂IO-108的临床申请,是国内首家。
声明:本文系药方舟转载内容,版权归原作者所有,转载目的在于传递更多信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除内容!