
2022-07-08 14:31:35来源:药方舟浏览量:679
7月7日,CDE官网显示,武田的Modakafusp Alfa注射液(TAK-573)临床试验申请获药监局受理。它是一款first-in-class的免疫靶向减毒细胞因子,旨在将减毒干扰素α-2b(IFNα2b)片段递送至表达CD38肿瘤细胞。

目前,武田正在国外开展AK-573用于治疗多发性骨髓瘤(MM)和实体瘤的I/II期临床。

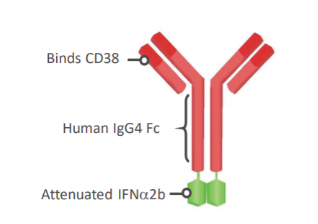
AK-573由通过基因融合到人源化抗CD38 IgG4单克隆抗体(mAb)Fc部分的两个减毒IFNα2b分子组成。减弱的IFNα2b分子对CD38特异性、与IFN受体结合亲和力降低,可以显著减少脱靶结合和毒性的可能性。
今年6月,武田在2022 ASCO大会上公布了TAK-573治疗转移性实体瘤Ib/II期研究(NCT04157517)中剂量递增阶段的安全性、药代动力学、免疫原性、药效学(PD)和初步疗效数据。
21例患者在剂量递增阶段接受0.1(n=3)、0.2(n=3)、0.4(n=3)、0.75(n=3)、1.0(n = 3)和1.5mg/kg(n = 6)Q3W给药;中位年龄63岁;男性57.1%;GI恶性肿瘤71.4%;中位既往治疗线数3(范围2-7)。
2例患者在cycle 1的1.5mg/kg剂量水平发生了剂量限制毒性(DLT);1例基线骨浸润患者发生了4级血小板减少,1例患者发生了3级意识模糊。截至2021年11月,所有剂量组的患者接受中位2个治疗周期(范围1-11)。81%的患者报告的TRAE包括输注相关反应(52.4%)、寒战(47.6%)和恶心(33.3%)。42.9%的患者报告的≥3级TRAE包括中性粒细胞减少症(14.3%)和高血压(9.5%)。
在14例可评价疗效的患者中,7例的最佳缓解为疾病稳定,包括1例靶病灶缩小21%的皮肤黑色素瘤患者。
声明:本文系药方舟转载内容,版权归原作者所有,转载目的在于传递更多信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除内容!