8月22日,石药集团宣布了两款在研1类新药的研发进展,包括:1)DPP-4抑制剂普卢格列汀片治疗2型糖尿病的两项关键3期临床试验均达到预设终点,拟于近期在中国递交上市申请;2)选择性的NTRK和ROS1双靶点抑制剂SYHX2009在中国获批临床。
DPP-4全称为二肽基肽酶-4,DPP-4抑制剂是治疗糖尿病的主要药物类型之一。公开资料显示,这类药物不仅能够抑制胰高血糖素样肽-1(GLP-1)和葡萄糖依赖性促胰岛素分泌多肽(GIP)的灭活,提高内源性GLP-1和GIP的水平,促进胰岛β细胞释放胰岛素,同时还能抑制胰岛α细胞分泌胰高血糖素,提高胰岛素水平,降低血糖,且不易诱发低血糖和增加体重。普卢格列汀片(DBPR108片)是石药集团附属公司石药集团中奇制药的1类新药,为一种新型口服DPP-4抑制剂,对DPP-4具有高选择性和强抑制性。据石药集团新闻稿介绍,该药通过抑制DPP-4,使内源性活性GLP-1水平升高,从而增强β细胞和α细胞对葡萄糖的敏感性,增加葡萄糖刺激的胰岛素分泌并增强葡萄糖对胰升糖素分泌的抑制作用,进而降低血糖水平。石药集团在中国开展了两项3期临床试验作为DBPR108片治疗2型糖尿病的关键临床试验,用于支持上市申报,分别为DBPR108片单药3期试验、DBPR108片联合二甲双胍3期试验。两项3期试验共入组约1000例2型糖尿病受试者,试验结果均显示较好的临床效果,达到预设终点。其中单药试验结果显示,在主要疗效终点第24周末糖化血红蛋白(HbA1c)较基线变化,DBPR108 片组显著优于安慰剂组,同时非劣于阳性药磷酸西格列汀片组。联合试验结果显示,在主要疗效终点第24周末HbA1c较基线变化, DBPR108片组显著优于安慰剂组。此外,DBPR108片组的安全性数据显示安全性与西格列汀组和安慰剂组相似。石药集团新闻稿表示,基于以上研究结果拟于近期向中国国家药品监督管理局(NMPA)提交上市前沟通交流的申请。
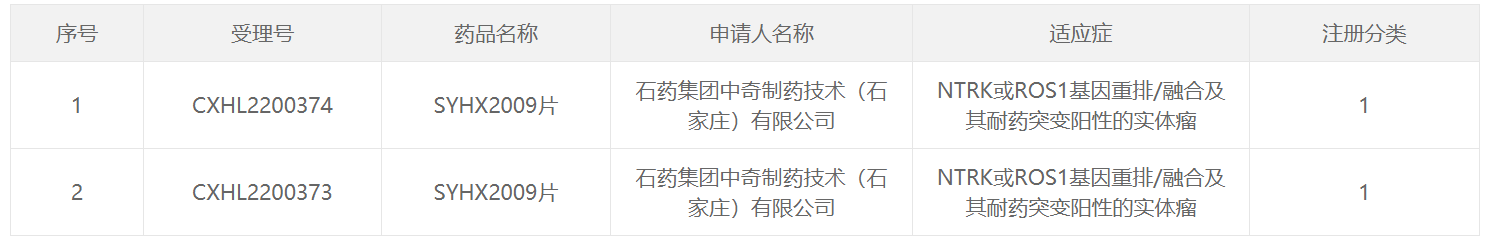
截图来源:中国国家药监局药品审评中心(CDE)官网
NTRK中文全称是神经营养因子受体酪氨酸激酶。NTRK融合阳性肿瘤产生的原因是NTRK1/2/3基因与其它基因融合,导致编码的TRK蛋白出现异常。变异的TRK或者TRK融合蛋白持续激活,从而引发永久的信号级联反应,这些蛋白在TRK融合癌患者中是驱动肿瘤增长和转移的主要因素。研究发现,NTRK基因融合可能出现在起源于身体不同位置的肿瘤中,这使得它成为了研究人员开发“不限癌种”疗法的靶标之一。ROS1是一种编码受体酪氨酸激酶的基因,与间变性淋巴瘤激酶(ALK)结构相似,是非小细胞肺癌明确的一种少见驱动基因。融合(重排)是ROS1基因的主要变异类型。SYHX2009为石药集团开发的1类新药,为一种选择性的NTRK和ROS1双靶点抑制剂。临床前研究显示,该产品具有优异的体内外活性和良好的安全性。本次,该药获批临床的适应症为:NTRK或ROS1基因重排/融合及其耐药突变阳性的实体瘤。
声明:本文系药方舟转载内容,版权归原作者所有,转载目的在于传递更多信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除内容!


