9月13日,天境生物宣布,基于II期研究(NCT04202003)的积极结果,CDE已批准来佐利单抗联合阿扎胞苷治疗初诊较高危骨髓增生异常综合征(HR-MDS)的III期注册性临床试验。

NCT04202003是一项多中心、开放标签I/IIa期研究,共纳入53例患者(截至2022.03.31),旨在探索来佐利单抗与阿扎胞苷联合治疗初诊HR-MDS的疗效与安全性。
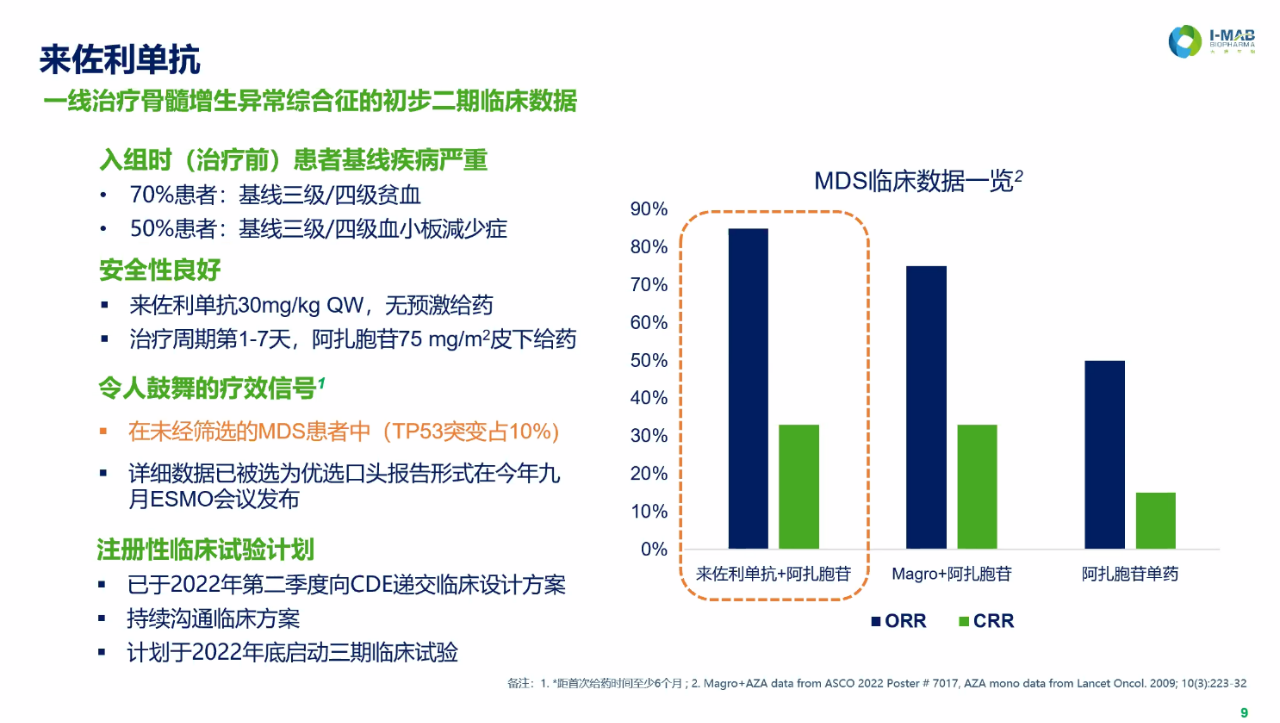
结果显示,该联合疗法治疗HR-MDS展现出了积极的疗效信号:
- 距离首次给药6个月及以上的15例患者,客观缓解率为86.7%,完全缓解率为40%;
- 距离首次给药4个月及以上的29例患者,客观缓解率为86.2%,完全缓解率为31%;
- 来佐利单抗无需预激给药,与阿扎胞苷联合疗法具有良好的耐受性,且安全性与阿扎胞苷单药治疗相当;
- 入组的患者多合并基础疾病,基线情况较差(74%伴有≥ 3级贫血,51%伴有≥3级血小板减少症)。
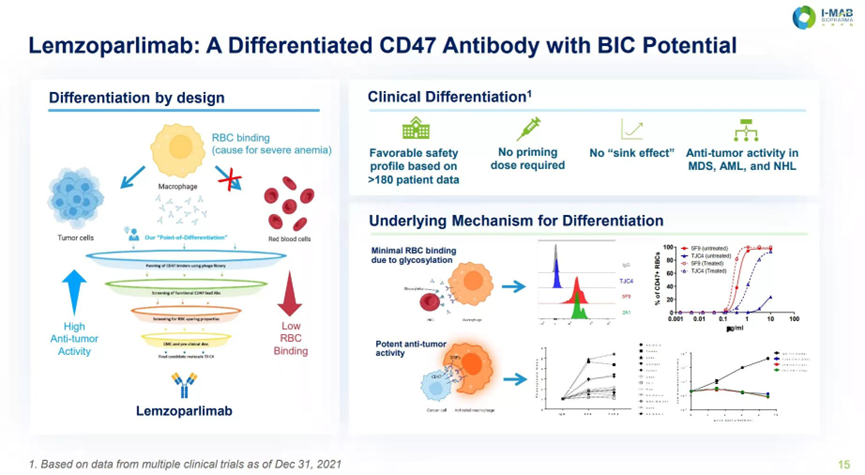
MDS临床多表现为无效造血和难治性血细胞减少。截至数据分析时,患者的中位血红蛋白和血小板水平随着治疗的进展而显著提升:在29例基线输血依赖的患者中,有9例(31%)转化为非输血依赖。此外,获得完全缓解患者的MDS相关驱动基因(包括TP53、TET2和RUNX1等)的突变频率(VAF)显著降低,并且 56%的完全缓解患者微小残留病灶为阴性(≤10-4)。上述临床数据表明,来佐利单抗的抗肿瘤活性和安全性特征与既往研究结果一致,进一步印证了来佐利单抗的差异化优势。CD47是一种在多种肿瘤中过度表达的细胞表面蛋白,可以通过向肿瘤吞噬巨噬细胞传递“不要吃我”的信号来保护肿瘤。CD47抗体可阻断该信号并使巨噬细胞能够攻击肿瘤细胞。然而,CD47抗体的血液学副作用较大,例如由CD47抗体与红细胞的自然结合引起的严重贫血,因此其临床应用严重受限。来佐利单抗(lemzoparlimab)是天境生物自主研发的一款高度差异化的CD47单克隆抗体。天境生物的研发团队通过差异化设计和针对性筛选发现了识别CD47抗原的独特表位,该表位与红细胞膜表面特殊的糖基化修饰相关,可大大降低CD47单抗与正常红细胞的结合,从而避免同类CD47抗体在临床试验中常见的血液系统毒性和药代动力学上的“沉没效应”。天境生物总裁朱秀轩博士表示:“骨髓增生异常综合征是一种治疗手段非常有限的恶性血液肿瘤,有相当大的临床需求尚待满足。作为天境生物自主研发管线中的核心产品,我们对来佐利单抗开展注册性研究乃至上市寄予厚望。此次CDE批准公司启动来佐利单抗联合阿扎胞苷治疗HR-MDS的III期临床试验,给予了我们充足的信心和鼓舞。我们期待尽快为饱受这一顽疾困扰的患者提供创新的治疗选择。”
声明:本文系药方舟转载内容,版权归原作者所有,转载目的在于传递更多信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除内容!