今日(9月14日),中国国家药品监督管理局药品审评中心(CDE)官网最新公示,由北京浦润奥生物科技有限责任公司(下称浦润奥生物)申请的1类新药伯瑞替尼肠溶胶囊拟纳入优先审评,拟用于具有间质-上皮转化因子(MET)外显子14跳变的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者。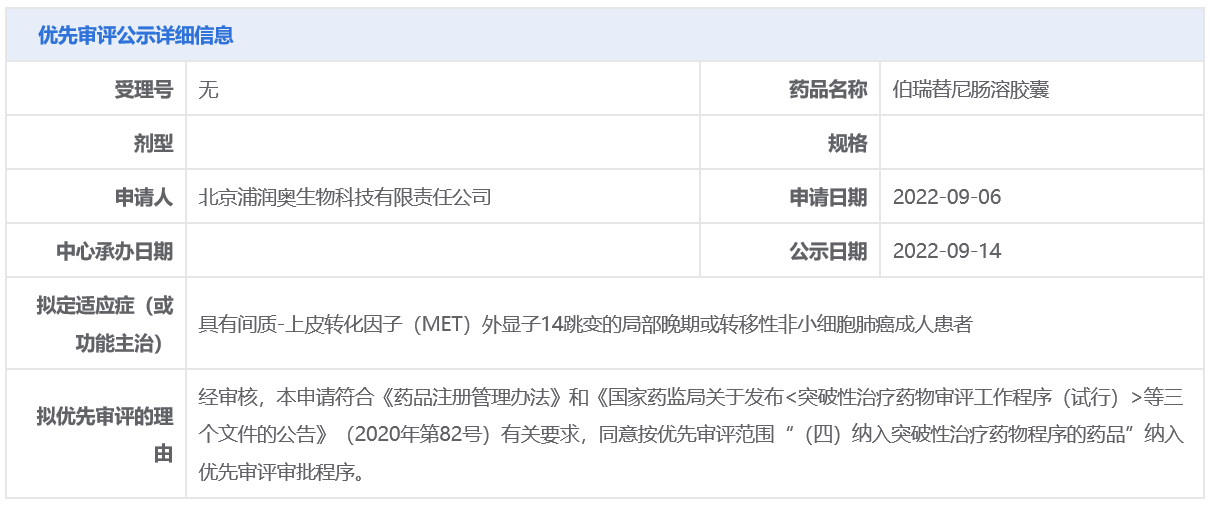
MET是癌症的驱动基因之一。在NSCLC中,带有MET突变的病例约占总数的3%-4%,MET信号通路在驱动肺癌对其它靶向疗法产生耐药性方面也具有重要作用。此外,研究人员也在多种癌症中观察到MET的异常表达现象,包括胃癌、肝细胞癌等。这也意味着,针对MET靶点开发的创新疗法有望对多个癌症产生效果。伯瑞替尼(bozitinib)正是一款针对c-MET的单靶点小分子靶向药物。它通过与ATP竞争位点结合,阻断酪氨酸激酶磷酸化发挥抑制c-MET激酶的作用。公开资料显示,该产品在中国的开发权由浦润奥生物拥有。2021年12月,鞍石生物宣布完成对浦润奥生物的收购,从而将伯瑞替尼纳入了其研发管线。在中国大陆、香港及澳门地区以外的其它地区,伯瑞替尼的开发权益归冠科美博(Apollomics)所有。据鞍石生物投资方维梧资本近日发布的新闻稿,伯瑞替尼目前由鞍石生物、首都医科大学附属北京天坛医院、北京市神经外科研究所江涛教授团队联合研发。江涛教授团队通过研究发现,PTPRZ1-MET(ZM)融合基因是脑胶质瘤的重要驱动基因之一,而伯瑞替尼作为小分子高选择性MET激酶抑制剂,能够透过血脑屏障,阻断ZM融合基因下游信号通路,达到抑制肿瘤生长和侵袭的作用。
在中国,伯瑞替尼曾被CDE纳入突破性治疗品种,拟用于c-MET外显子14突变的非小细胞肺癌。此次该产品拟纳入优先审评,针对的适应症为MET外显子14跳变的局部晚期或转移性NSCLC成人患者。此前,伯瑞替尼治疗c-MET异常的晚期NSCLC的中国境内多中心1期临床试验结果,已在2020年美国癌症研究协会(AACR)年会上公布。该研究由广东省人民医院吴一龙教授牵头。结果显示,伯瑞替尼总体耐受性良好,未出现剂量限制性毒性。在所有36例疗效可评估的患者中,伯瑞替尼的客观缓解率(ORR)为30.6%,疾病控制率(DCR)高达94.4%。在携带c-MET过度表达、扩增和外显子14突变的三个亚组中,患者ORR分别为35.7%,41.2%和66.7%。携带c-MET过度表达和扩增(N = 6)患者的ORR为50%。携带外显子14突变和扩增(N = 4)的患者ORR为100%。这表明,伯瑞替尼具有良好的耐受性和可控的安全性。在外显子14突变和/或扩增的患者中观察到初步的抗肿瘤活性,尤其是在携带外显子14突变的患者中。
根据中国药物临床试验登记与信息公示平台,目前伯瑞替尼正在开展多项临床试验,包括:一项多中心、多队列、开放的2期临床研究,以期在c-Met异常的晚期NSCLC患者中评估伯瑞替尼肠溶胶囊有效性和安全性;一项多中心、2/3期临床研究,旨在评价伯瑞替尼治疗ZM融合基因阳性继发性胶质母细胞瘤的安全性和有效性。希望伯瑞替尼此次拟纳入优先审评,能够加快该产品在中国的注册申报进度,早日为患者带来创新疗法。[1]中国国家药监局药品审评中心. Retrieved Sep 14, 2022, from https://www.cde.org.cn/main/xxgk/listpage/9f9c74c73e0f8f56a8bfbc646055026d[2]A phase Ⅰ study of cMET inhibitor bozitinib in patients with advanced NSCLC harboring cMET alterations. Retrieved August 2020, from https://cancerres.aacrjournals.org/content/80/16_Supplement/CT127[3]鞍石生物携手天坛医院推出伯瑞替尼,助力脑胶质瘤迈进靶向治疗时代 | 维梧生态圈 . Retrieved Sep 1, 2022, from https://mp.weixin.qq.com/s/j4HcsO1LhL2KBKhXy7Epmg[4]鞍石生物完成超2亿美元融资,维梧资本领投 . Retrieved Dec 9, 2021, from https://mp.weixin.qq.com/s/MeYikuQbjdR4lAVLV5TUfA
声明:本文系药方舟转载内容,版权归原作者所有,转载目的在于传递更多信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除内容!



