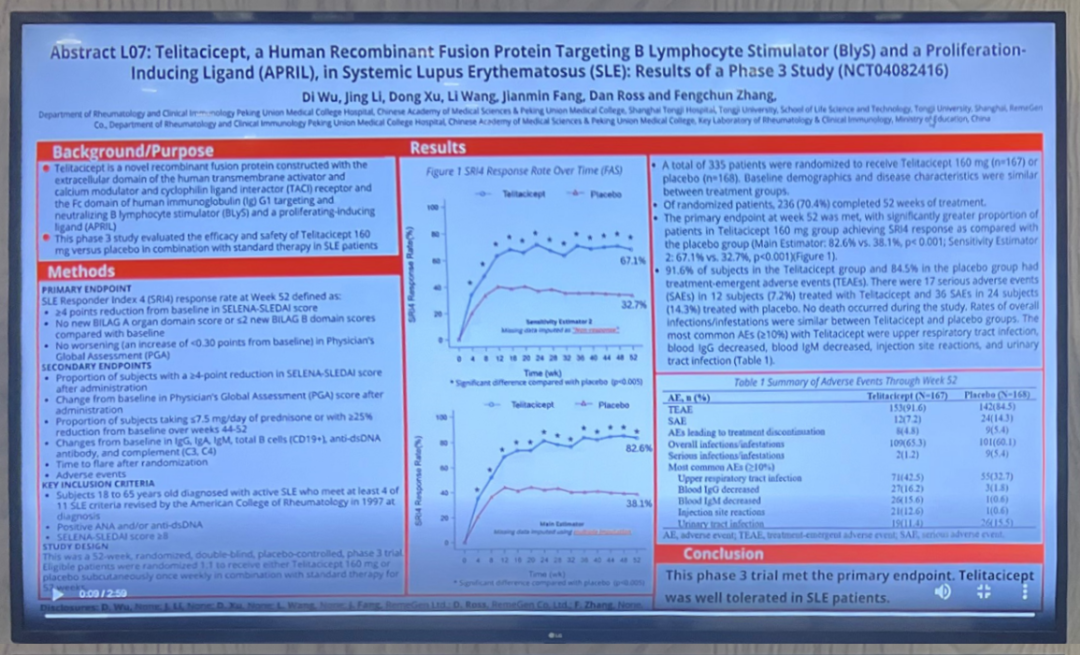
当地时间11月14日下午,2022年美国风湿病学会年会(American College of Rheumatology,ACR)的线下会场,一项重磅研究引发广泛关注——荣昌生物制药(烟台)股份有限公司以重要壁报形式公布了泰它西普治疗系统性红斑狼疮的国内Ⅲ期临床研究。美国风湿病学会(ACR)成立于1934年,是一个非营利性、全球医学协会。作为世界规模最大、最负盛名的风湿学会议,ACR年会汇聚了最新的研究成果和最具影响力的演讲嘉宾,每年都会吸引全球100多个国家约16000余名代表参与,已成为医学人士获取最前沿风湿病学研究与临床应用信息的重要平台。本届年会上,评分前10%的壁报可被纳入“热力演讲”(Ignite talk)环节,而泰它西普就是其中之一。会上,荣昌生物全球商务拓展高级副总裁Dan Ross代表公司发表演讲并参与现场讨论。Dan Ross介绍了,由北京协和医院张奉春教授牵头完成的泰它西普治疗系统性红斑狼疮(SLE) 患者的国内Ⅲ期确证性研究情况。短短五分钟的汇报,吸引了与会专家及国际媒体的目光,大家纷纷驻足交流,对泰它西普的全球开发计划表示出极大兴趣。这不是泰它西普首次亮相美国风湿病学会(ACR)年会。2019年12月5日,泰它西普治疗系统性红斑狼疮的关键临床研究作为“最新突破性进展”在ACR大会万人主会场作口头报告,成为当年大会的重磅消息,也是ACR大会历史上中国原创新药第一次获此殊荣,引起国际业界强烈反响。此次亮相的泰它西普国内Ⅲ期确证性研究是一项多中心、随机、双盲、安慰剂对照的临床研究,共入组335例SLE患者,患者随机分配到泰它西普(160毫克)组或安慰剂组,每周皮下注射一次,与标准治疗相结合,为期52周。初步结果显示,本研究达到了预设的临床终点,第52周SRI-4应答率在泰它西普组为82.6%,安慰剂组为38.1%,泰它西普组的SRI-4反应率均明显高于安慰剂组,显示出了良好的安全性和耐受性。目前,泰它西普治疗系统性红斑狼疮患者的全球多中心Ⅲ期临床试验正在顺利推进,已于今年上半年在美国完成首例受试者入组给药。泰它西普是由公司CEO、首席科学官房健民教授发明设计的一个抗体融合蛋白药物分子,通过同时抑制BLyS和APRIL两个细胞因子的过度表达,“双管齐下”阻止B细胞的异常分化和成熟,从而治疗B细胞介导的系统性红斑狼疮等一系列自身免疫性疾病。2021年3月9日,泰它西普系统性红斑狼疮适应症正式获得国家药监局的国内上市批准,同年底进入国家医保药品目录。除系统性红斑狼疮适应症外,泰它西普治疗类风湿性关节炎、IgA肾炎、原发性干燥综合征、视神经脊髓炎谱系疾病、重症肌无力、多发性硬化等适应症的Ⅲ期临床研究也在推进中。
声明:本文系药方舟转载内容,版权归原作者所有,转载目的在于传递更多信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除内容