
2023-06-06 09:34:03来源:医药观澜浏览量:852
根据中国国家药监局药品审评中心(CDE)官网,在刚刚过去的5月份,有多款1类新药获得临床试验默示许可,其中首次在中国获批临床的抗肿瘤1类新药有约30款。这些新药包含了抗体疗法、细胞和基因疗法、小分子新药,以及放射性核素偶联药物(RDC)、抗体偶联药物(ADC)等当下热门的新药研发形式。
按照新注册分类,“1类新药”是指尚未在全球任何国家和地区获批上市的药物。这类新药往往代表了药物研发领域的前沿方向,它们获批临床也让广大存在未满足临床需求的患者看到了希望。本文中就让我们看看5月获批临床的1类新药都有哪些?(完整数据详见文末表格) 。
截图来源:CDE官网
经过梳理发现,5月获批临床的抗肿瘤1类新药中包含了十余款抗体疗法,涵盖融合蛋白、单抗、双抗以及多特异性抗体。如:和铂医药靶向B7H7的单抗HBM1020,拟开发治疗晚期实体瘤;诺艾新生物非IL-2阻断型CD25单克隆抗体9MW3911注射液,拟开发治疗晚期恶性肿瘤;安进(Amgen)/百济神州靶向DLL3和CD3的双特异性T细胞衔接蛋白(BiTE)tarlatamab,拟用于接受含铂一线化疗后的复发性小细胞肺癌受试者;赛诺菲(Sanofi)在研的靶向CD123的NK细胞接合剂SAR443579,也是一款创新多特异性抗体分子,它通过激活NK细胞来杀伤癌细胞,拟开发治疗12岁及以上复发/难治性恶性血液病。
抗体疗法之外,5月获批临床的抗肿瘤1类新药中还包含了多种细胞和基因疗法(CGT)。如:恒瑞源正T细胞受体(TCR)-T产品HRYZ-T101注射液,拟开发用于人乳头瘤病毒18亚型阳性(HPV18+)的实体瘤;诺未科技靶向GPC3的DNA核酸药物NWRD06裸质粒DNA注射液,这是一款体内基因治疗药物,拟用于GPC3阳性原发性肝细胞癌根治术后患者;中生康元生物个性化肿瘤树突状细胞(DC)疫苗注射液,拟用于治疗恶性实体肿瘤。
此外还有RDC、ADC类新药以及多款小分子1类新药获批临床。比如:远大医药引进的靶向生长抑素受体(SSTR)的RDC产品镥[177Lu]依多曲肽注射液,拟开发用于神经内分泌肿瘤;阿斯利康(AstraZeneca)靶向EGFR-cMET的ADC产品AZD9592,拟单药和与抗癌药物联合用药治疗晚期实体瘤;映恩生物靶向HER3的ADC产品注射用DB-1310,拟用于晚期/转移性实体瘤。小分子1类新药则涵盖了KAT6、CDK7、SHP2等创新靶点,来自辉瑞(Pfizer)、同源康医药、海正药业等公司。
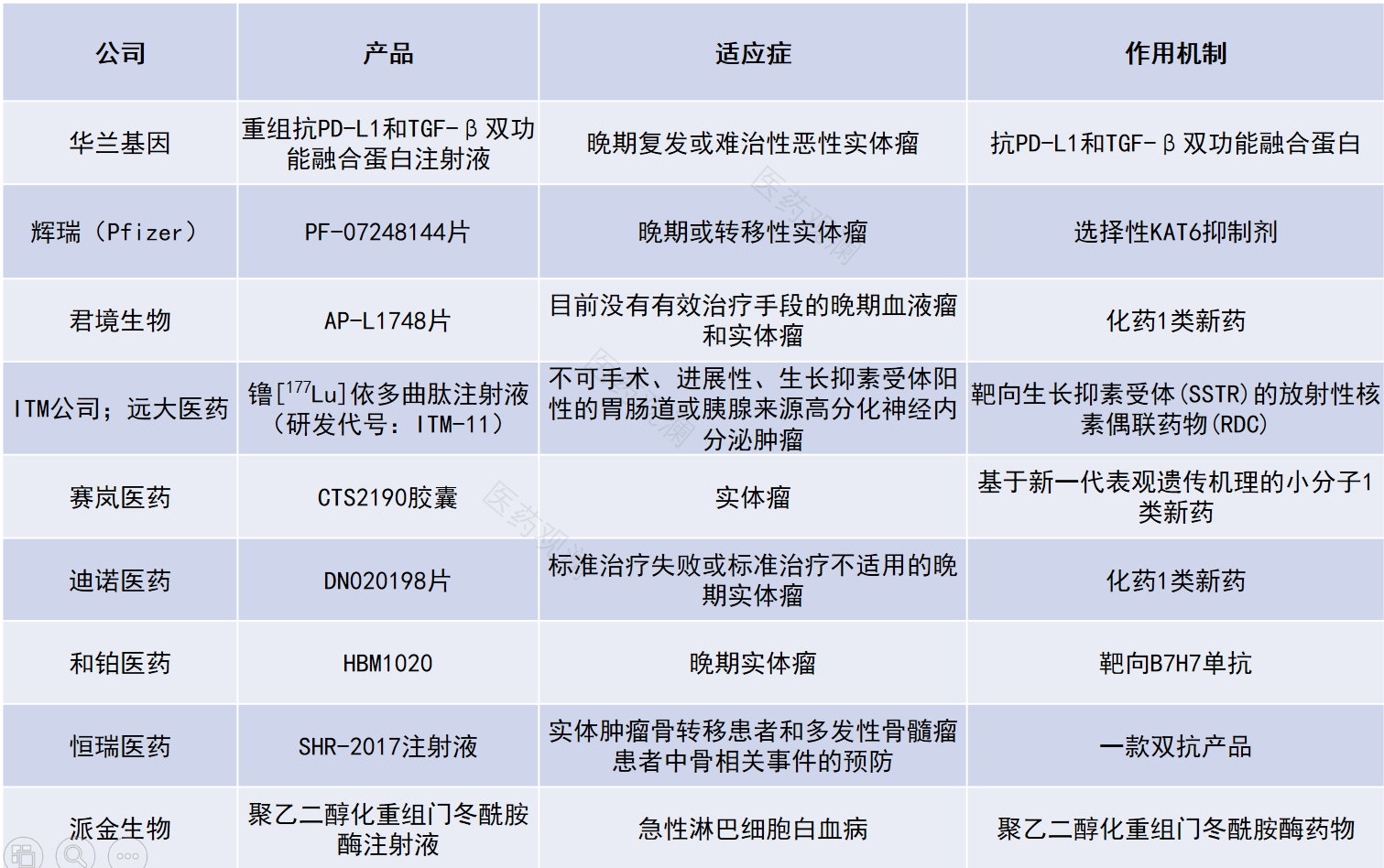
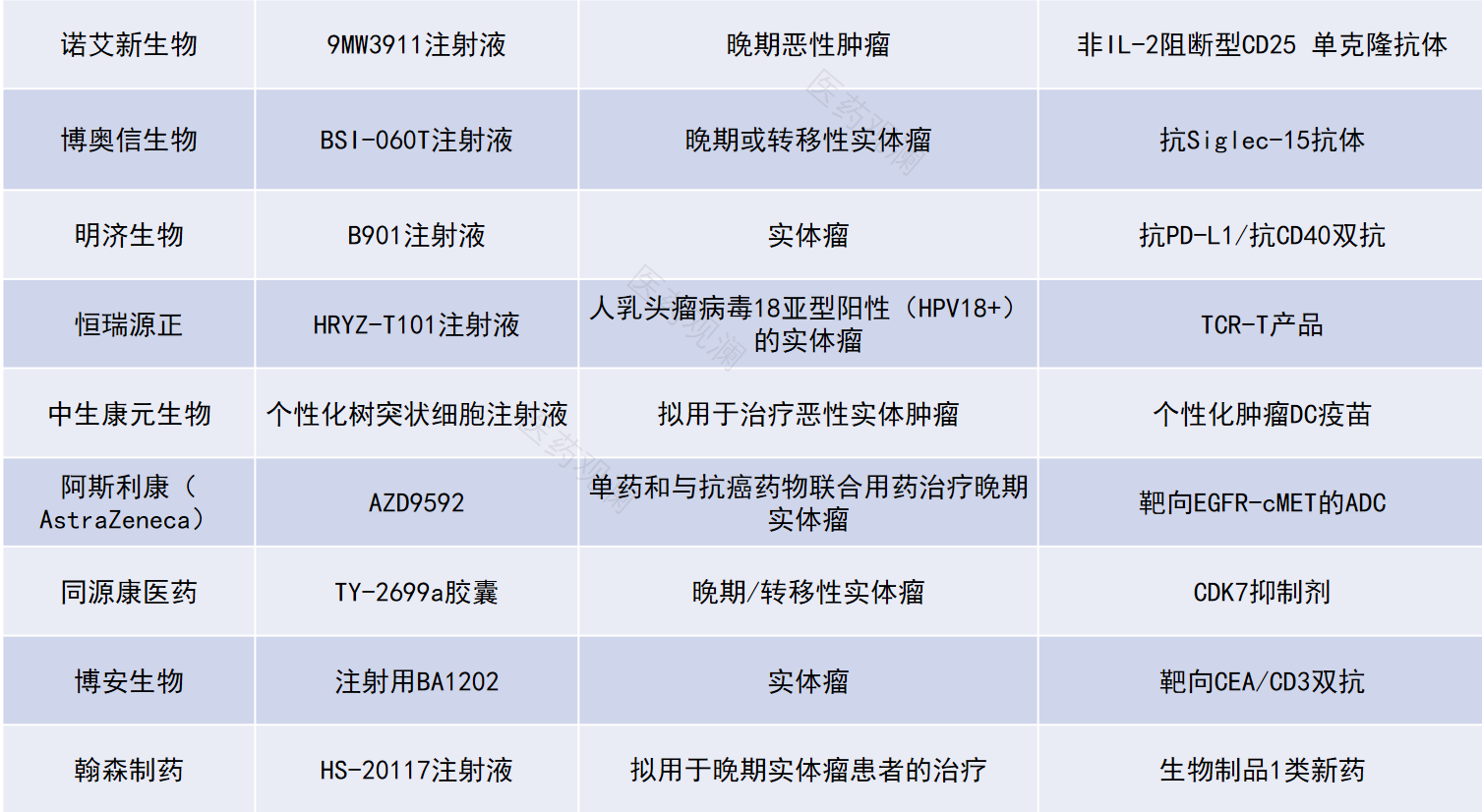
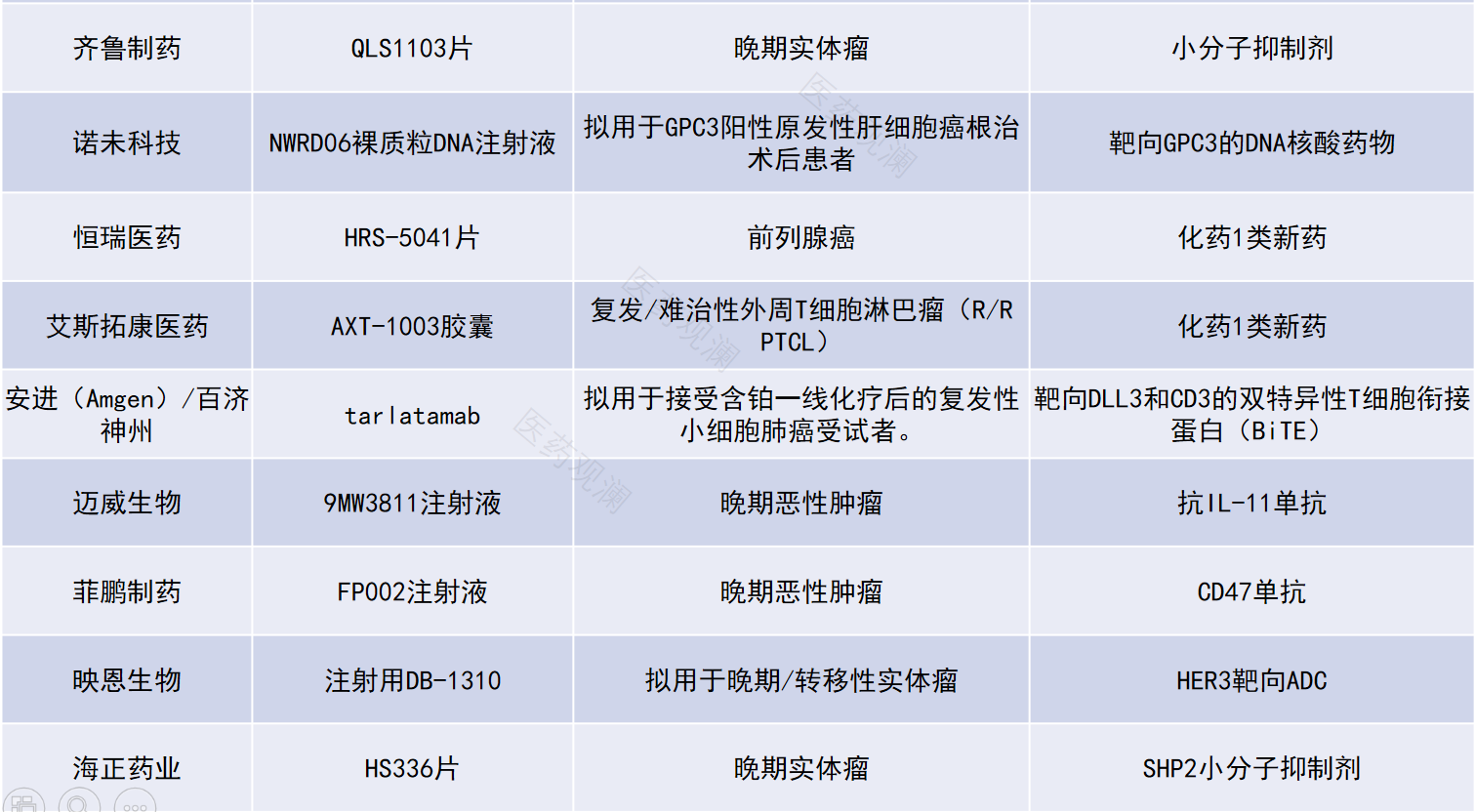
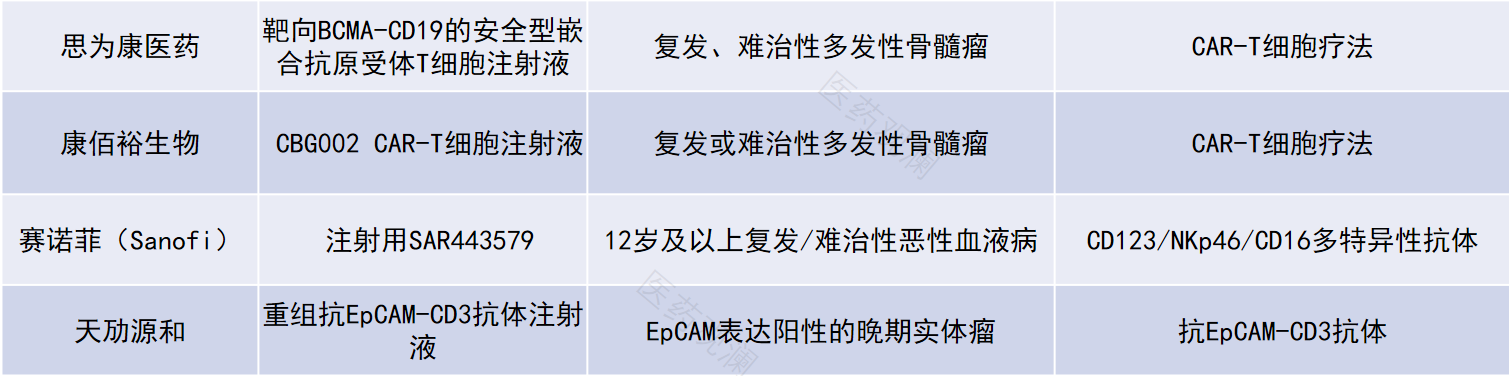
数据来源:CDE官网、各公司公开新闻稿。统计日期范围:5月1日~5月30日。本表根据公开资料梳理,如有遗漏,欢迎补充。
声明:本文系药方舟转载内容,版权归原作者所有,转载目的在于传递更多信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除内容