药企持续稳定的现金流,成为企业经营状态的“晴雨表”,而药品销售额则成为其重要组成部分。
为此,笔者特别统计了“2022全球化药销售额TOP100”榜单(按通用名计),以解读全球化药品种销售趋势及市场格局。据药智数据、药企年报等数据来源的统计,该榜单前100名销售额“门槛”为63亿元,超过百亿元的药品有62款,超过千亿元的药品有2款(奈玛特韦片/利托那韦、阿哌沙班),以下为具体销售额榜单数据。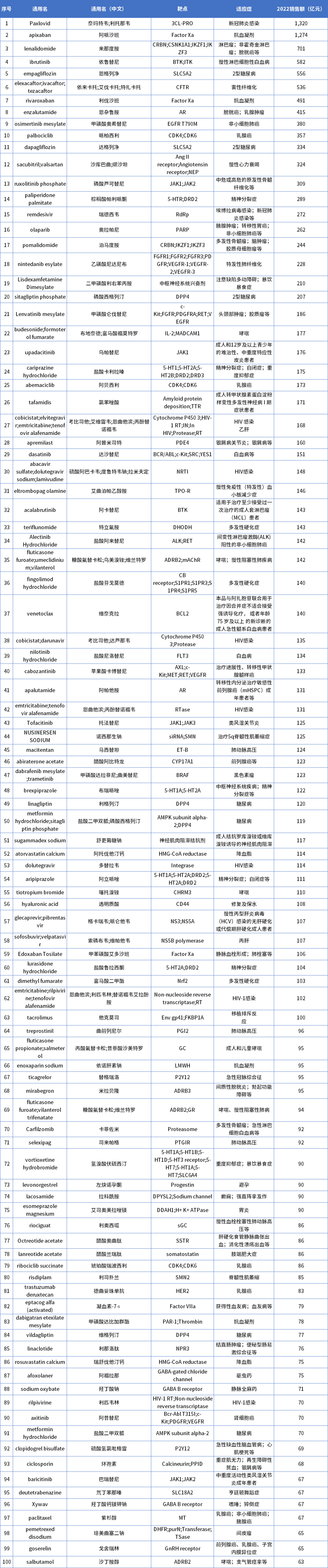
据该榜单,2022全球化药(按通用名计)销售额第一名为奈玛特韦片/利托那韦(1320亿元),其次为阿哌沙班(1274亿元),销售额皆超过千亿元,第三名来那度胺则为701亿元。具体来看,在统计的化药销售额榜单中:63亿元为上榜“门槛”,销售额60—100亿元的药品有38个,占比38%;销售额100亿元以上有62个,占比62%,百亿品种占据绝大部分比重。值得注意的是,化药销售额TOP100中,第1名1320亿元,第100名63亿元,两者差距较大,超过千亿元。从适应症来看,抗肿瘤领域占据绝大部分比例,包括来那度胺、恩杂鲁胺、甲磺酸奥希替尼、哌柏西利等超3百亿元销售的化药。抗感染领域为跃升黑马,比如榜单第一名抗病毒药物奈玛特韦片/利托那韦。从TOP5品种来分析,Paxlovid(奈玛特韦片/利托那韦)、Apixaban(阿哌沙班)、Lenalidomide(来那度胺)、Ibrutinib(依鲁替尼)、Empagliflozin(恩格列净)为榜单前五名。面对全球严峻复杂的疫情防控形势,抗病毒药物Paxlovid(简称P药)引起全球广泛关注。据悉,口服新冠药物Paxlovid于2021年12月获FDA紧急使用授权,仅2022年一年,其销售额猛增1320亿元,其火爆程度远超市场想象。据辉瑞2023年一季度财报显示,Paxlovid一季度销售额为291亿元。“随着全球疫情基本结束,新冠药物市场将持续萎缩,P药销售额将受影响;预计心血管疾病类药物需求将持续增长,在今年的销售额TOP榜单中,以抗癌药物、心血管药物为主。”韩国嘉泉大学药学院费翔博士谈到。阿哌沙班是一种强效、口服有效的可逆、直接、高选择性的Xa因子活性位点抑制剂,其抗血栓活性不依赖抗凝血酶III。阿哌沙班可以抑制游离及与血栓结合的Xa因子,并抑制凝血酶原酶活性。原研产品阿哌沙班由百时美施贵宝和辉瑞公司联合研发,2012年12月被FDA批准在美国上市,2013年1月获CFDA批准上市,进入中国。基于其优异的临床数据,阿哌沙班全球销售额快速上涨,于2015年突破10亿美元大关,在2018年一举获得全球小分子药物销售第一名。“预计今年,阿哌沙班将持续优异的市场成绩,有望超越P药、成为第一。”一位不愿具名的医药博士说到,“但是,值得注意的是,Paxlovid今年第一季度的销售额为291亿元,远远超过华尔街预期的192亿元。与2022年同期相比也增加了199亿元。辉瑞将这一业绩归功于中国市场的强劲需求,以及在其他国际市场的新产品上市。并且,北半球的夏季即将结束,随着冬天的来临,新冠感染人数增多,可能会带动Paxlovid的销售。”来那度胺用于多发性骨髓瘤、骨髓增生异常综合征和套细胞淋巴瘤等,原研产品由美国Celgene生物制药公司开发,于2005年底获FDA批准上市。据数据统计,2016年,全球来那度胺销售额已经达到约495亿元,复合增长率高达102%。目前,来那度胺已成为全球治疗多发性骨髓瘤的推荐用药,被称为“新三大神奇药物”之一,据药智数据统计,国内已有双鹭药业(首仿)、正大天晴、齐鲁制药、扬子江药业等至少12家仿制药获批上市,竞争日益激烈。依鲁替尼是一种Burton酪氨酸激酶(BTK)的小分子不可逆强效抑制剂,原研产品由Pharmacyclics和强生共同研发,于2013年获得FDA批准上市。该药物适应症广泛,包括套细胞淋巴瘤、小淋巴细胞淋巴瘤、慢性淋巴细胞白血病等11项,且随着适应症的扩大,销售一路猛涨,于2015年突破10亿美元,随后6年间增长了8.8倍。恩格列净是高选择性的SGLT2抑制剂,拥有独特的不依赖胰岛素的降糖途径,即通过减少葡萄糖在肾脏的重吸收而从尿中直接排糖。除具有明确的降糖效果外,还能带来减轻体重、降低血压、降低尿酸的额外获益。原研产品由勃林格殷格翰和礼来共同开发,2014年8月被FDA批准在美国上市,2017年9月在中国获批上市。据药智数据统计,国内已有江苏豪森、四川科伦药业、正大天晴药业等12家仿制药获批上市。声明:本文系药方舟转载内容,版权归原作者所有,转载目的在于传递更多信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除内容

