
2023-08-25 15:23:04来源:医药魔方浏览量:1442
8月24日,南京方生和医药科技有限公司(以下简称“方生和医药”)宣布,其沙库巴曲缬沙坦钠片(商标名:一心坦®)获批上市。根据医药魔方数据库,这是我国首家申报的沙库巴曲缬沙坦钠片仿制药,也是全球法规市场首个通过自主创新突破原研专利壁垒成功获批上市的该品种药物。

沙库巴曲缬沙坦钠片是由诺华开发的重磅心衰产品(商品名:诺欣妥®),代表了心衰新药研发领域20多年来的重大突破。其临床价值也通过销售业绩充分体现:2023上半年Entresto全球销售额达到29.15亿美元,同比增长31%。
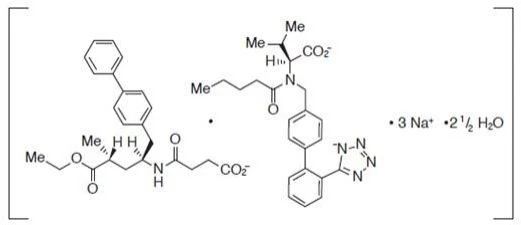
从分子结构上看,诺欣妥®是由沙库巴曲与缬沙坦按照1:1摩尔比例结合而成的盐复合物晶体(共晶药物),每个药物分子含有2.5个结晶水。诺华在中国市场为诺欣妥®分别申报了组合物专利(专利号:ZL201110029600.7)和晶型专利(专利号:ZL200680001733.0 / ZL201210191052.2),尤其是独特的晶型专利让诺欣妥®在中国市场的独占期可持续到2026年11月。
目前,诺华登记的沙库巴曲缬沙坦钠片组合物专利在中国已经被宣告无效(注:该专利近期在美国也已被无效),扫清了国内沙库巴曲缬沙坦钠仿制药上市销售的初步障碍,但真正制约国内仿制药厂家的其实是上述晶型专利。寻找一个稳定的新晶型并且做到生物等效有很高的技术门槛,对于两个分子形成的共晶化合物来说,更是如此。
医药魔方早在2018年就关注到了一心坦®在国内的申报并持续跟踪(见:首个Entresto仿制药惊现江湖!已完成BE试验,即将申请上市)。一心坦®是含有3个结晶水的新晶型,规避了原研含有 2.5 个结晶水的晶型专利障碍,从而实现了仿制药的合法提前上市。
放眼国内外,仿制药通过创新晶型突破原研专利壁垒提前上市成功案例不在少数,但由此产生的专利药和仿制药的法律诉讼纠纷也是一个绕不过的话题。事实上,创新和仿制的平衡是医药产业生态维持健康的基础保障。想要在保护原研药鼓励创新积极性与鼓励仿制药提高药物可及性之间做到平衡,就需要健全的法律体系。值得庆幸的是,我国在2021年7月终于颁布了《药品专利纠纷早期解决机制实施办法》,标志着我国的“专利链接制度”正式落地,为专利药和仿制药的和谐发展打下了良好的基础。
方生和医药官网上的一则新闻是很好的案例。方生和医药在2022年4月提交了达格列净片的仿制药上市申请,并按法规要求提出了4.2类专利声明(即:专利规避)。之后原研公司依据《药品专利纠纷早期解决机制实施办法》迅速提出了行政裁决请求,方生和医药也积极应对,2023年1月国家知识产权局发出了药品专利纠纷行政裁决结案通知书,原研公司撤回了该行政裁决的请求,意味着方生和医药在产品获批之前解决了专利纠纷的风险。
随着中国医药市场与欧美成熟药品市场在药品监管政策、数据保护政策、知识产权保护、市场保护政策等领域的全方面接轨,以及法律制度愈发的完善,中国医药市场会更加成熟,类似一心坦®这样的药物加快上市也会进一步拓展中国患者对创新药物的可及性。
声明:本文系药方舟转载内容,版权归原作者所有,转载目的在于传递更多信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除内容