
2024-03-20 09:31:28来源:RNAScript浏览量:1639
从2016年起,小核酸药物的上市数量持续增多,迎来了快速发展阶段。回顾近两年,小核酸药物维持至少两款的上市频率,不断扩充产品阵容,2023年有4款小核酸突出重围,走上商业化之路。截至目前全球已有19款小核酸药物获批上市。小核酸全球总销售额从2016年的0.1亿美元增长至2023年的43.2亿美元。而Evaluate Pharma和BCG则大胆预计2024年全球小核酸市场规模将达到86亿美元。除去Kynamro、Vitravene、Macugen三款产品因销售额过低而退市,目前在市产品共包含9款ASO、6款siRNA药物和1款RNA适配体药物,治疗领域主要集中在进行性肌营养不良症(DMD)、罕见的血脂异常、脊髓性肌肉萎缩症(SMA)、肌萎缩侧索硬化(ALS)等罕见病领域。
目前,已上市小核酸药物的研发企业高度集中,Sarepta、Ionis和Alnylam呈“三足鼎立”之势,Sarepta与Ionis 雄霸ASO产品市场,而Alnylam近乎垄断siRNA市场。与此同时,葛兰素史克、诺和诺德、武田等不少制药巨头也果断投身小核酸药物赛道,并加快管线布局。
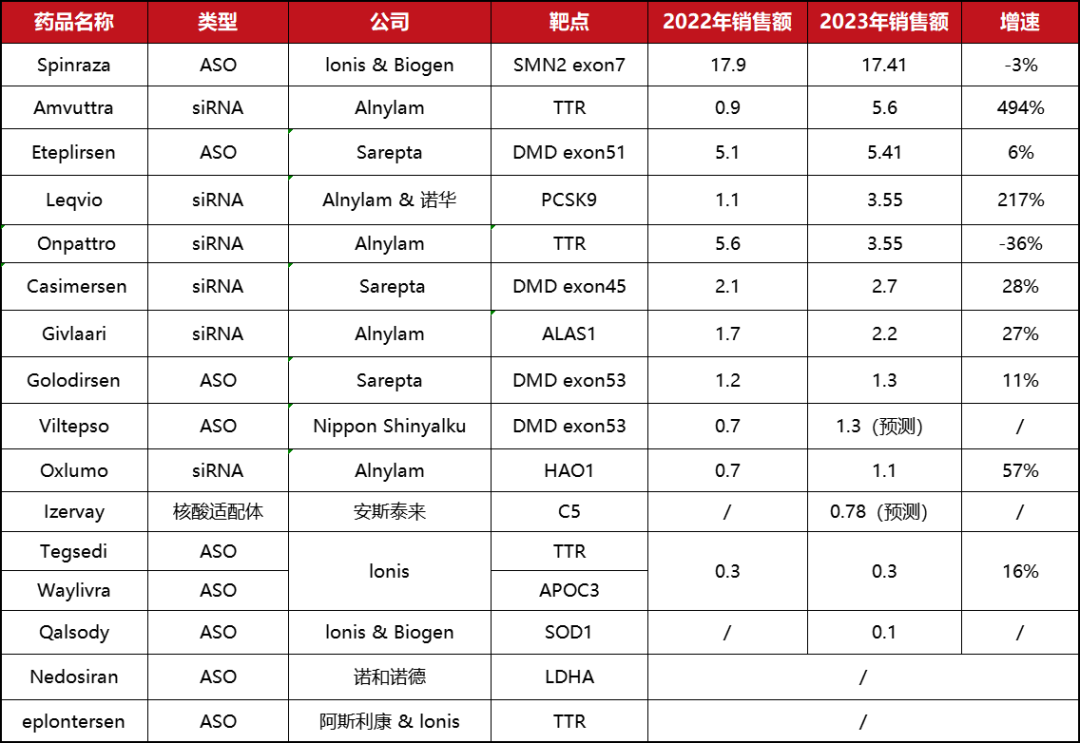
▲ 2023年全球小核酸药物销售额(亿美元)
(图片来源:星耀研究院整理)
从2023年的销售额排名来看,Biogen/Ionis旗下的Spinraza虽然销售额存在小幅下降,但依然凭借全球首个脊髓性肌萎缩症(SMA)治疗药物以及全世界最贵小核酸的头衔牢牢占据第一排名,市场的高认可度与高定价使其销售额远超第二、三、四名之和。
Alnyalm的Amvuttra反超老牌产品Onpattro,成为Alnylam新的销售担当,更是首次超过Sarepta的Eteplirsen,取得亚军位置;Leqvio(inclisiran)持续放量,升到了第四名。从增速来看,Amvuttra、Oxlumo以及Leqvio三款药物增速明显,同比增速分别为494%,57%,217%,而这三款产品都是Alnylam研发或合作的产品。另外值得一提的是,Alnylam的两款TTR靶点产品管线创造了近10亿美元的销售额,占总营收过半。在“三足鼎立”的格局下,Alnylam的发展潜力更是不可限量。
销售额前10的小核酸药物
Spinraza
Ionis & Biogen合作开发的Spinraza 2023年销售额17.412亿美元,相比2022年销售额下降2.92%,其市场占比主要受到了诺华的Zolgensma和罗氏的Evrysdi的冲击。
Spinraza是全球首个SMA治疗药物,于2016年12月获批上市。据悉,Spinraza在美国的标价为每次注射11.8万美元,这使得第一年的治疗成本为70.8万美元,之后每年为35.4万美元,是目前全世界上市的最贵的小核酸药物。但高昂的价格并未阻止市场对Spinraza的高涨热情。2019年2月,Spinraza进入中国,成为国内首个获批治疗SMA的药物,注射液参考价格为69.7万一支,低于美国售价。在2022年1月1日纳入国家医保正式执行后,Spinraza降至3万多/针。
Amvuttra
2022年6月上市的Amvuttra(vutrisiran)由siRNA药物龙头企业Alnylam开发,2023年销售额为5.6亿美元,同比大涨494%,排名升至第二位。
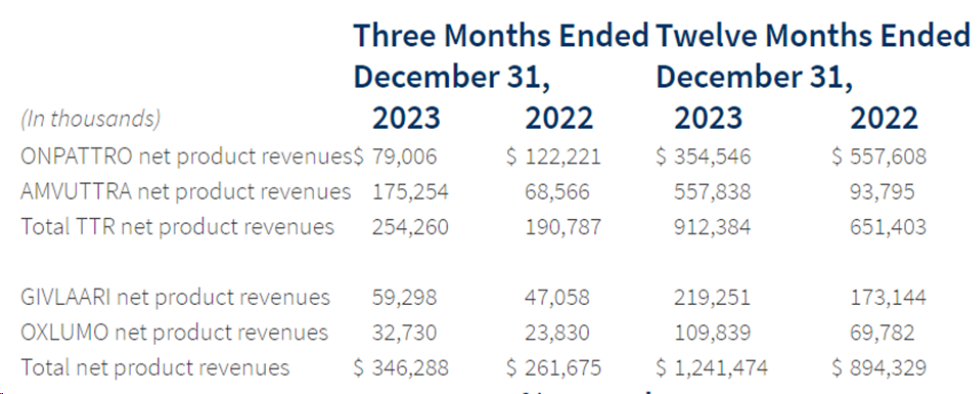
Amvuttra是首个治疗遗传性转甲状腺素蛋白淀粉样变性伴多发性神经病(hATTR-PN)患者的药物,也是首个FDA批准的能逆转神经损伤的、长效的RNAi治疗药物。相比Onpattro,Amvuttra制造成本低、不需要频繁的给药并且拥有着皮下注射的便利性。
除了已获批用于治疗hATTR-PN,Alnylam正在努力推进Amvuttra针对转甲状腺素蛋白淀粉样变性心肌病(ATTR-CM)的临床研究,Alnyam预计该市场患者数量至少是已获批适应症ATTR-PN的五倍。
Eteplirsen
由Sarepta开发的Eteplirsen(exondys 51)凭借5.41亿美元销售额位列2023年小核酸销售第三,同比增加6%,销售稳定增长。
Eteplirsen于2016年9月19日获批上市,成为首个获批治疗杜氏肌营养不良症(DMD)的药物,也是第一款获批的使用PMO改造的反义寡核苷酸,适用于已确诊DMD基因突变且适合外显子51跳过的患者。
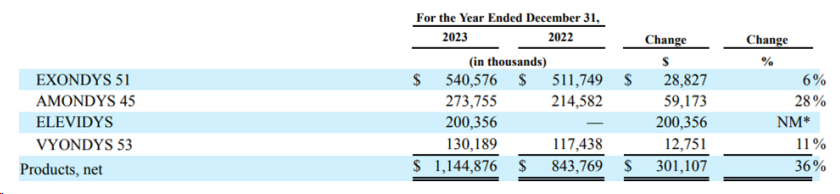
Eteplirsen通过诱导缺陷基因变异中的外显子跳跃来介导其作用。Eteplirsen选择性地与肌营养不良蛋白前mRNA的外显子51结合,在适合于外显子51跳跃的基因突变的患者中的mRNA处理过程中排除该外显子。通过外显子跳跃,Eteplirsen恢复DMD基因的开放阅读框,并允许产生功能性肌营养不良蛋白。
Leqvio
2023年,RNAi降胆固醇新药Leqvio(inclisiran)的总销售额达到3.55亿美元,同比上涨217%——成为诺华重要的销售额增长动力之一。诺华表示,Leqvio早期在中国的自费市场也取得了不错的成绩。
Leqvio于2021年12月取得FDA批准,用于治疗接受最高耐受剂量他汀疗法后,仍存在高水平低密度脂蛋白胆固醇(LDL-C)的成人患者。Leqvio是诺华斥资97亿美元收购The Medicines Company获得,Alnylam作为该药物的原研企业,仍拥有其全球净销售额的10%销售分成。目前,Leqvio已经在全球94个国家/地区获得批准,诺华还在扩大其批准范围,加强患者入组、消除准入障碍和加强医学教育,进一步增强Leqvio的销售潜力。
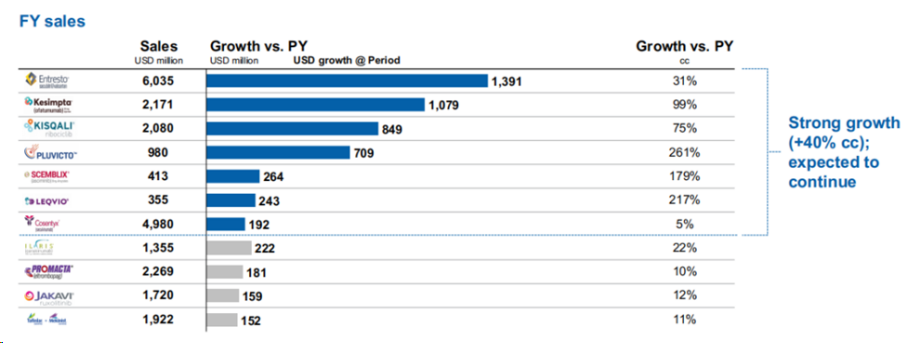
Leqvio能在短期内迅速放量,与小核酸药物独特的优势密切相关。相较于 PCSK9单抗,同样靶向PCSK9的Leqvio不仅实现了与其相差不大的降血脂效果,还大大降低了给药频次(每年仅需两次注射给药),相比需要每两周或每月给药一次的PCSK9 单抗,患者依从性更好。这都得益于化学修饰和以GalNAc为代表的的递送系统,大幅提升了小核酸药物的稳定性和递送/入胞效率,使得给药方式、频次和剂量得到大幅优化。
Onpattro
由Alnylam开发的Onpattro是首款获得FDA批准上市的商业化RNAi治疗产品,在2023年的销售为3.55亿美元,同比下降36.4%。主要是由于药物迭代导致的销售下跌,新一代药物Amvuttra给药间隔时间长,患者的依从性更好,患者快速完成换药后,Onpattro销售下跌,Amvuttra迅速上涨。
为了避免Onpattro失去商业价值,Alnylam公司曾尝试扩大Onpattro的适应症标签。去年2月,Alnylam向FDA提交新药补充申请(sNDA),将Onpattro扩充应用于治疗转甲状腺素蛋白淀粉样变性心肌病(ATTR-CM),但遗憾因“没有明显的临床治疗效果”被美国 FDA拒绝。
Casimersen
由Sarepta开发的Casimersen(amondys 45)2023年销售额2.7亿美元,同比增长28% ,位列榜单第六位。
Casimersen于2021年02月25日获FDA批准,用于外显子45跳跃基因突变的DMD患者。Amondys 45成为继Exondys 51 和Vyondys 53之后,第3个在美国获批的DMD基因突变的ASO疗法,这也是FDA首次批准用于治疗这种突变患者的靶向疗法。
Givlaari
由Alnylam开发的Givlaari 2023年销售额2.2亿美元,同比增长27%,位列第七。
2019年11月,FDA批准givosiran上市,用于治疗成人急性肝卟啉症(AHP)。截至2023年底,全球有超过650名患者正在接受商业化Givlaari治疗,超过430名患者正在接受商业化Oxlumo治疗。
Golodirsen
由Sarepta开发的Golodirsen(vyondys 53)2023年销售额1.3亿美元,同比增长11%,位列第八。
Golodirsen是一种Sarepta专利磷酰二胺吗啉代低聚体化合物,被设计为可以与抗肌萎缩蛋白前体mRNA的第53外显子相结合,从而在mRNA剪接时排除或“跳过”这一外显子。
Viltepso
NS Pharma(日本新药)的Viltepso(viltolarsen)官网公布了2023年的销售额预测数据,2023年4月-12月实际销售额13,225百万日元,预计2023年全年销售额18,300百万日元(约1.3亿美元),位列第九。
Viltepso是一种反义寡核苷酸(ASO)药物,通过跳过外显子53,使部分患者DMD基因的移框缺失变为同框缺失,以减轻症状,可以与DMD基因的pre-mRNA 53号外显子位置相结合,在形成成熟mRNA后,切除53号外显子部分,从而部分修正mRNA读码框,给药方式为静脉输注给药。2020年3月25日,Viltepso首次在日本获批上市,同年8月19日在美国获批上市,用于治疗DMD基因发生53外显子跳跃基因突变的(DMD)。
Oxlumo
由Alnylam开发的Oxlumo(lumasiran)2023年销售额1.1亿美元,同比增长57%,位列第十。Oxlumo在2020年11月23日获美国FDA批准,这是FDA批准的第一款治疗原发性高草酸尿1型(PH1)药物。 同时,这也是Alnylam公司第三款获批的RNAi疗法。
Oxlumo是一种靶向羟基酸氧化酶1(HAO1)mRNA的RNAi疗法,HAO1参与编码乙醇酸氧化酶(GO),而GO是一种可导致PH1缺陷的上游酶。lumasiran通过降解HAO1 mRNA,减少GO的合成,抑制草酸生成。
结语
ASO是最早开发的小核酸药物类型,商业化发展更为成熟,在整体小核酸药物中的份额较高。siRNA是继ASO之后小核酸领域最集中的研究方向,对于由基因异常表达或基因突变引起的疾病,如癌症、病毒感染和遗传疾病等的治疗具有巨大的应用潜力。而核酸适配体发展则较为缓慢,仅有1款上市。
已上市的小核酸药物适应症多集中在罕见病领域,如杜氏肌营养不良、脊髓性肌萎缩症等,患者群体有限。而长效降脂药Inclisiran(leqvio)开创了小核酸药物适应症走入慢性病的先河。各大企业正依托现有管线,围绕患者群体大的心血管代谢疾病适应症重点合作发力,预计未来随着适应症的持续突破,小核酸药物将迎来发展新拐点。
声明:本文系药方舟转载内容,版权归原作者所有,转载目的在于传递更多信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除内容


微信公众号

药方舟手机版

