
2024-11-12 13:53:20来源:医药观澜浏览量:1700
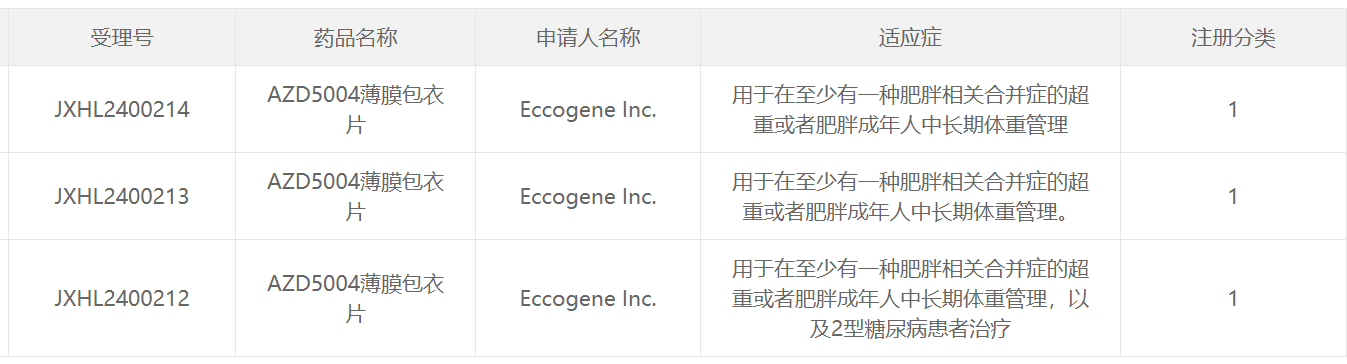 图片来源:CDE官网
图片来源:CDE官网
AZD5004是一款每日一次、低剂量的小分子GLP-1受体激动剂,该药物在临床前研究中证明具有理想的疗效和安全性。
2023年11月,阿斯利康与诚益生物达成独家协议,以潜在超20亿美元的总额获得ECC5004(即AZD5004),用于治疗包括肥胖症、2型糖尿病和其他合并症在内的适应症。阿斯利康将获得在中国以外的所有地区对ECC5004的任何适应症的开发和商业化的独家权利。在中国,诚益生物和阿斯利康将合作共同开发和商业化ECC5004。

此前的1期临床试验初步结果显示,与安慰剂相较,AZD5004在低剂量10mg与30mg展现积极的减重与血糖降低效果,并具有>70%的口服生物利用度以及良好的耐受性。
近日(11月5日),阿斯利康公布了AZD5004在患有2型糖尿病的肥胖患者中进行的1期临床试验的最新结果。数据显示,患者是否伴随食物服用AZD5004均不会影响它的药代动力学特征。探索性疗效分析显示,接受剂量为50mg的AZD5004治疗的患者中,4周后患者体重与基线相比降低5.8%,约为9.4斤。同时,患者的空腹血糖等指标也有所下降。
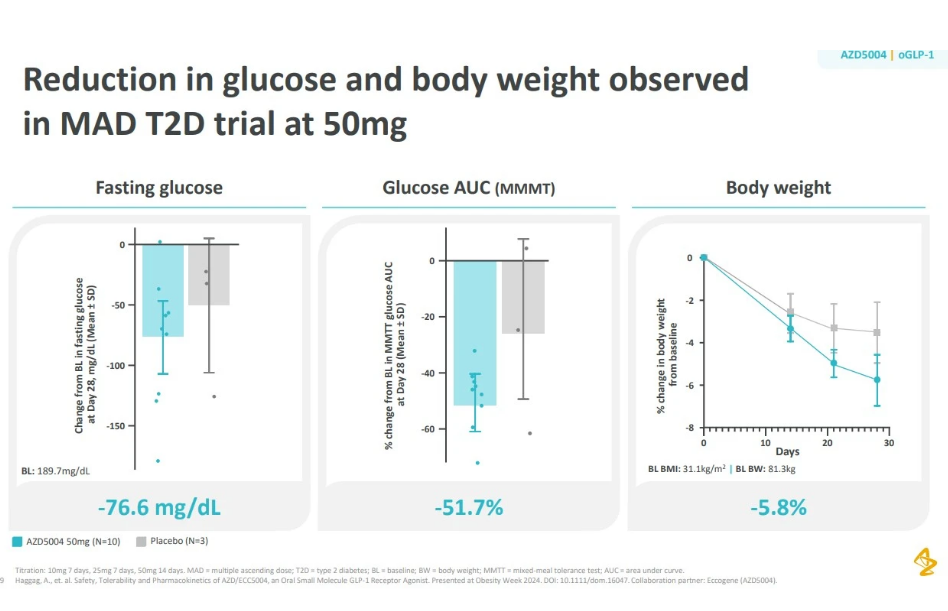
阿斯利康彼时的新闻稿表示,这些数据支持AZD5004进入2期临床试验,在患有和不患有2型糖尿病的肥胖患者中进一步评估其减肥效果。同时,该公司还计划将AZD5004与SGLT2抑制剂dapagliflozin联用,治疗2型糖尿病、慢性肾病和心力衰竭患者;AZD5004与口服PCSK9抑制剂AZD0780联用具有进一步降低高风险心血管疾病的潜力。
本次这款小分子GLP-1受体激动剂在中国也获批临床,意味着其即将在中国开展注册性临床研究。
声明:本文系药方舟转载内容,版权归原作者所有,转载目的在于传递更多信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除内容