
2025-02-27 18:01:38来源:药时空浏览量:3083
2月25日,Precigen宣布美国食品药品监督管理局(FDA)受理其HPV治疗性疫苗PRGN-2012的上市申请并授予优先审评资格,用于治疗复发性呼吸道乳头状瘤病(RRP),PDUFA日期为2025年8月27日。若顺利获批,其将成为首款针对RRP的治疗方案,也是首款HPV治疗性疫苗。
此前,PRGN-2012已获得FDA的突破性疗法和孤儿药认定,以及该机构的加速批准通道,同时还获得了欧盟委员会的孤儿药认定。
01 具有“数十亿美元的全球重磅炸弹潜力”
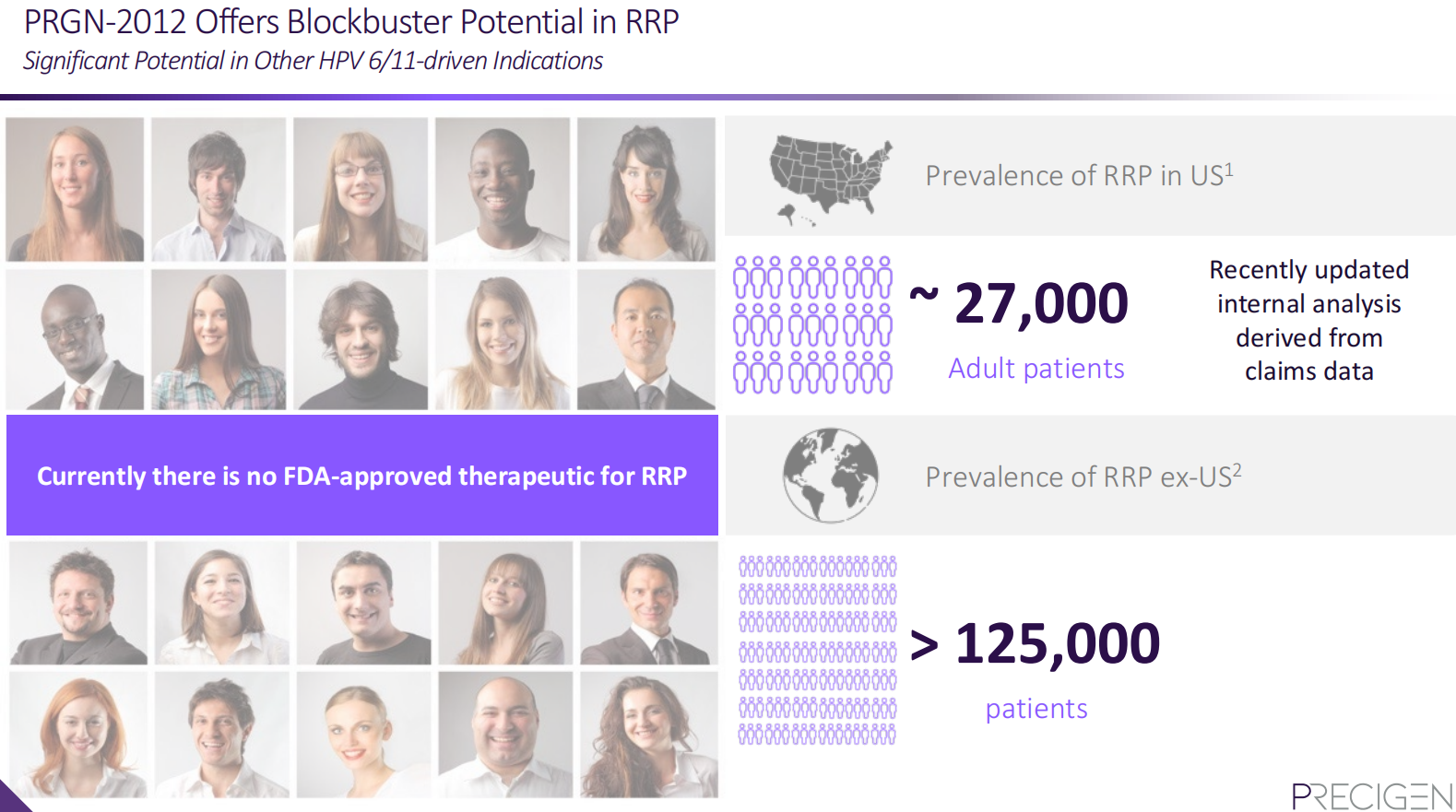
RRP是一种罕见疾病,由人乳头瘤病毒(HPV)6型或11型感染引发,是一种可危及生命的终身性上下呼吸道肿瘤疾病。据Precigen称,基于最新更新的内部分析,美国约有2.7万名成人患有RRP,美国以外的患者数量超过12.5万。目前,RRP患者的标准治疗方案包括多次手术。
PRGN-2012的通用名称为zopapogeneimadenovec,是一种基因疗法。Precigen预计,PRGN-2012具有“数十亿美元的全球重磅炸弹潜力”。不过,公司尚未向投资者透露该基因疗法的预计定价,但公司总裁兼首席执行官HalenSabzevari博士近期向《GEN Edge》表示,自去年夏季以来,公司一直专注于PRGN-2012的后期临床开发和最终商业化。7月,Precigen宣布任命PhilTennant为首席商务官,其首要职责是监督PRGN-2012潜在上市的商业筹备工作。
Sabzevari表示:“我们已基本组建好商业团队,Phil也已负责起商业工作。我们相信,一旦获得FDA批准,我们能够立即推出该产品。”她补充道,这项工作将涉及Precigen与在商业活动方面经验丰富的合作伙伴合作,这些合作伙伴将直接向公司的商业团队汇报:“这完全在我们的掌控之中。我们认为,这是最快、最有效的方式,而不是仅靠内部力量直接构建每一个环节。”
去年8月,Precigen在重新规划临床产品组合和资源优先级时,将推进PRGN-2012列为首要任务,在此过程中裁减了超过20%的员工。目前,Precigen约有100个工作岗位。尽管如此,公司计划在战略岗位上增加一些高管,特别是在商业医疗事务方面,“以满足我们目前对PRGN-2012的需求。”Sabzevari说。
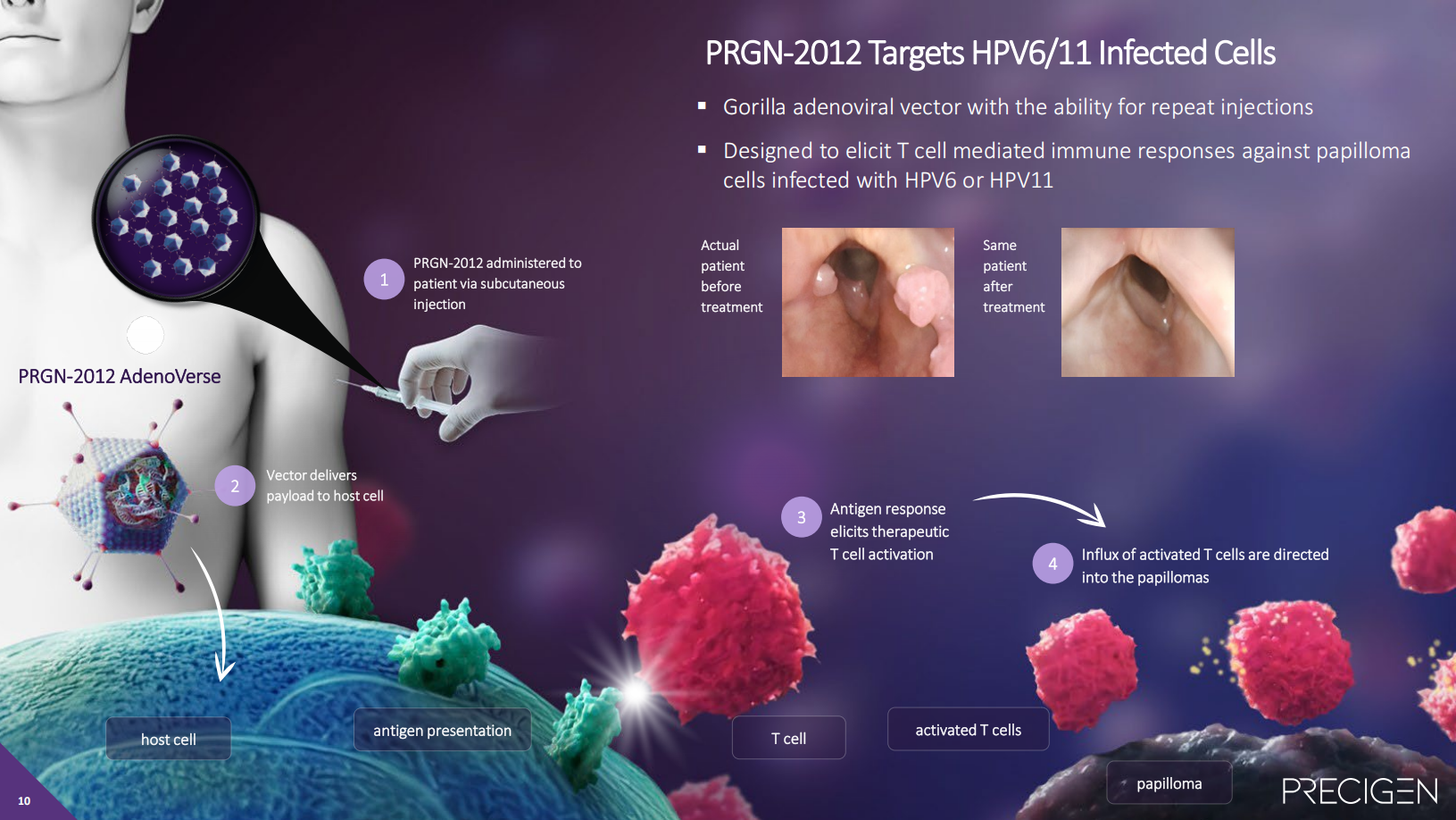
PRGN-2012是通过公司的AdenoVerse®平台开发的,该平台使用腺病毒载体库,用于高效传递治疗效应物、免疫调节剂和疫苗抗原,以调节免疫系统。Precigen表示,其AdenoVerse基因疗法已被证明能够产生高水平且持久的抗原特异性T细胞免疫反应,并且可以通过重复给药来增强这些反应。
Precigen公司的BLA申请得到了关键I/II期试验(NCT04724980)积极数据的支持。该试验结果于2024年6月在美国临床肿瘤学会(ASCO)年会上公布,并于上个月发表在《柳叶刀呼吸医学》杂志上。
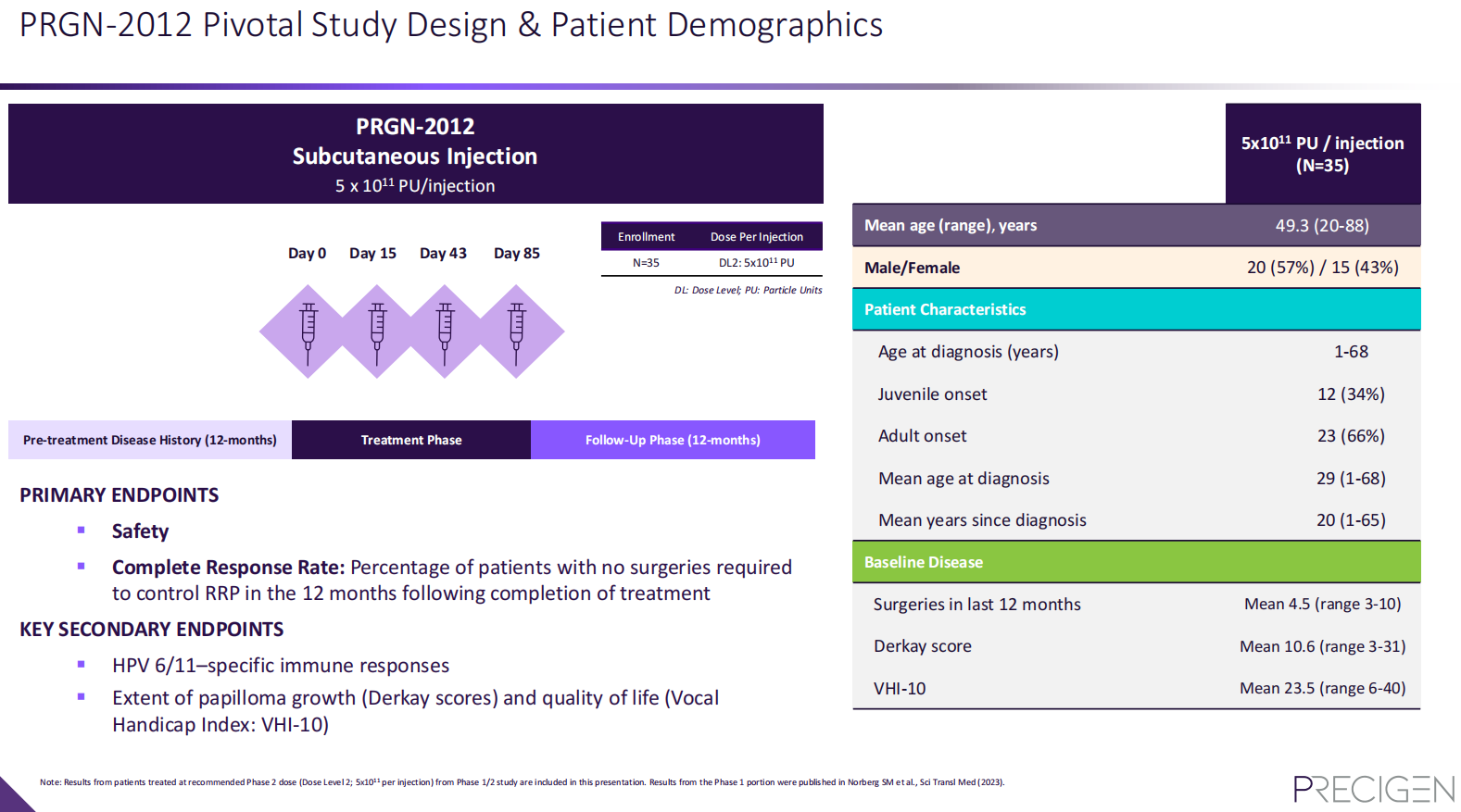
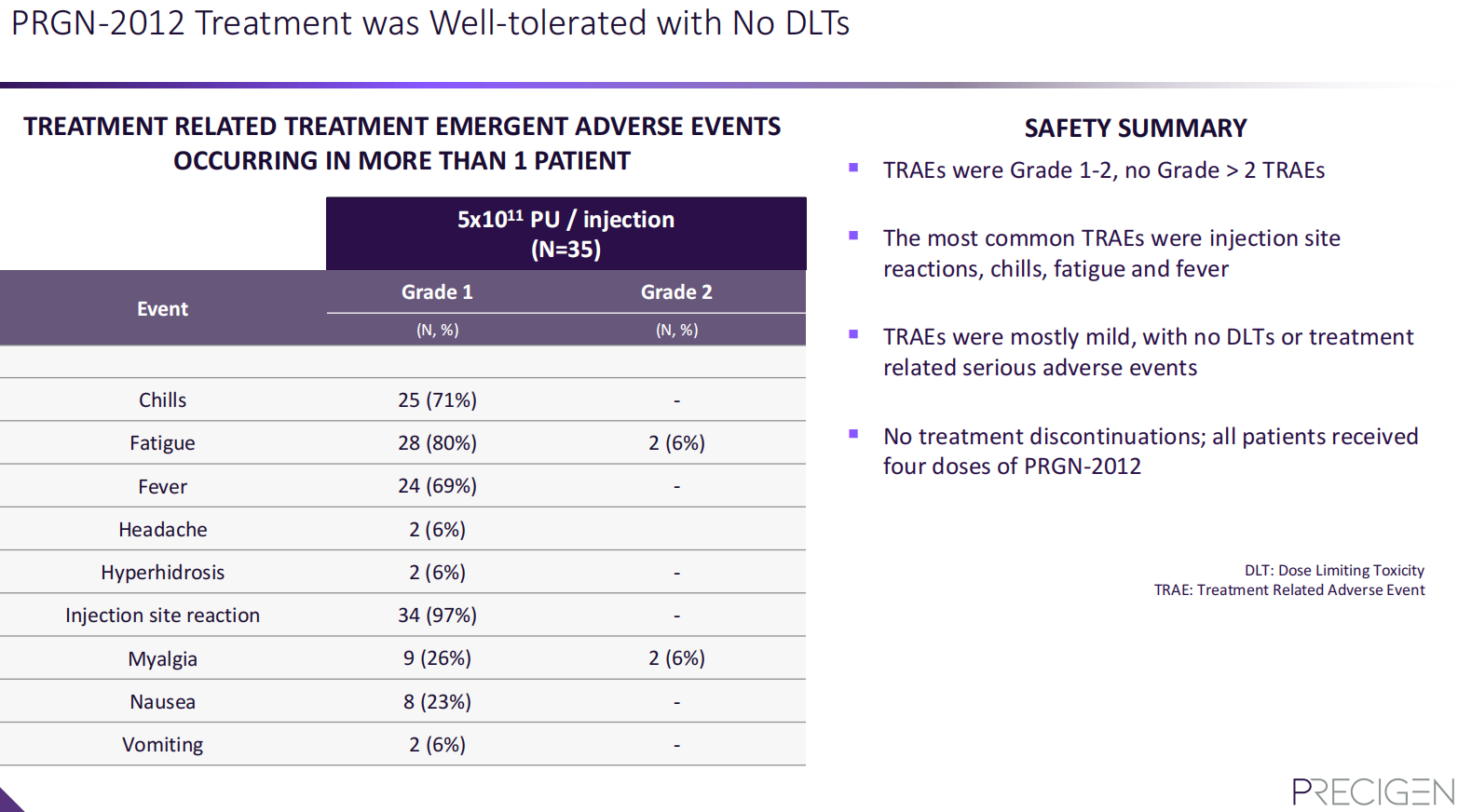
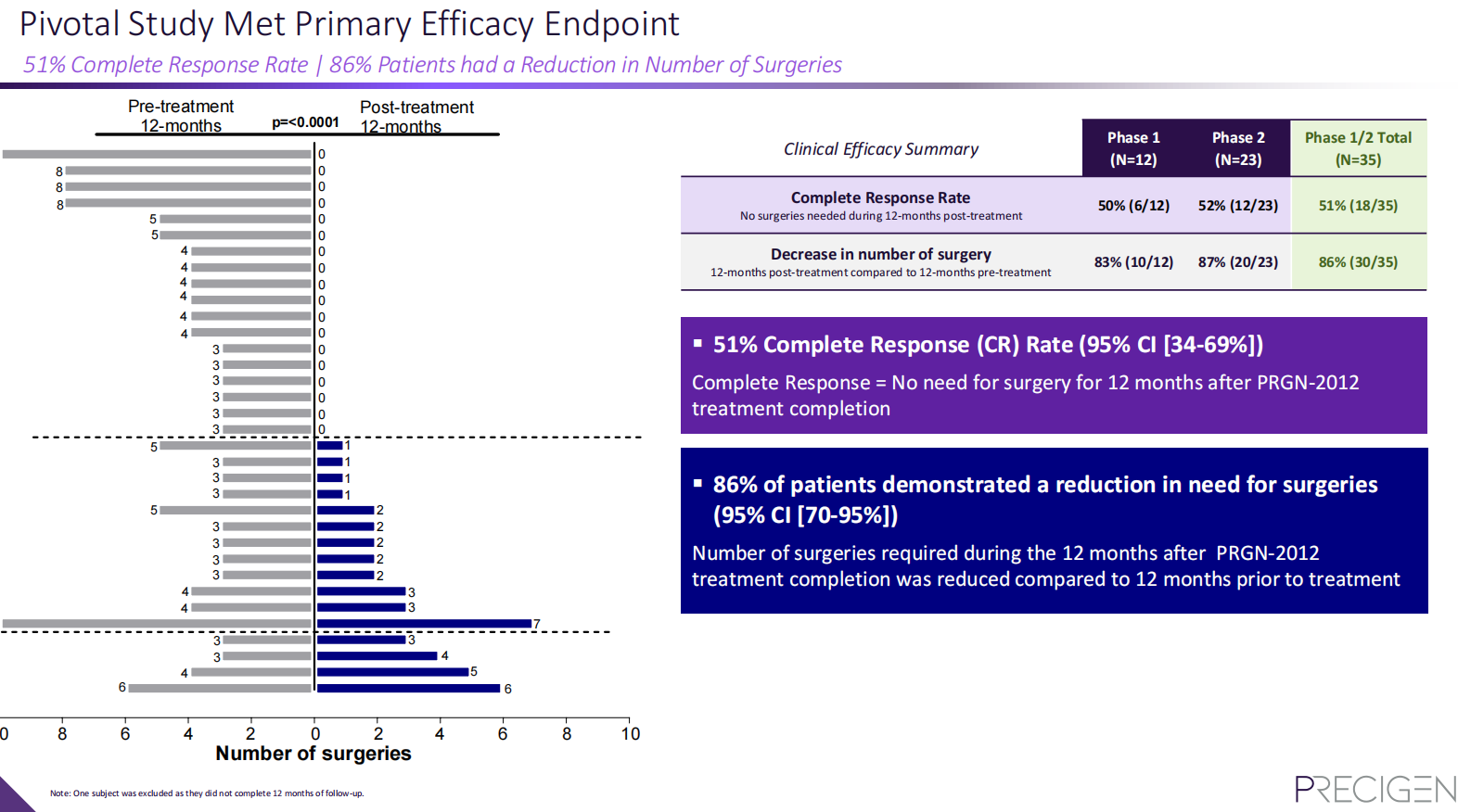
该试验达到了主要结果指标,35名患者中有18名(51%)实现了完全缓解,即治疗后12个月内无需干预来控制RRP的患者比例。与治疗前一年相比,35名患者中有30名(86%)在接受PRGN-2012治疗后的一年中手术干预次数减少。更令人鼓舞的是,接受PRGN-2012治疗的患者手术次数中位数从4次降至0次。
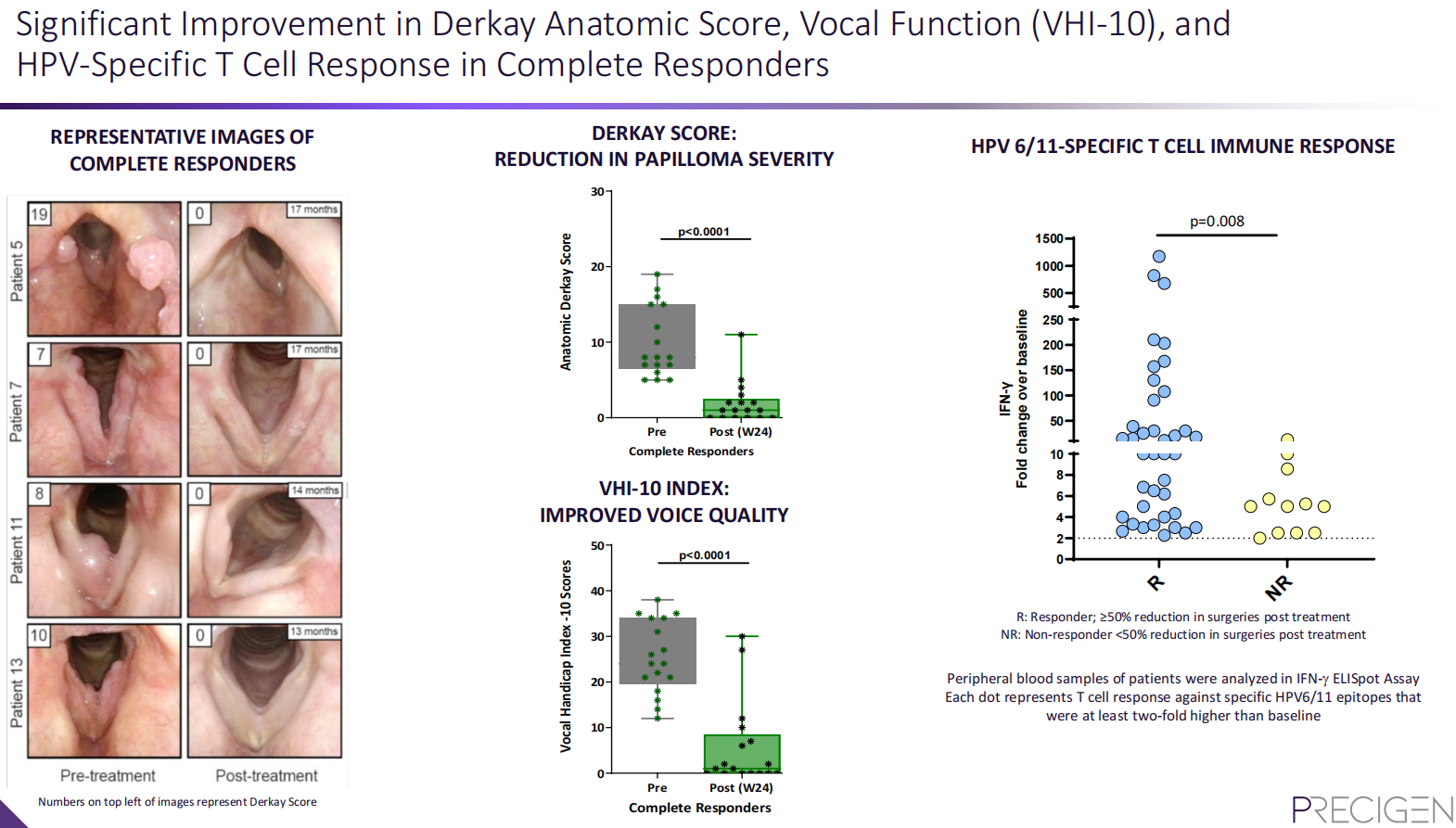
试验的关键次要终点包括针对HPV的免疫反应、通过Derkay评分衡量的乳头状瘤生长程度,以及通过声音障碍指数-10(VHI-10)衡量的生活质量。
此外,公司还有PRGN-2009的联合疗法,这是一种针对HPV癌症的首创AdenoVerse基因疗法,加上默沙东的重磅癌症免疫疗法Keytruda®(pembrolizumab。该组合正在进行新诊断的HPV相关口咽鳞状细胞癌(OPSCC)的II期试验(NCT05996523)和复发性或转移性宫颈癌的另一项II期研究(NCT06157151)研究。Precigen正在根据与美国国家癌症研究所(NCI)的合作研发协议(CRADA)进行这两项试验。

02 HPV治疗性疫苗在研情况
根据美国临床信息公示数据库(www.clinicaltrials.gov)统计结果,截止到2024年2月21日,已经完成和进行的治疗性HPV疫苗临床试验有90多项,共包含30多种疫苗产品。目前尚无治疗性HPV疫苗被批准上市。根据技术路线不同,候选治疗性HPV疫苗主要分为蛋白疫苗、多肽疫苗、DNA疫苗、RNA疫苗、活载体疫苗和细胞疫苗等。
其中,全球7种候选治疗性HPV DNA疫苗包括VGX-3100、INO-3112(MEDI0457,VGX-3100的升级产品)、GX-188E、VB10.1、pBI-11、NWRD08以及pNGVL4aCRTE6E7L2。VGX-3100、INO-3112是Inovio公司的产品,据悉,Inovio的HPV DNA疫苗也将在今年中递交RRP的上市申请。
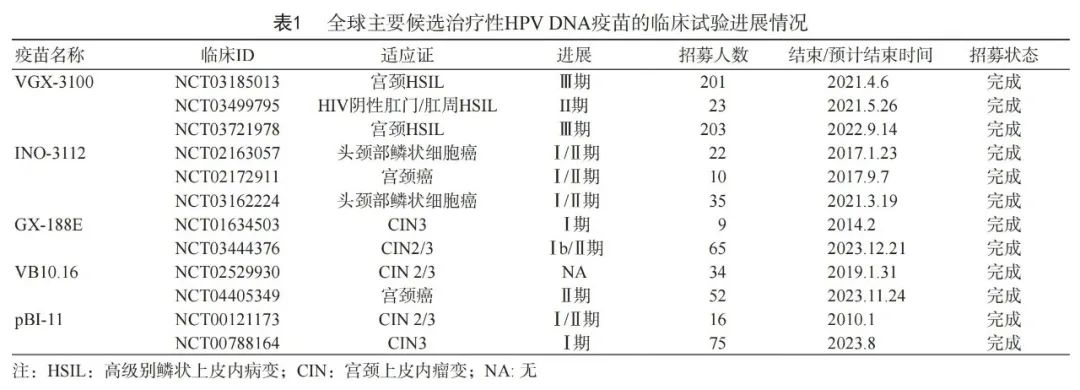
至于国内,也已有多家企业布局HPV治疗性疫苗,如东方略(引进Inovio的VGX-3100),还有奥罗生物、诺未生物、石药集团、阿法纳生物、仁景生物等的HPV mRNA治疗性疫苗,均已进入临床阶段。
声明:本文系药方舟转载内容,版权归原作者所有,转载目的在于传递更多信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除内容