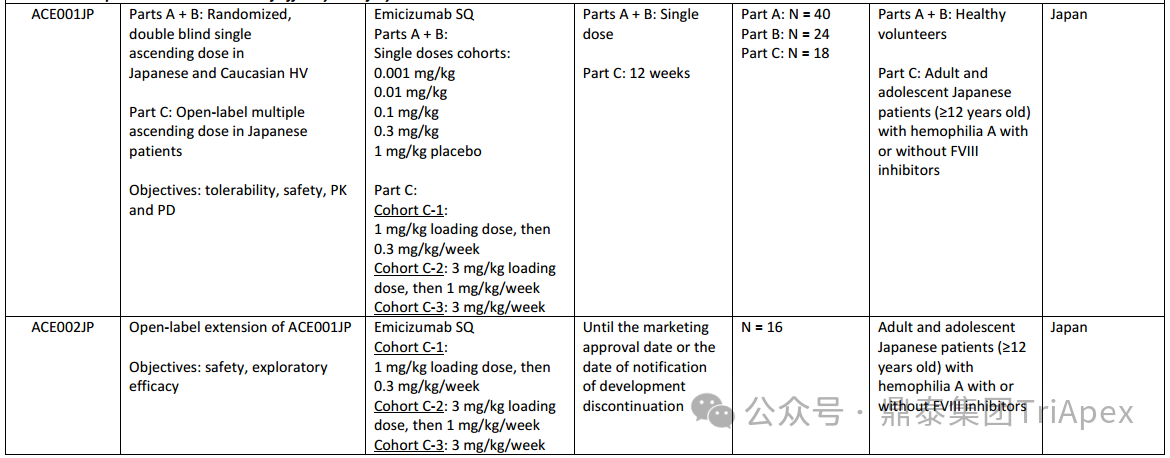
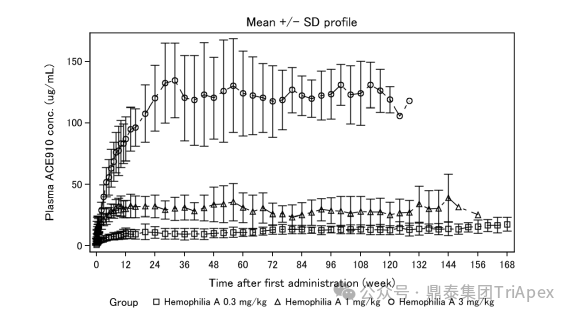
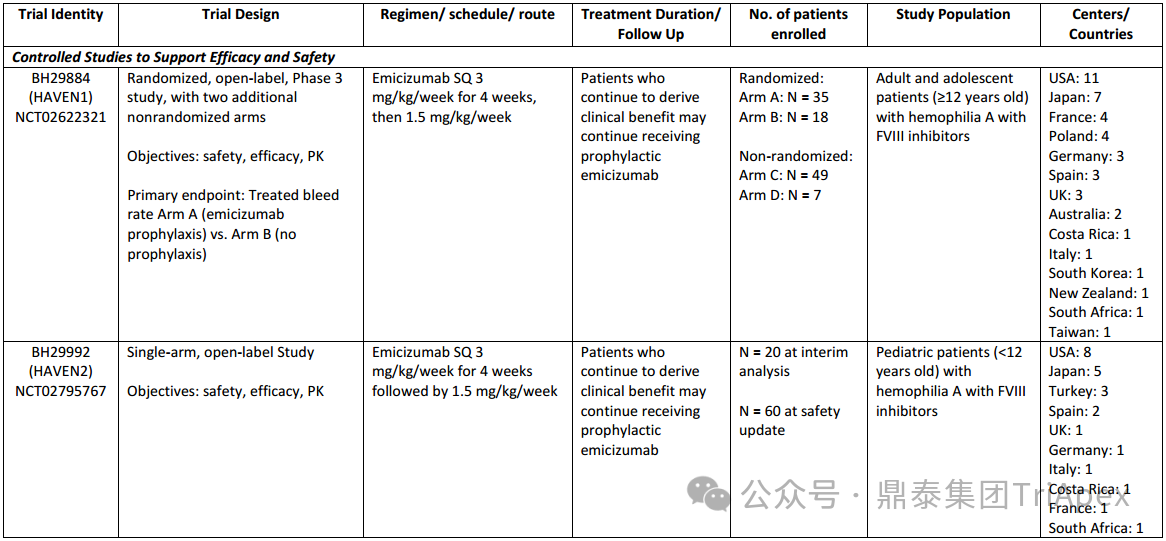
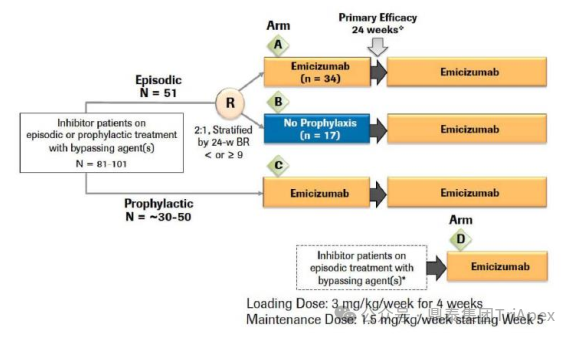
2025-11-27 14:15:20来源:鼎泰集团TriApex 浏览量:778
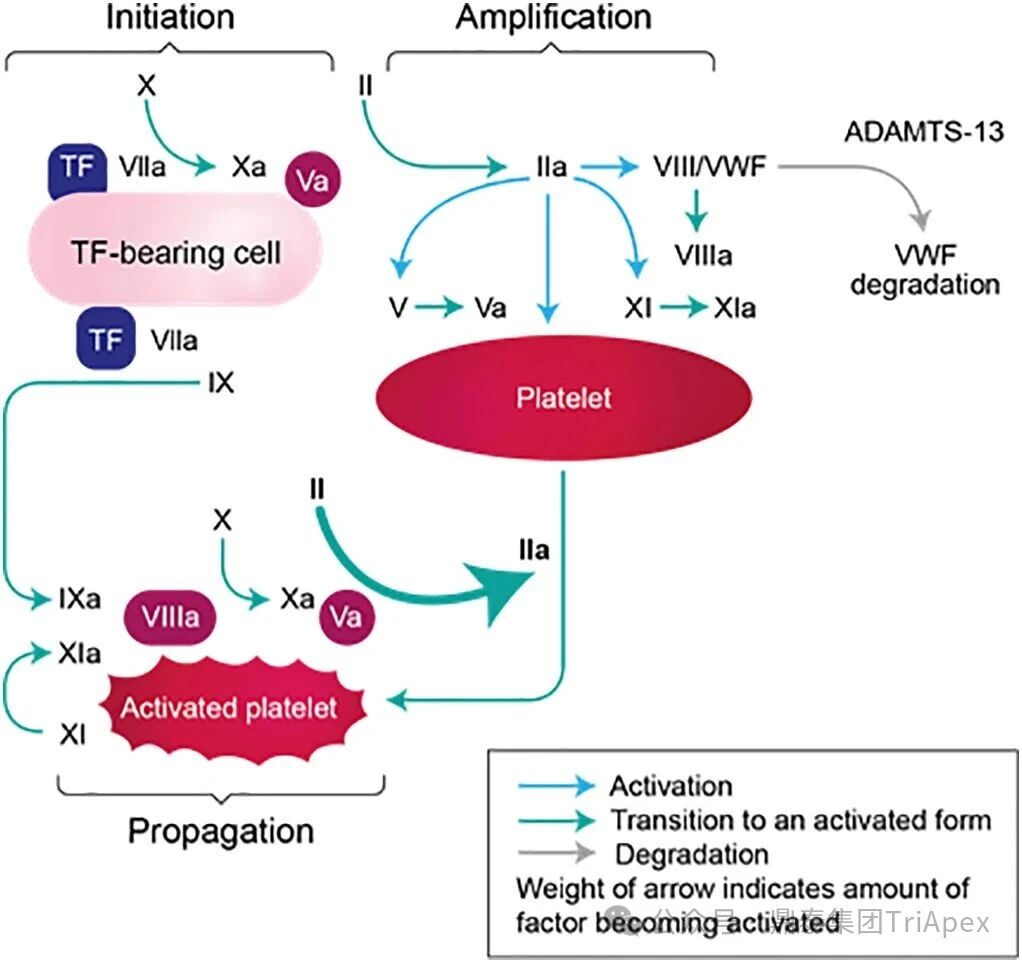
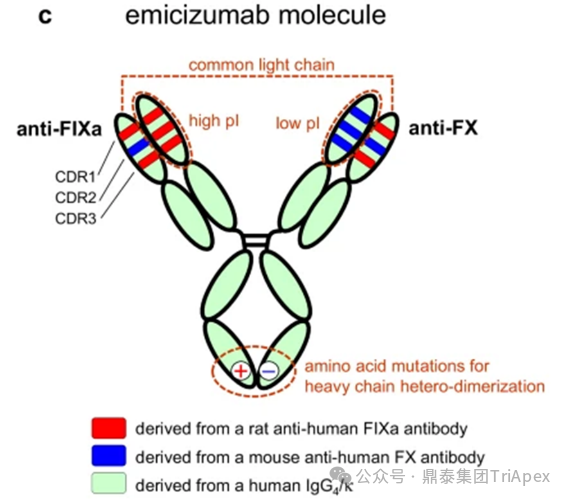
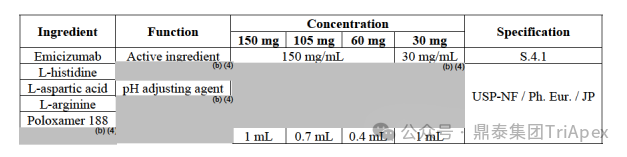
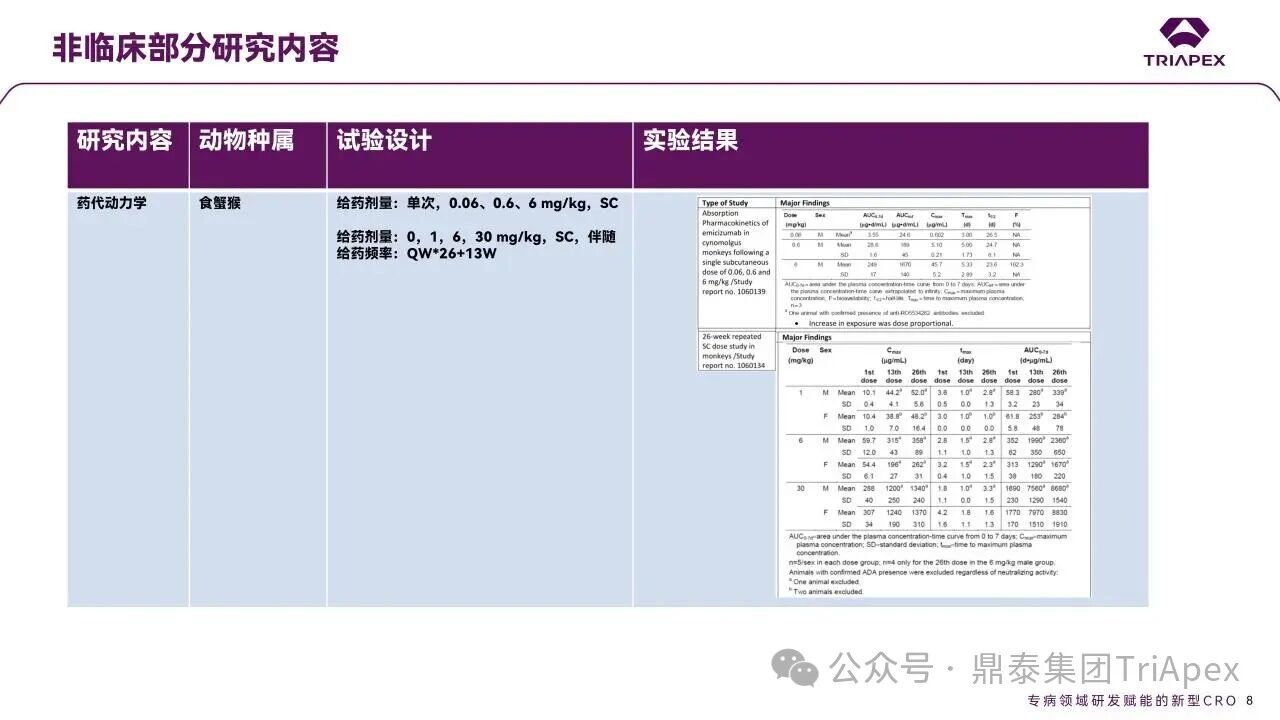
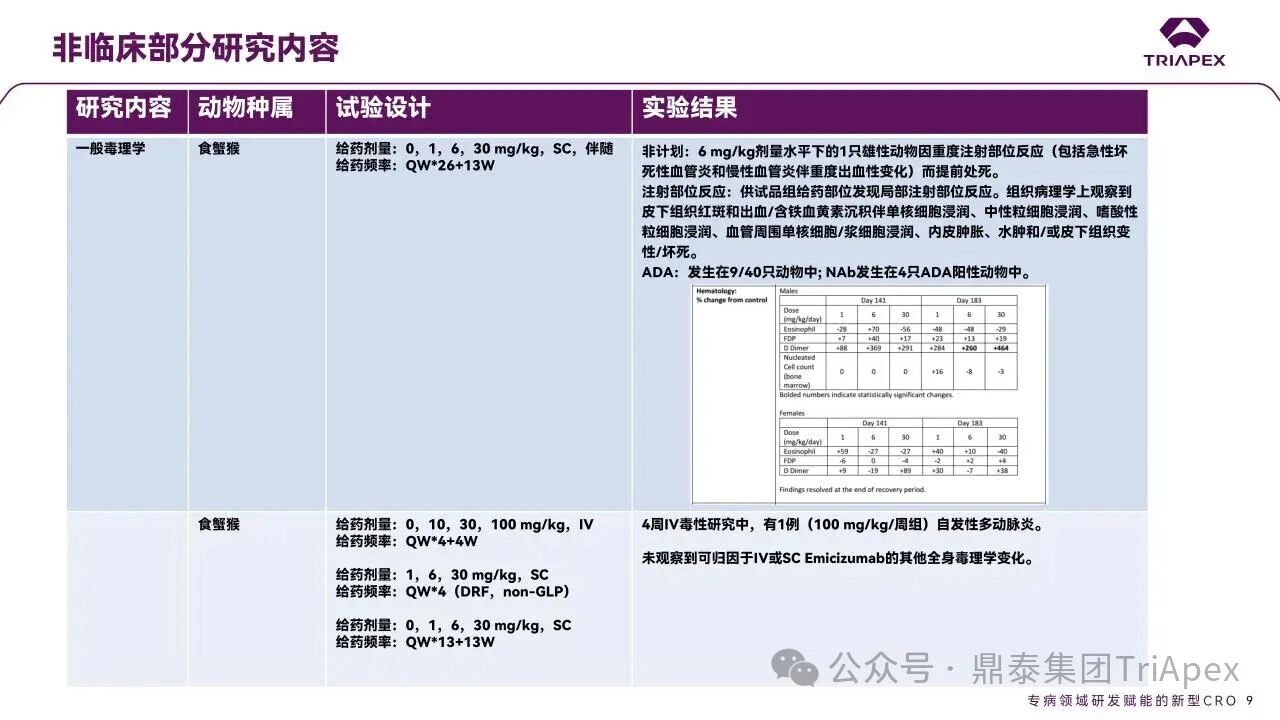
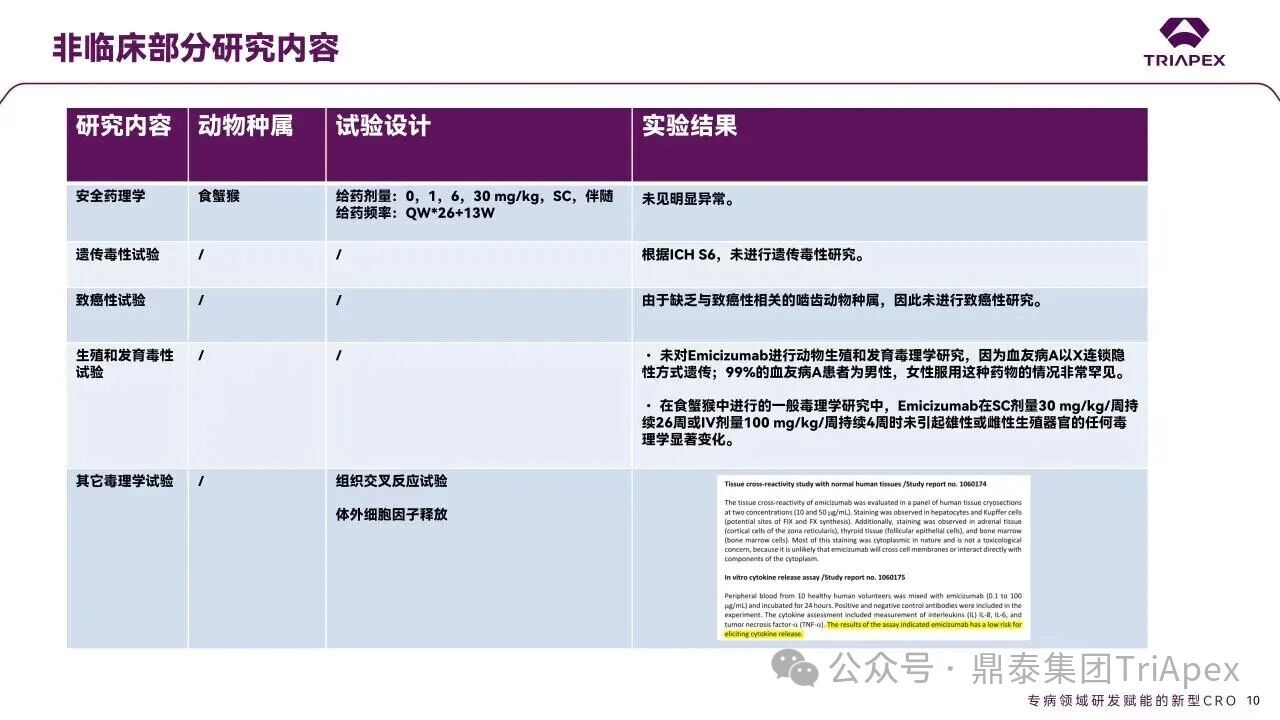
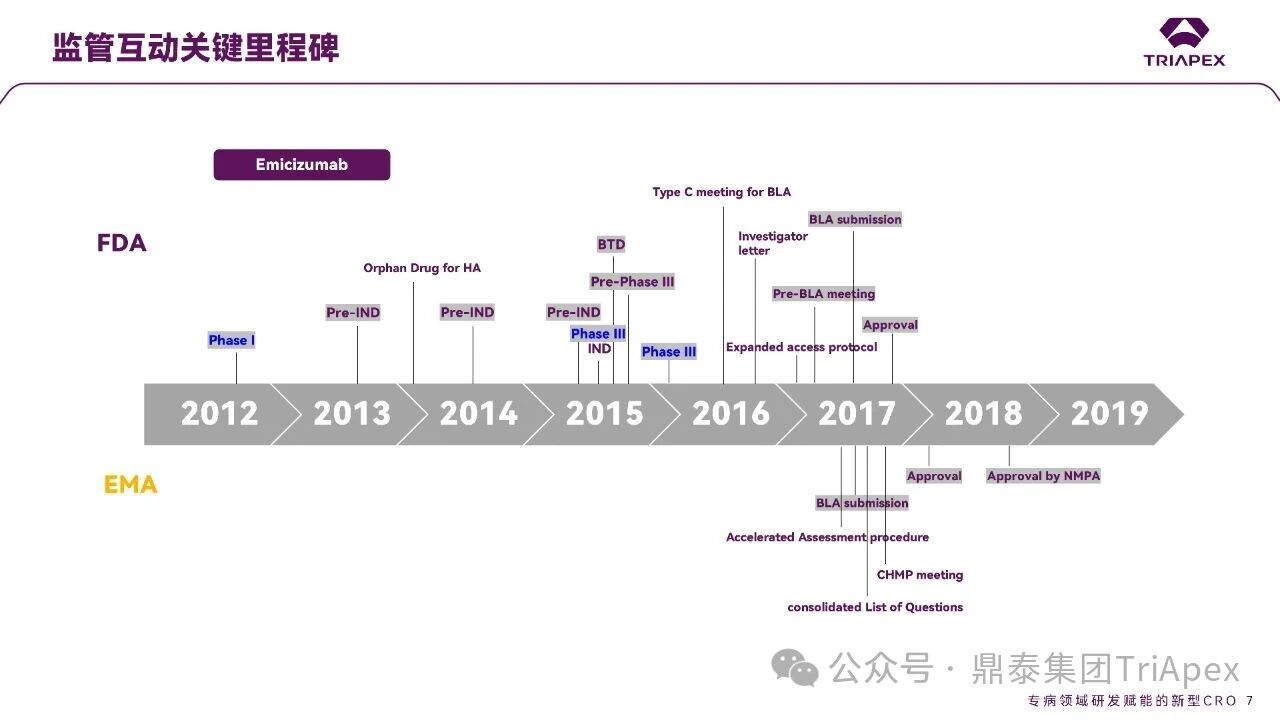
Emicizumab,关键质量属性,非临床&临床试验设计,生物类似药,科学考量 全文共:8348 字 19 图 预计阅读时长:25 分钟 艾美赛珠单抗(Emicizumab)是 FDA 批准的首个用于治疗体内存在凝血因子 Ⅷ 抑制物的 A 型血友病的新药,也是目前国内获批上市的唯一一款适用于伴有凝血因子 Ⅷ 抑制物的 A 型血友病患者的预防性治疗药物。因为半衰期长、合理给药方案下体内药物浓度恒定且适用于体内存在凝血因子 Ⅷ 抑制物的患者,该药改变了此前这类患者无有效预防性药物可用的局面。艾美赛珠单抗从递交 IND 申请到 2017 年首个适应症获批上市历时约 4 年。其临床开发路径、药政策略和相关的支持性非临床研究具有重要的参考价值。 随着专利临期,艾美赛珠单抗生物类似药的研发如火如荼,国内已有多家企业正在进行布局。在前期文章《生物类似药非临床研究 —— 从原则性要求到审评实践的演化》(点击查看原文)中,鼎泰团队系统梳理了生物类似药研究的基本路径和申报资料、中外法规和技术指导原则层面的比较、质量比对研究的重要性,并对已上市生物类似药非临床研究内容进行回顾。对于具体品种(如艾美赛珠单抗)生物类似药如何开展非临床研究,仍是长期以来困扰我们的难题。 恰在近期(2025年10月29日),FDA 更新了简化生物类似药开发的科学考量指南草案,确定在某些特定条件下无需开展与参照药的对比性临床研究,质量比对研究 +PK+ 免疫原性评估足以支持论证相似性。 基于此,本期内容将对艾美赛珠单抗的上市历程及临床开发路径进行复盘,结合 FDA 更新的简化生物类似药指南草案对其生物类似药的研发思考进行分享,以期对深度理解该产品和指导其生物类似药的开发提供借鉴。 声明 本文仅为行业科普及学术研究用途,不构成对任何药品、医疗器械或相关产品的推广、推荐或商业宣传。文中提及内容均基于公开资料,不涉及具体产品功效暗示或商业利益关联;若与特定品牌或产品名称有所提及,均为事实描述,不代表任何商业导向。请读者勿将相关信息作为医疗建议或购买依据,任何诊疗或用药请遵从专业医师意见。 ★ 文章导览 ★ 01 产品研发背景 关键词:疾病背景、治疗手段 02 Emicizumab 产品信息 关键词:作用机制、获批适应症、关键质量属性 03 Emicizumab 临床开发路径 关键词:2 项关键 Ⅲ 期、安全性结果 04 非临床与临床试验关联性分析 05 Emicizumab 监管互动 06 结语 产品研发背景 1.1 疾病背景 血友病是一种由于血液中某些凝血因子缺乏而导致患者产生严重凝血障碍的遗传性出血性疾病,包括血友病 A、血友病 B 和血友病 C 三种,以 A 型血友病(hemophilia A,HA)最为常见,约占所有血友病的 80%~85%。 HA 是一种 X 染色体连锁隐性遗传性出血性疾病,以凝血因子 VIII(FVIII)的先天性生成不足或功能障碍为特征。编码 FVIII 的基因位于 X 染色体长臂上,通常为男性患病,含有一条突变基因 X 染色体的女性为携带者。HA 的发病率为每 5000 个新生男孩中出现 1 例 HA 患儿。 出血是血友病最主要的临床表现。HA 患者因为 FVIII 的缺乏导致凝血因子 IX 和凝血因子 X 活化受阻,致使血液不能正常凝固,引起不受控的自发性出血。 图1. 凝血机制示意图[2] 1.2 治疗手段 HA 的治疗原则是综合性的,以往患者需采取 FVIII 的替代治疗,如以重组 FVIII 或血浆源性 FVIII 浓缩物进行的 FVIII 静脉输注(IV)替代疗法,其目的是阻止出血。HA 患者在接受替代治疗的过程中所面临的最大挑战是中和性 FVIII 抗体(抑制物)的产生,重型 HA 患者中抑制物的发生率大约是 20%-30%,通常在治疗开始后的 50 个暴露日内发生。对于伴有高水平抑制物(高滴度或 ≥5 Bethesda 单位 [BU]/mL)的 HA 患者,由于 FVIII 替代治疗无效,疾病状况和生存质量将受到巨大影响。 含有抑制物的患者可接受旁路制剂治疗预防出血,可应用的旁路制剂包括凝血酶原复合物(aPCC/PCC)和重组活化人 FVII。aPCC/PCC 需要 25-60 分钟静脉输注;而重组活化人 FVII 的半衰期仅有 2-3 小时,因此需要频繁的输注。频繁、大体积静脉输注的临床依从性差,大大影响了患者的生活质量。患者迫切需要一种能够提供疗效可靠且长久、低成本及易于使用的治疗方案,以防止出血从而提高生活质量,Emicizumab 由此应运而生。 Emicizumab 产品信息 2.1 作用机制 Emicizumab 是一种抗凝血因子 IXa(FIXa)和抗凝血因子 X(FX)的重组人源化 IgG4 双特异性抗体,可在低至 µM 浓度内与 FIXa 及 FX 结合,形成模拟 FVIIIa 的分子桥,模拟 FVIIIa 的活性促进 FIXa 对 FX 的活化,显著增加凝血酶的生成,使 FVIII 功能障碍或完全缺乏 FVIII 的 HA 患者的出血部位止血。此外,Emicizumab 与 FVIII 之间没有结构关系,不会诱导或增加 FVIII 或其他凝血因子的抑制物的出现,其止血作用也不因存在 FVIII 抑制物而改变。 图2. Emicizumab 作用机制示意图[3] 2.2 获批适应症 Emicizumab 获批适应症为预防或降低存在 FVIII 抑制剂的成人和儿童 HA(先天性凝血因子 VIII 缺乏症)患者的出血发作频率。推荐剂量为 3 mg/kg,前 4 周每周一次,随后为 1.5 mg/kg,每周一次,皮下注射。 图3. Emicizumab 产品信息图 相较于传统的 FVIII 的替代治疗和旁路制剂治疗,Emicizumab 治疗的特点见下表: 表 1. HA 不同治疗方案比较 2.3 关键质量属性(CQAs) Emicizumab 的关键质量属性包含活性药物成分、药物原料和源自药物生产过程及药物的通用属性(详见相关 FDA 审评报告)。 (1)活性药物成分 Emicizumab 通过人源化和氨基酸替换来优化模拟 FVIII 的功能特性和其他特性(包括等电点、稳定性、溶解度、免疫原性)。其包含两条不同的重链和两条相同的轻链,其中 anti-FIXa 重链(Q 链)、anti-FX 重链(J 链)和轻链的 CDRs 分别来自人 FIXa 免疫大鼠、人 FX 免疫小鼠和两者(图4)。通过静电转向突变,重链的 Fc 区被设计为优先异源二聚化。 图4. 分子结构示意图[4] 活性药物成分的 CQAs 包括效力、分子量变体、电荷变体、糖型、结构变体等,相关 CQAs 的改变会影响 Emicizumab 的生物学活性、安全性、PK、免疫原性等特征。 (2)药物原料相关 Emicizumab 是在基因工程 CHO 细胞中生产的,其药物产品是一种无菌、不含防腐剂、无色至淡黄色的皮下注射溶液,包含 30 mg/1.0 mL、60 mg/0.4 mL、105 mg/0.7 mL 或 150 mg/1.0 mL 4 种规格,每种规格的组成成分见下表: 表 2. Emicizumab 药物产品规格[7] 原料药(DS)的 CQAs 包括与工艺相关的杂质(宿主细胞 DNA、宿主细胞蛋白、纯化用 protein A 等)、外源微生物(病毒、钩端螺旋体、支原体)、细菌内毒素、Bioburden、成分和理化性质(蛋白质含量、渗透压、pH、外观、氨基酸含量等),相关 CQAs 的改变主要影响 Emicizumab 的安全性、生物活性、免疫原性、纯度等。 (3)源自药物生产过程及药物的通用属性 Emicizumab 的主要容器封闭系统由 3 mL I 型玻璃小瓶,14 mm 的橡胶塞和 15 mm 铝盖与塑料翻转盘组成,瓶和瓶塞符合 USP /欧药典/日本药局标准。源自药物生产过程及药物的通用属性的 CQAs 包含可见颗粒物、瓶内容物、污染物(无菌程度、内毒素)、容器密封完整性、成分和理化性质(蛋白质含量、物理状态、颜色、透明度等),相关 CQAs 的改变主要影响 Emicizumab 的安全性、生物活性、免疫原性特征等。 CQAs 决定了候选药物的生物学活性、安全性、免疫原性等特征,是一切研究的基础。 关联解读: 对于生物类似药来说,通过全面的质量比对研究来确立候选药物与参照药的质量一致性同样是后续研究的基础。FDA 的完全回复函(CRL)显示,部分生物类似药由于关键质量属性无法建立相似性而未被批准。因此,Emicizumab 的生物类似药研发应当首先关注其 CQAs 。 Emicizumab 临床开发路径 支持 Emicizumab 首次 BLA 批准的主要临床试验包含 1 项 Ⅰ 期试验,1 项 Ⅰ/Ⅱ 期试验和 2 项关键 Ⅲ 期临床试验。 (1)Ⅰ期临床(ACE001JP/ ACE002JP) 表 3. Emicizumab Ⅰ 期临床试验设计[7] ■ 试验设计 ACE001JP 临床试验分为 Part A+B 单次给药和 Part C 重复给药两部分研究,给药方式均为皮下注射给药,其中 Part A+B 是在日本和高加索健康志愿者中开展的随机、双盲、单次剂量递增试验,主要目的是为了评估 Emicizumab 单次给药的 PK 特征,给药剂量为 0.001-1mg/kg,包含安慰剂对照组。 ACE001JP 临床试验 Part C 部分和 ACE002JP 是 Emicizumab 进一步的剂量探索和拓展研究,分为 3 个给药队列(详见表 3),对象为日本成人和年龄大于 12 岁的青少年血友病患者(伴或不伴FⅧ 抑制物),用以评价 Emicizumab 在 HA 患者长期治疗期间的安全性、耐受性、PK、免疫原性和对出血的抑制作用。 ■ 起始剂量 Ⅰ 期临床显示,Emicizumab 的 FIH 起始剂量为 0.001 mg/kg。在 FDA 审评报告中并未明确计算过程。通过查阅资料及结合现有的材料,推测其 FIH 起始剂量设计可能有以下几方面的考虑: 考虑到 Emicizumab 的作用机制为模拟 FVⅢa 的功能,强效促进凝血,可能引起过度凝血,形成血栓,因此采用更保守的 MABEL 原则计算 FIH 起始剂量可能更加合适; 体外凝血试验结果显示,体外最小生物效应水平约为 0.1 μg/mL,结合非临床药代动力学数据,通过异速缩放模型,预测 Emicizumab 在人体内的 PK 参数,显示皮下注射 0.001 mg/kg 后,人体内 Cmax 约为 0.1 μg/mL; 基于传统的 NOAEL 方法进行界定。食蟹猴作为非临床研究相关种属,其 SC 重复给药 QW*4(共给药 5 次)的研究结果显示,NOAEL 为 30 mg/kg,基于 BW 进行推算,安全系数取 10,HED 为 0.9 mg/kg,提示 0.001 mg/kg 剂量具有较高的安全窗口。 ■ 研究结果 Ⅰ 期临床结果显示,在所有给药组中,Emicizumab 血浆浓度在 C-1 和 C-2 组中随时间增加,达到稳态的时间约 12 周;0.3、1 和 3 mg/kg/周剂量组的稳态谷血浆浓度(Css,trough)分别为 10.3 ± 4.5 μg/mL、29.9 ± 6.9 μg/mL 和 120 ± 26.8 μg/mL,以剂量比例方式增加。该试验组合支持了 Emicizumab 每周 3 mg/kg 的剂量选择,同时还显示出一定的疗效-反应关系(ER),即在 Emicizumab 稳态谷血浆浓度下(Css,trough≥ 45 μg/mL),中位年出血率(ABR)为 0。 图5. HA 患者每周皮下注射 Emicizumab 后血浆中 Emicizumab 的平均变化曲线[7] (2)Ⅲ 期临床 Emicizumab 在拟定患者人群中的疗效和安全性得到了两项 Ⅲ 期临床试验的支持:HAVEN 1(BH 29884)和 HAVEN 2(BH 29992)。 表4. Emicizumab Ⅲ 期临床试验设计[7] 1 BH 29884 ■ 试验设计 BH 29884 是 1 项随机、开放标签、多中心的 Ⅲ 期临床研究,包含随机与非随机队列(入组前 24 周内的出血次数,<9次 vs. ≥ 9次);入组患者为≥12 岁伴 FVIII 抑制物的 HA 患者(N=109),目的是为了在携带抑制物的 HA 患者中评估预防性应用 Emicizumab 与非预防性应用 Emicizumab 的疗效、安全性和药代动力学。 给药方案为在前 4 周按 3 mg/kg/周的负荷剂量给药,之后按 1.5 mg/kg/周的维持剂量给药。所有入组患者分组详见表 4,主要设计参见图 6:共有 53 名在研究入组前接受旁路药物间歇性治疗的抑制物患者按 2:1 的随机化比例入组,接受预防性 Emicizumab 治疗(A组)或不接受预防性治疗(B组)。为了获得额外的安全性和有效性数据,随机分配至未接受 Emicizumab 治疗的患者(对照组,B组)将在完成 24 周研究后接受相同剂量和方案的 Emicizumab 预防性治疗。 在预防性 Emicizumab 治疗 24 周后,所有患者都能够继续维持 1.5 mg/kg/周的剂量,或者如果他们达到方案规定的次要终点并获得医学监查员的批准,则可以选择将其剂量增加至 3 mg/kg/周。入组前接受旁路药物预防性治疗的 HA 抑制物患者入组 C 组,以与 A 组相同的剂量和方案接受预防性 Emicizumab 治疗。接受间歇性旁路药物治疗并参加研究 BH 29768(一项非干预性研究)但无法入组 A 组或 B 组的患者入组 D 组,接受预防性旁路药物治疗但无法入组 C 组的患者也入组 D 组。 BH 29884 的主要疗效终点为评估期内治疗的出血次数(出血率),次要疗效终点包括所有出血,经治疗的关节出血,经治疗的自发性出血等。 图6. BH 29884 临床试验设计[7] ■ 研究结果 该研究达到了 A 组与 B 组相比治疗出血的主要终点,治疗出血减少了 87%;中位年出血率(ABR)为 0,表明与使用 FVIII 抑制剂的 HA 患者的现有治疗相比有所改善。 表 5. BH 29884 临床试验结果(主要终点,治疗出血,A组vs.B组)[7] 疗效结果-次要疗效终点结果显示,包括:所有出血;治疗的关节出血;治疗的自发性出血;治疗的靶关节出血在内,Emicizumab 预防组(A组)患者的出血数量显著少于未预防组(B组)患者的出血数量。 表 6. BH 29884 临床试验结果(次要出血相关终点,A组vs.B组)[7] 2 BH 29992 ■ 试验设计 BH 29992 是 1 项非随机、单组、多中心、开放标签的 Ⅲ 期临床研究,该临床研究招募了年龄小于 12 岁的 HA 的患者(招募的患者需 <40 kg,因为 ≥40 kg 患者入组 HAVEN 1),这些患者具有 FVIII 抑制剂,患者在研究前可能已接受旁路药物预防性或间歇性治疗。该研究目的是为了评价 Emicizumab 每周一次皮下给药的疗效、安全性和药代动力学,给药方案为前 4 周接受 3 mg/kg 每周一次的负荷剂量,然后接受 1.5 mg/kg 每周一次的维持剂量,主要设计参见图 7。BH 29992 的主要疗效终点为年出血率(ABR)和健康相关生活质量结果(Health-Related Quality of Life Results,HRQoL)评分。 图7. BH 29992 临床试验设计[7] ■ 研究结果 在 90 天安全性更新的中期分析时,研究 BH 29992 共入组了 60 例受试者,其中 23 例年龄小于 12 岁的受试者已接受 Emicizumab 预防治疗至少 12 周(疗效人群)。结果显示,观察期内,治疗性出血、治疗性自发性出血和治疗性关节出血的 ABR 小于 1,所有出血的 ABR 小于 2.9,所有类型出血的中位 ABR 均为 0(所有出血除外,为1.5);大多数患者的治疗出血、治疗自发性出血、治疗关节出血和靶关节出血均为零出血事件,23 例患者中有 8 例(34.8%)发生所有出血。结果与 BH 29884 类似,有效性数据支持使用 FVIII 抑制剂的 HA 儿童患者的适应症。 表 7. BH 29992 临床试验结果(出血事件,疗效人群)[7] 关联解读: Emicizumab 的临床试验数据充分表征了其 PK/PD 特征,同时提供了充足的安全性和有效性数据,在开发其生物类似药时有可借鉴参考之处: 1)可根据候选药物的 PK 特征,评估相似性,建立可能的跨地区参照药的桥接证据;评估疗效-反应(ER)关系以证实候选药物的药理作用;基于已建立的 PK 相似性,确定是否开展 Ⅲ 期临床以比较安全性和有效性。 2)患者接受多剂量 aPCC 作为疑似出血的旁路药物后,可能发生血栓性微血管病(Thrombotic microangiopathy,TMA)和/或血栓栓塞(Thromboembolism,TE)的严重不良事件(Serious Adverse Event,SAE),提示应尽可能避免候选药物与 aPCC 一起作为用于出血的旁路药物,并在需要时使用尽可能低剂量的 aPCC,建议将该 SAE 传达给医生、患者和护理人员。 3)Emicizumab 临床试验中存在免疫原性,但免疫原性方法对 Emicizumab 并不敏感。因此,监管要求申请人发布上市后承诺(PMC),要求在完成经充分验证的免疫原性方法后(包含结合抗体与中和抗体),描述抗 Emicizumab 抗体的发生率及其对安全性、疗效和 PK 的影响。 4)申请人考虑到 Emicizumab 为分解代谢,而非肝、肾代谢,预计不会产生影响,因而临床试验中未对肝、肾功能障碍的患者进行评估。 Emicizumab 非临床研究 及临床研究关联性分析 非临床研究与临床研究有着十分密切的关系。一方面,非临床研究方案的设计依赖于拟定的临床研究方案中的基本信息,包括 PK、PD 和安全性监测相关指标的确立;另一方面,非临床研究结果对临床给药方案的制定、安全性和有效性的评估等有重要参考意义。 ■ 药效学研究 Emicizumab 的 PD 核心研究内容包括体外机制验证、体外药效学验证和体内药效学模型评估。如通过表面等离子共振(SPR)技术证实 Emicizumab 的靶点结合能力;通过体外全血/血浆验证 Emicizumab 模拟FⅧ辅因子功能、促进凝血酶生成以及缩短凝血时间的能力;通过 HA 动物模型监测凝血功能恢复能力等。PD 研究结果证实了 Emicizumab 的作用机制,尤其可绕过 FVIII 直接激活凝血共同通路,同时预测了药物在含有 FVIII 抑制物患者体内的止血效果,为临床试验打下了基础。 ■ 药代动力学研究 Emicizumab 的 PK 研究主要结果显示,Emicizumab 皮下注射给药的生物利用度 >85%,药物达峰时间在 24~48 h,消除半衰期 28~35 天,且 AUC 与剂量呈线性关系,支持临床灵活的剂量调整。此外,Emicizumab 主要分布于血浆,无特定器官蓄积,包括在重复给药试验中也是如此,说明长期用药安全;其不被 CYP450 代谢,提示药物相互作用风险低。开发了电化学发光法(ECL)检测血浆中的 ADA,ADA 阳性动物表现出 Emicizumab 的更快消除。 关联解读: 由于 CQAs 比对并不能涵盖微小的、无法检测到的结构差异(如三维构象、翻译后修饰的微小异质性),这些差异可能在复杂的生物体内环境被放大,导致功能或药代行为的差异。因此在生物类似药的开发中,非临床 PD 和 PK 研究发挥着不可替代的桥梁作用,两者是将质量相似性与临床相似性连接起来的关键证据链。如果在非临床的 PD/PK 研究中就发现了显著差异,那么候选药物在人体中表现相似的可能性将大大降低,这可以在早期帮助淘汰不合格的候选药物,降低临床开发风险和成本。 图8. Emicizumab 非临床 PK 研究结果[7] ■ 安全性评价 Emicizumab 非临床安全性评价提示了临床试验中可能出现的不良反应,主要为注射部位的改变和血液学变化。其中注射部位主要可见皮下组织红斑和出血,含铁血黄素沉积伴炎性细胞浸润以及个别皮下组织变性/坏死等。临床试验中出现了注射部位 SAE 的青少年患者,且注射部位反应为主要的 AE,患者发生率约为 18%。 在食蟹猴 QW*26 周的毒理学研究中,于 D141 和 D183 观察到了血液学变化(D-二聚体和纤维蛋白降解产物(FDP)增加),但在检查的器官和组织中未见血栓;短周期的毒理试验中未见 D-二聚体和纤维蛋白降解产物(FDP)增加,因此认为这些变化不具有毒理意义。临床试验中发生了 TMA 和 TE,经调查怀疑是使用过量的 aPCC 导致。在食蟹猴中检测出抗药抗体(ADA)和中和抗体(NAb),实际临床试验中 ADA 风险很小。 此外,3 mg/kg QW 给药方案是预期在患者中产生最高暴露量的方案,而在食蟹猴QW*26 周的研究(1060134)中,NOAEL 剂量为 30 mg/kg,稳态 AUC0-168h(AUC0-168h ss)的暴露量为 8680 µg.d/mL,约为 3 mg/kg QW 临床给药方案下暴露量的 11 倍,表明非临床试验已充分暴露 Emicizumab,满足临床试验的评估需求。 图 9. Emicizumab 非临床研究内容[7] 由于缺乏相关的啮齿类动物种属用于评估致癌性风险,且 IgG 抗体预期不会直接与 DNA 或其他染色体物质直接发生相互作用,因此未进行致癌性和遗传毒性研究,这也符合 ICH S6(R1)指导原则要求。 此外,因为 HA 以 X 连锁隐性方式遗传,约 99% 的 HA 患者为男性,女性服用这种药物的情况非常罕见;同时,在食蟹猴中进行的一般毒理学研究中,Emicizumab 在 SC 剂量高达 30 mg/kg/周持续 26 周或 IV 剂量高达 100 mg/kg/周持续 4 周时,未引起雄性或雌性生殖器官产生任何毒理学显著变化,因此未对 Emicizumab 进行专门的动物生殖和发育毒理学研究。目前,尚不清楚孕妇服用该药物是否会对胎儿造成伤害或影响生殖能力,也没有关于动物或人乳中存在 Emicizumab 的信息。 图 10. Emicizumab 非临床研究内容[7] 关联解读: 目前,EMA 和 FDA 已认可当药学与体外功能数据足够充分时,可豁免生物类似药的重复毒理试验,尽管中国 NMPA 等部分监管机构对某些生物类似药仍保留重复剂量毒性试验要求(尤其首仿品种)。在评价生物类似药与参照药的可比性时,比对研究主要包括 CMC 和 PK/PD,其中 CMC 比对是基础,PK/PD 比对有助于进一步评估相似性,前文已对此进行关联解读。若已建立充分的 CMC 和 PK/PD 相似性证据,其它试验则根据申报的监管要求及药物特点展开,如开展重复给药毒性试验(头对头设计,含 TK)来评估安全性。重复给药毒性试验中亦可加入免疫原性风险评估,如果候选药在参照药未引发 ADA 的相同动物模型中引发了更强的 ADA 反应,提示其质量上的某些差异(如聚体水平、宿主细胞蛋白残留)可能增加了免疫原性风险。当然,需要合理解读非临床研究中出现的 ADA 差异。 Emicizumab 监管互动 Emicizumab 的成功上市,与合理的临床试验设计息息相关,当然也离不开与监管的高效互动。在 Emicizumab 的上市历程中,就临床试验设计、BLA 申报等问题,多次与监管紧密互动,如 pre-IND 会议、pre-phase III 期会议、Pre-BLA 会议等。 图 11. Emicizumab 上市历程[7] 关联解读: 对于生物类似药来说,与监管的互动也至关重要,互动结果可能会极大地影响非临床乃至临床试验的设计。本年度博安生物 BA1104(纳武利尤单抗注射液生物类似药)和百奥泰 BAT3306(帕博利珠单抗)的临床开发计划调整就是最好的案例。 随着经验的积累,中外监管机构对于生物类似药的监管理念也在不断演化和完善,当然也存在差异。EMA 和 FDA 主张简化审批流程,强调生物类似药应在质量、安全性、有效性方面与参照药一致,同时通过桥接试验证明参照药具有可比性,总体较为灵活;NMPA 对于生物类似药的审批、评价原则以及参照药选择相对保守。与之相对应的是国内外监管机构对于生物类似药出台的一系列的指导原则/草案: NMPA 于 2021 年 2 月发布了《生物类似药相似性评价和适应症外推技术指导原则》,对生物类似药相似性保持相对全面的证据要求,应对药学、非临床、临床比对研究设计和结果进行综合评价,以确定候选药与参照药的整体相似性。强调生物类似药逐步递进研究的不同阶段均应开展相似性评价,非临床和临床研究应基于前期药学比对结果进行针对性设计以解决候选药和参照药间的不确定性,进而支持整体相似性评价。 EMA 于 2025 年 4 月发布了的《Reflection paper on a tailored clinical approach in biosimilar development》 草案,该草案指出在生物类似药结构高度相似且质量分析充分的情况下,仅通过全面的质量比对+ PK 比对研究即可证明相似性,无需临床疗效比对试验(Comparative Efficacy Studies,CES)试验,但需确保生产一致性和免疫原性风险可控。 FDA 于 2025 年 10 月 29 日更新了简化生物类似药开发的科学考量指南草案,认为: 1)CES 在检测产品差异方面不如现代分析技术灵敏; 2)CAA(comparative analytical assessment)足以支持证明拟开发的生物类似药与其参照药高度相似,即使在临床非活性成分方面存在细微差异; 3)一项设计合理的人体药代动力学相似性研究和免疫原性评估可能足以评估拟开发的生物类似药与参照药在安全性、纯度和效力方面是否存在具有临床意义的差异。 结语 截至目前,Emicizumab 是国内唯一已获批用于 HA 预防治疗的抗体类药物。其应用为 HA 的长期预防管理提供了更为便捷、依从性更高且安全性良好的治疗选择,助力患者生活质量的改善。当然,Emicizumab 的成功上市,离不开合理的非临床设计、科学的临床转化和高效的监管互动。 本文对艾美赛珠单抗的上市历程进行复盘,结合生物类似药研发路径,即重视关键质量属性的比对,深入理解产品特性和监管要求的基础上精简非临床试验设计,同时灵活地进行临床试验比对,期望为后续同类产品的研发提供经验和启示。