
2021-07-09 09:52:26来源:药智网浏览量:716
导读:敢问,路在何方?
7月2日,国家药品监督管理局药品审评中心发布公开征求《以临床价值为导向的抗肿瘤药物临床研发指导原则》(下称《指导原则》)意见的通知,涉及到临床对照药物的部分两项要求直接加大了创新药物通过临床试验的难度。
一石激起千层浪,医药股连日迎来剧烈调整,跌幅霸屏。
《指导原则》征求意见稿所阐明的精神确实击中了中国创新药行业发展的痛点,市场对行业分化作出了解读,“伪创新”被解读为严打的对象。
我们尝试探讨“伪创新”兴起的缘由。
费用居高:最烧钱TOP10新药项目
据PhRMA成员公司数据显示,1970年成功研发一个新药的平均成本(含平摊失败项目成本,下同)只需1.79亿美元;
到1990年,成功研发一个新药的平均成本已达10亿美元;
到了2010年,成功上市一个创新药的成本已经高达惊人的26亿美元。
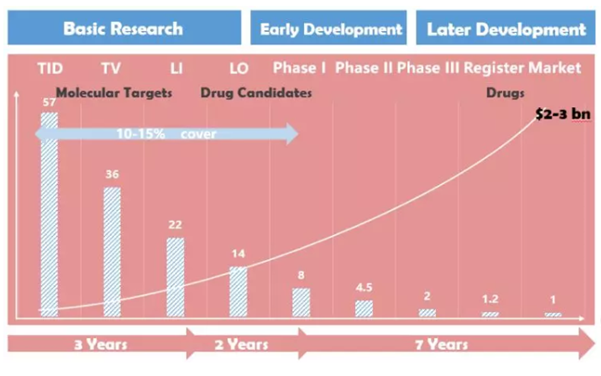
图1新药研发历程、进入各个阶段小分子化合物数量占比及研发投入。
数据来源:Roche,清华大学医学院,华夏幸福产业研究院
另外一个维度,从新药研发的临床投入对整体新药研发投入也可见一斑。
全球知名生命科学行业市场咨询公司Evaluate旗下EPVantage发布报告预测了生物制药领域最烧钱的Top10新药研发项目。
Top10新药研发项目预测在2020年临床费用总计40.17亿美元,排首位的载脂蛋白(Apo)A-I输注疗法(名称:CSL112)预计一年的临床投入就高达6.21亿美元。
Top10新药研发项目预测在整个临床研发投入高达177.90亿美元,吉利德和Galapagos公司联合研发的口服JAK1抑制剂(名称:filgotinib)预计临床投入35.8亿美元(约合232亿人民币),震撼人心。
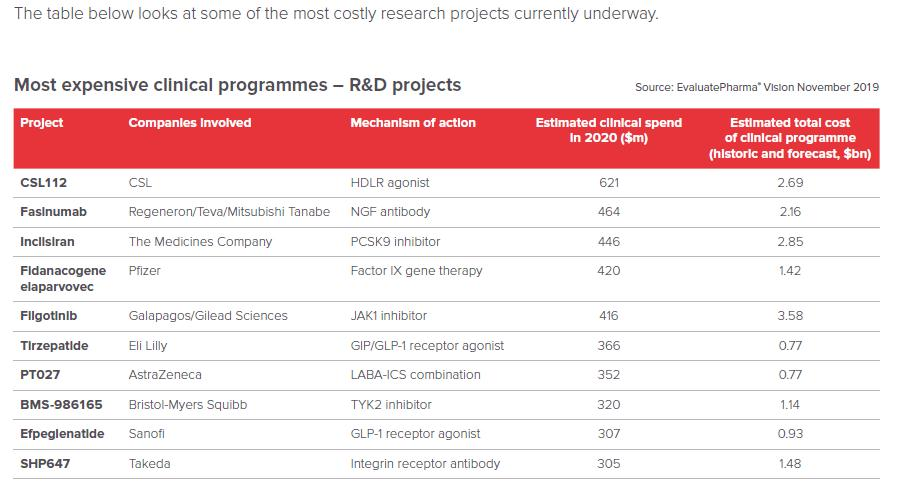
图22020年生物制药领域最烧钱的TOP10新药研发项目预测
资料来源:EPVantage
一方面,巨额的研发投入让大部分企业望而却步,另外一方面,即使公司愿意投入巨大的资金用于技术更新,但是其销售额仍远远跟不上新药研究和开发所需费用的迅速增长。
伴随着上述问题的出现以及全球医药价格上的竞争,Me-too策略在新药研究开发中应运而生。
H2受体拮抗剂、血管紧张素转化酶抑制剂、质子泵抑制剂、二氢吡啶类钙拮抗剂、羟甲戊二酰辅酶A还原酶抑制剂等的Me-too研究,创造了一个又一个的营销神话,也激励着各大企业蜂拥而至。
据EvaluatePharma和Deloitte统计,国内创新药到NDA(上市申请)或者获批上市的研发费用中值仅在1亿元左右。
在新药研发资金投入相对不足、研究水平相对落后的现实情况下,采用Me-too策略发现新药,相对于新药创新来说,降低了技术难度、风险和研发成本,似乎是一个不错的选择。
成功率低:新药上市率仅为1.2%
一款成功创新药从研发到上市需要经历以下10个步骤:
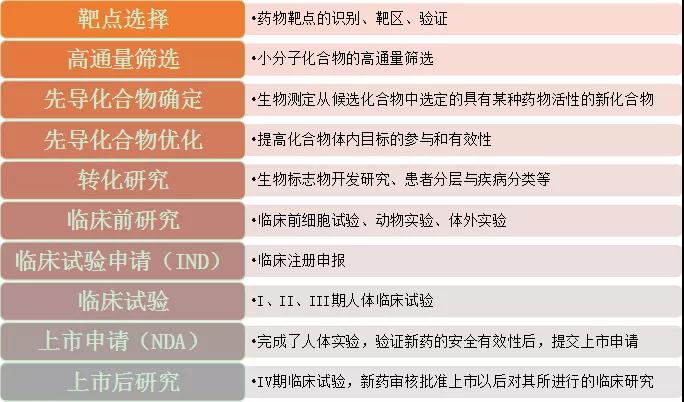
图3新药研发流程
数据显示,新药研发从药物靶点发现到靶点确认的阶段比例为36%,进入先导化合物筛选阶段的比例为22%,进入到先导化合物优化筛选阶段的概率为14%;
进入临床I期的比例为8%,进入II期临床的概率为4.5%,进入III期临床的概率为2%;
进入到上市注册环节的概率为1.2%。
完全创新意义的新药研发(指原创性的Firstinclass,从靶点发现开始),最终成功概率仅为1.2%。
有人对如此低的成功概率望而却步,有人却在概率分析中找到了突破口。
通过创新技术来提高开发新药的成功率和速率的过程已变得日趋艰难,而提高成功率最快捷的一个办法,就是减少新药研发的步骤。
例如,已有靶点确证,那就从高通量筛选开始,甚至更高超的Metoo,直接从先导化合物优化开始,自然而然整体成功率就提高了,研发时间也缩短了。
投资回报率低:仅1.8%
据Deloitte统计的数据显示,全球TOP12大型药企(Amgen,AstraZeneca,Bristol-MyersSquibb,EliLilly,GlaxoSmithKline,Johnson&Johnson,Merck&Co.,Novartis,Pfizer,Roche,Sanofi,Takeda)2010年一款新药平均投资回报率可达到10.1%。
但2019年该数字已降低至1.8%,创下历史新低。
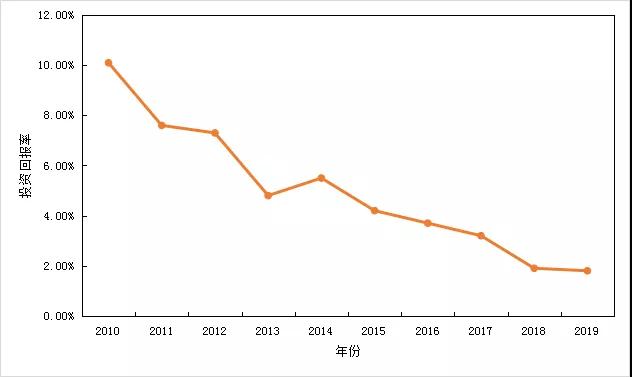
图3新药研发投资回报率
资料来源:Deloitte官网
创新研发已经如此高难度,药企们的头上还悬着一个达摩克斯之剑——专利悬崖。
以美国新药研发的“双十定律”简单来测算,即10年投资10亿美金研发一款新药。
一般来说,一款新药的专利保护期20年,而这个专利保护期是从新药专利申请开始的,即一款新药上市后大概只有不到10年让原研企业独家卖,要收回研发成本,一款新药至少在专利保护期的10年内每年的利润至少要有1个亿美金。
如果一款新药研发投入达到26亿美金,则相应需要每年2.6亿美金利润空间。
根据艾美仕(IMSHealth)预测,过去十年,每年品牌药品因专利到期导致的销售收入损失将超过1000亿美元。
现状:创新药井喷时代
新药研发的原研企业面临着上述三重难题。
与此相对应的是,中国已经进入了创新药井喷的时代,从过去的一年批一两个新药,到现在一年批四五十个新药,甚至很多新的药物都在争夺同一个靶点。
在这样的情况下,从研发到销售,药企都面临着新的价值重塑,原有的格局与商业模式被彻底打破。
如何降低营销费用和提高研发效率,让产品尽快进入应用场景并广泛覆盖,成了药企生存和发展的必答题。
从国内医药创新趋势来看,未来3到5年将进入临床后期开发和落地兑现阶段,这意味着药企从立项起就要提前考虑商业化回报问题。
Metoo则是企业为了实现业务稳定的发展,逐步向创新驱动的不二选择。
当大部分企业转型期间均瞄准这种方式,热度的高涨自然就带来行业整体“伪创新”的景象。
四大破局之道
过去十多年来,我国医改政策的重点是提高药品可及性和控制成本,如今则转向提高药品审批速度、扩大医保准入、鼓励创新和提升质量。
加速驱动整个医药产业的创新发展,创新医药企业的进阶之路便由此展开。
面对新药研发挑战,笔者建议四大破局之道:
1、挖掘细分领域价值,制定清晰的准入策略
中国目前尚未建立系统的评估体系,预期挑战较大的产品,应主动在适应症人群中挖掘优势亚组,在制定好清晰的准入策略后,用它来指导价值数据的产生与价值材料的组织,统一给各类利益相关方传递信息,最终实现研发目标。
2、大数据助力价值挖掘
价值证据在新药审评审批、甚至医保准入中至关重要,而随着新药上市到准入周期缩短,准备充实的价值证据将成为新药研发的重大挑战。企业可以借助大数据加快真实世界数据收集、挖掘支撑疾病负担研究和支撑成本效益分析。
3、创新和高效的专家沟通
新药研发“唯快不破”,企业可以考虑建立跨部门合作项目管理办公室(PMO),明确分配职责,设置KPI和时间表,并紧密追踪进度,敏捷反应。
4、积极参与政策倡导和探索
我国新药技术评估的体系尚处于起步阶段,技术评估结果转化为行业政策的机制还在探索阶段。有关部门正在编制相关的技术评估的指导意见,而体系的形成尚需不断的探索尝试和数据积累。制药企业可积极参与到政策探索中。
在市场环境和政策环境的驱动下,药企唯有苦练内功、扎实推进产品创新升级,才能在这强者恒强的环境下长足发展。
声明:本文系药方舟转载内容,版权归原作者所有,转载目的在于传递更多信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除内容!