
2026-05-07 10:38:35来源:鼎泰集团TriApex浏览量:6
随着寡核苷酸药物(ONTs)在心血管代谢疾病等慢性疾病治疗领域的研发逐步推进至关键性临床试验阶段,大量候选药物需要根据 ICH S1 评估致癌性试验的必要性。对于需要进行致癌性试验的 ONTs,其致癌性试验面临特有的科学与监管挑战:
试验时机:应在临床开发的哪个阶段提前规划,以匹配 NDA 申报计划?
沟通交流:如何准备一套有效的致癌性试验 SPA 沟通交流?
替代分子:对于在啮齿类动物中没有药理学活性的,是否需要开展替代分子的致癌性试验?
剂量设计:仅参考暴露量的“25 倍”确定高剂量足够吗?
统计分析:基于 ONTs 的独特作用机制,统计分析方法是否需进行调整或补充?
提交时限:致癌性试验报告是否必须在 NDA 申请前完成并提交?
全文共:12466 字 17 图
预计阅读时长:30 分钟
近年来,ONTs 成为继小分子化学药和抗体等生物药之后现代制药的第三次浪潮。随着研发管线的快速推进及长期用药需求的增加,ONTs 的安全性,尤其是致癌性风险,已成为行业与监管机构共同关注的核心科学问题。
相较于传统小分子药物,ONTs 的分子特性、作用机制及体内作用路径具有显著特殊性,使其致癌性风险评估面临独特挑战。当前,全球范围内尚无专门针对 ONTs 致癌性试验的指导原则,业界在试验策略、相关种属确定、免疫原性潜在干扰及非传统毒性机制(如免疫调节、脱靶效应、组织蓄积与慢性炎症)的致癌潜能评估等方面,尚缺乏统一共识与成熟经验,亟需通过更多案例积累与系统研究加以明确。
围绕前文所述的困扰众多 ONTs 药物研发企业的核心问题与挑战,本文将结合国内外监管指南、已上市代表性产品的致癌性评价路径及审评考量、基于致癌性试验和 ONTs 药物的评价逻辑,系统梳理当前的科学认知与监管要求,旨在为 ONTs 非临床致癌性试验的设计,以及开展策略的制定提供务实参考。
声明
本文仅为行业科普及学术研究用途,不构成对任何药品、医疗器械或相关产品的推广、推荐或商业宣传。文中提及内容均基于公开资料,不涉及具体产品功效暗示或商业利益关联;若与特定品牌或产品名称有所提及,均为事实描述,不代表任何商业导向。请读者勿将相关信息作为医疗建议或购买依据,任何诊疗或用药请遵从专业医师意见。本文内所引用的第三方图表、数据及产品信息,其知识产权归属于相关权利人,本文引用仅为学术研究及说明之目的,特此说明并致谢。
★ 文章导览 ★
01 | 致癌性试验的监管要求 —— 理解 ONTs 致癌性试验的必要性和一般要求 1.致癌性试验概述及相关指导原则 2.ONTs 开展致癌性试验的必要性和一般要求 |
02 | 已上市 ONTs 致癌性评价概况 —— 学习上市药物的致癌性试验实施经验 1.致癌性试验开展情况 2.致癌性试验的开展时机 |
03 | 从 Fitusiran 致癌性试验了解试验设计细节 —— 剂量选择逻辑和关键数据 1.SD 大鼠 2 年致癌性试验 2.CB6F1-TgN (RasH2) 转基因小鼠致癌试验 3.Fitusiran 致癌性试验给予的启示 |
04 | 从 Avacincaptad pegol 经验看如何运用 WoE 证据进行致癌性评估 —— 基于 WoE 的豁免案例 |
05 | 未来方向 —— 从“常规范式”到“科学化、个体化的整合性评估” |
06 | 结语 |

致癌性试验的监管要求
理解 ONTs 致癌性试验的必要性和一般要求
致癌性试验概述及相关指导原则
致癌性试验的目的在于系统评估化学物质、生物制剂或物理因素长期或终生暴露下,诱发实验动物肿瘤发生的能力与潜在风险,进而评估其对人体的相关风险。
主要检测指标包括实验动物在受试物长期作用下,良性和恶性肿瘤的发生率、类型、发生部位、发生时间(潜伏期)以及肿瘤的多发性;检测范围通常涵盖药物对整体生存率、体重变化、摄食饮水消耗、血液学与血清生化指标、器官重量以及各组织器官病理学改变(尤其是肿瘤性病变)的综合性影响。
在开展致癌试验时,可参照下表中致癌性相关指导原则进行。
表 1. 致癌性试验相关指导原则
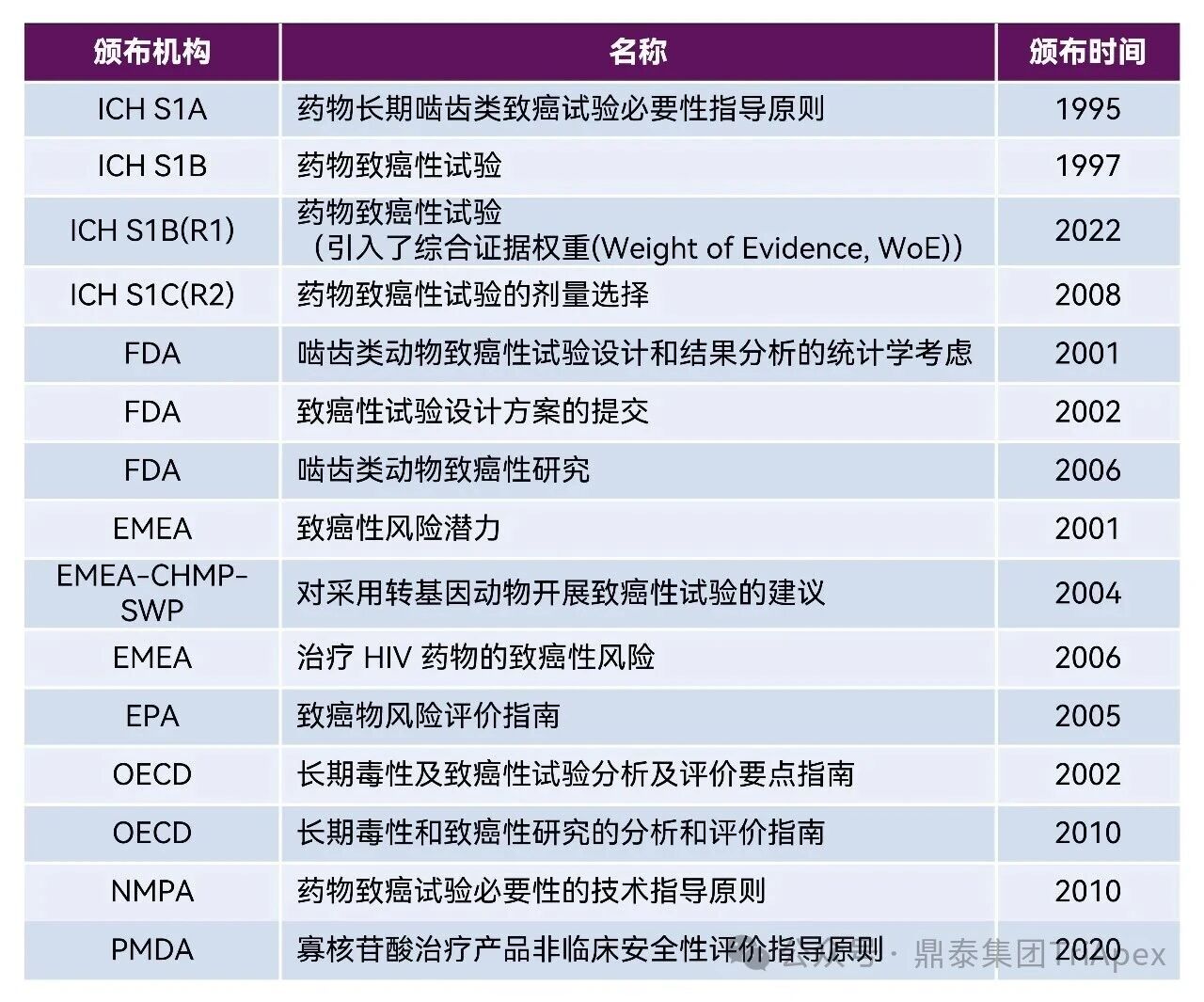
在遵循表 1 所列指导原则的基础上,还需同步参考 ICH M3(关于体内致癌性研究的提交时机)与 ICH S6 等指南中针对致癌性试验的相关建议。
2. ONTs 开展致癌性试验的必要性和一般要求
ONTs 兼具生物制品与化学药物的双重属性,其非临床研究内涵与传统化学药有所不同。这类药物常通过化学修饰提高稳定性与疗效,但同时也可能引发独特的脱靶毒性及潜在的致癌风险。鉴于多数 ONTs 需长期甚至终身给药(例如用于治疗遗传性疾病或慢性疾病),现有长期安全性数据尚不充分,因此除非用于晚期肿瘤等预期寿命较短的适应症,致癌性试验通常具有开展的必要性[1]-[3]。
表 2. 监管机构对于 ONTs 开展致癌性试验的要求

ONTs 具有高特异性和低系统暴露的特点[4]-[6],虽然其直接的遗传毒性风险较低,但其独特的药代动力学特征(组织蓄积、长期滞留)和机制相关的间接风险(免疫刺激、脱靶效应),使得通过标准化致癌性研究评估其致癌风险成为必要,以保障长期用药安全并满足监管要求。
评估 ONTs 致癌风险时,应考虑其药理学效应,如在 2 个种属中开展致癌试验,应在至少 1 个种属中考察药理学效应相关的致癌风险。当临床分子在啮齿类动物中无药理活性时,可以使用在某种属中具有药理活性的替代分子来评估致癌风险[7]。
当存在以下的几种情况时,采用替代分子评估药理学相关致癌风险不是必须的:
◆ 作用机理明确且有致癌风险;
◆ 替代分子在野生型大鼠中的作用不能反映人体中预期的药理学作用;
◆ 啮齿类动物中不存在对应的靶点。此时,在啮齿类中需要开展 1 项两年致癌试验评估临床分子非杂交依赖的脱靶效应[7]。
基于以下考虑,选择替代分子时仍需慎重:
1)寡核苷酸微小的序列和模式差异可能导致毒性的巨大改变;
2)啮齿类动物具有种属特异性毒性,与人体相关性有限;
3)可能需要额外的 CMC 研究[2]。
总体而言,当前行业内逐渐形成共识,通常应结合 ONTs 独特的分子特征,评估其开展致癌性试验的必要性,如需开展,相应的致癌性试验策略需建立在科学性原则基础上。
已上市 ONTs 致癌性评价概况
学习上市药物的致癌性试验实施经验
1. 致癌性试验开展情况
截至 2025 年 12 月底,已有 21 种 ONTs(不含撤市药物)在全球范围内上市[4][8][9]。表 3 对已上市 ONTs 致癌性试验的开展情况,包括动物种属、是否使用替代分子、是否在 NDA 之前完成等进行了汇总。
表 3. 已上市 ONTs 致癌性试验完成情况汇总(不包括撤市药物)
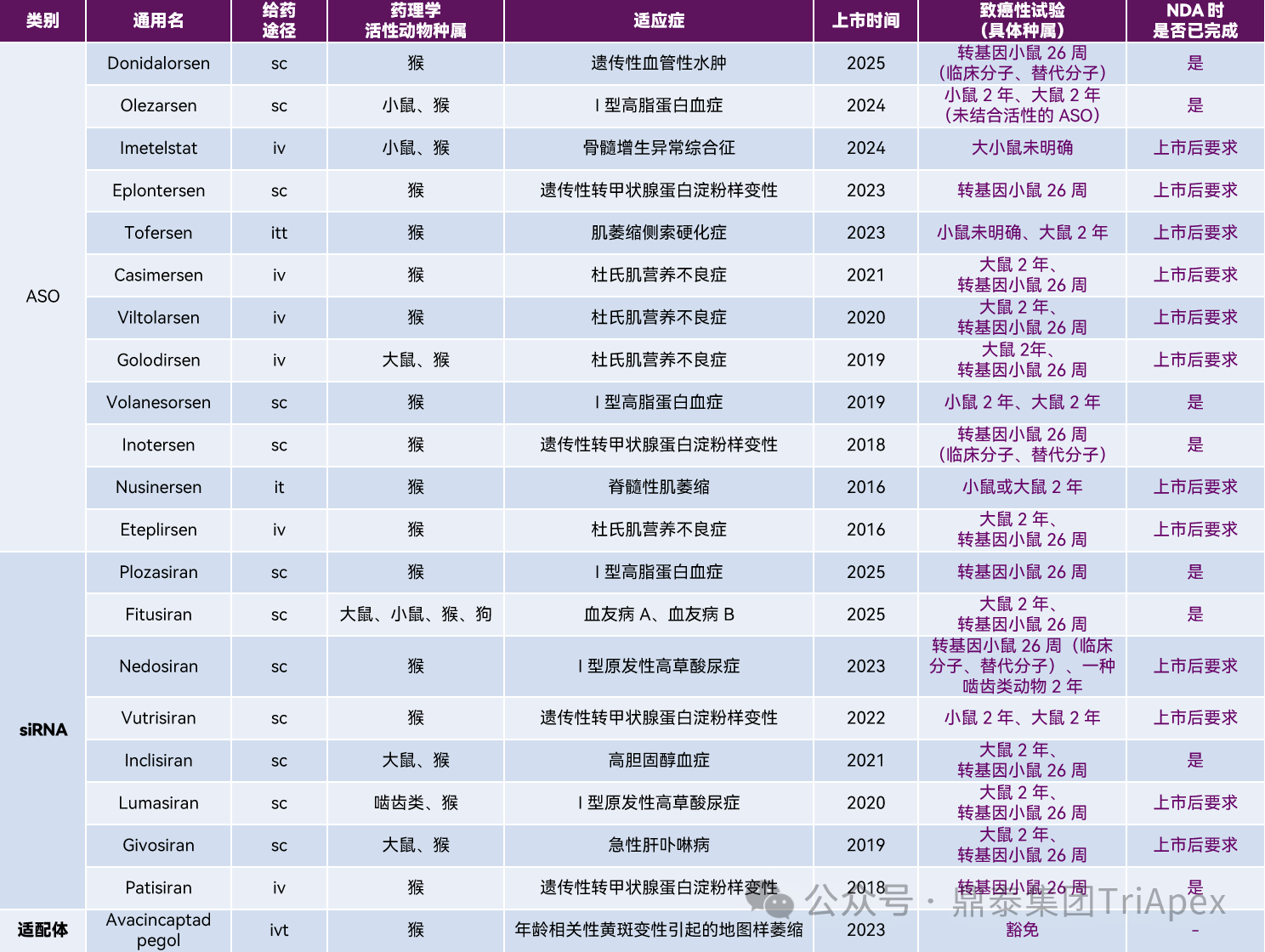
注:未单独标注供试品的,均采用临床分子。
从表 3 可以看出,已上市 ONTs 致癌性试验一般选择大鼠开展为期 2 年的致癌性试验,另外开展 1 项转基因小鼠 26 周致癌性试验或小鼠 2 年致癌性试验。对于属于已充分表征致癌性风险类别的 ONTs 类,进行单一种属的两年致癌性研究也是可行的[7]。
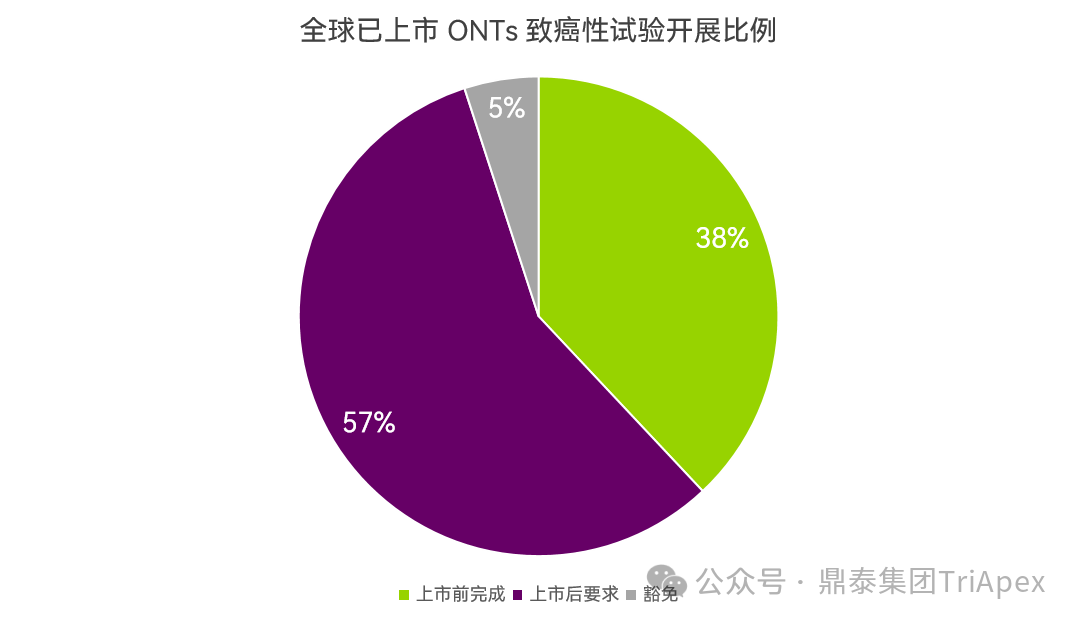
图 1. 全球已上市 ONTs 致癌性试验开展比例
致癌性试验的开展时机
从图 1 可以看出,已上市的 ONTs 中,8 款(占比 38%)在上市前完成了致癌性试验;12 款(占比 57%)则是在 NDA 后按要求开展致癌性试验,1 款获得豁免。
为何有的可在上市后开展?有的在上市前完成?有的可豁免开展?
这一差异主要是由于近年来,致癌性试验的策略发生了从“固定范式”向“个性化策略+WoE 分析”的转变。
ICH S1A 建议,对于“临床连续用药 6 个月以上”的药物,原则上需提交致癌性试验。然而,对于治疗慢性病的 ONTs(需长期给药),在实操过程中对于致癌性的开展时机,申请人采取了灵活策略:
如果药物的目标适应症是严重或危及生命的疾病,且现有治疗手段有限,即使需要长期用药,也可在上市后完成该项试验。
在上述上市后开展致癌试验的药物中,部分产品获得了孤儿药、突破性疗法或快速通道资格。这些资格可能在一定程度上支持了申请人加速审批途径,将确证性长期安全性数据(包括致癌性)作为上市后要求(Postmarketing Requirement, PMR)。这种做法确保了患者能尽快用上“救命药”,同时还能通过法规手段补全长期安全性数据。
为何部分药物在上市前完成了完整的致癌性研究?
就这一类药物的适应症来看,针对的是非致命性或已有成熟疗法的慢性病。在这种情况下,不开展完整的致癌性试验或许是“风险大于获益”的,因此,这部分产品往往在上市前即完成致癌性的完整评估。同时,如果在早期发现了一些特定风险信号,同样也会在上市前完成致癌性评价。
例如,Inotersen 在肝脏和肾脏组织中暴露较高,在 NDA 阶段即完成了转基因小鼠致癌性试验。对于 Patisiran 来讲,由于在雄性动物中可见细支气管肺泡腺瘤,在 NDA 阶段开展了转基因小鼠致癌性试验,原则上大鼠 2 年致癌性试验也应在 NDA 申请前完成,但是由于抗药抗体(针对 LNP)的形成导致药物暴露减少,故豁免了 2 年大鼠致癌性试验。
除此之外,2022 年 ICH S1B(R1) 指导原则的增补修订,标志着致癌性试验监管思维的革新。它不再要求所有药物都“一刀切”地进行 2 年的大鼠致癌试验,而是鼓励通过 WoE 进行综合评估。如果从药物靶点、信号通路、毒理学研究等综合分析,认为药物致癌风险很低,或者明确有致癌风险,则 2 年大鼠致癌性试验开展的意义并不大。
WoE 分析维度如下图所示,包括靶点生物学作用、次要药效学、重复给药毒性研究结果、对激素的影响、遗传毒性和免疫调节作用等。
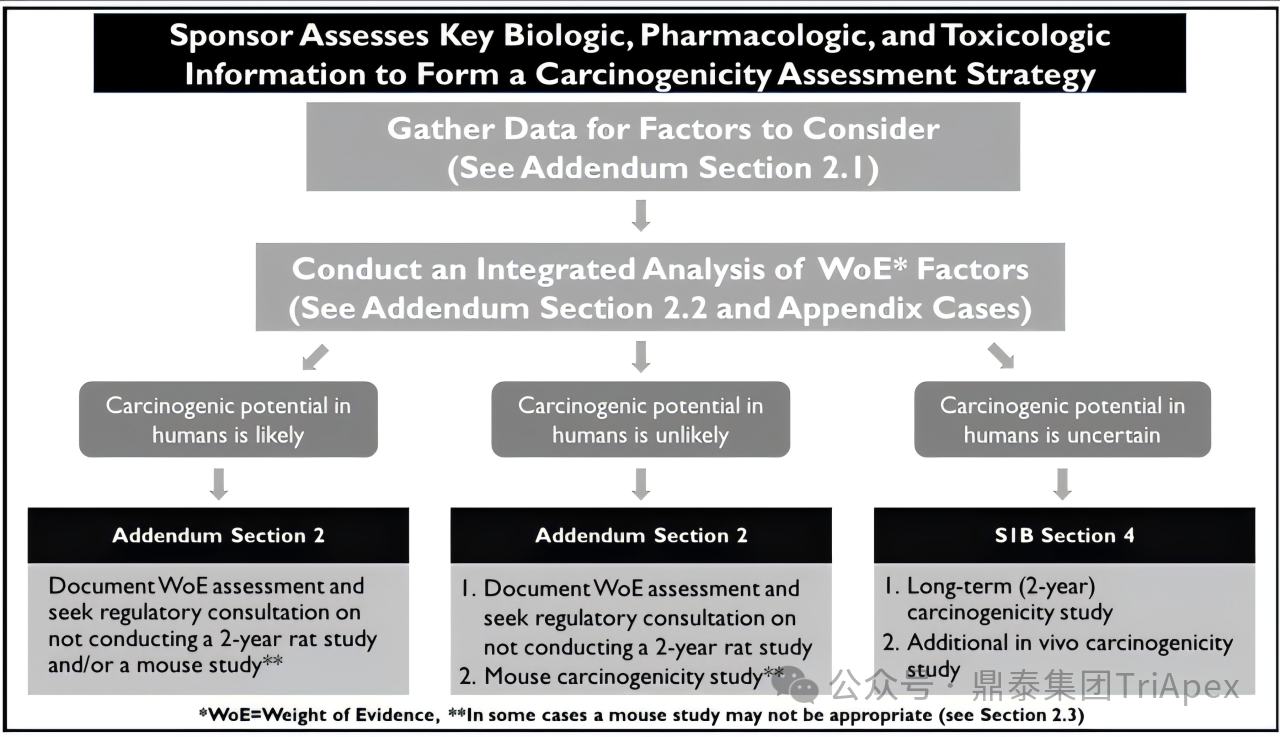
图 2. 致癌性评估策略的关键步骤和选择
(图片来源:S1B(R1) TESTING FOR CARCINOGENICITY OF PHARMACEUTICALS)
总体而言,ONTs 致癌性试验的开展时机并非统一标准,而是基于现有数据是否提示风险信号、以及临床获益-风险评估的结果进行差异化决策。
基于上述考量,接下来我们首先来详细解读最新上市的Fitusiran的致癌性试验设计、剂量选择逻辑与关键数据;随后,再以此为契机,探讨另一款上市 ONTs Avacincaptad Pegol 的致癌性试验豁免策略,以呈现不同科学背景下的监管考量。
从 Fitusiran 致癌性试验了解试验设计细节
剂量选择逻辑和关键数据
Fitusiran 是 FDA 于 2025 年批准的第 7 款 siRNA 药物,用于 12 岁及以上成人和青少年 A 型或 B 型血友病患者的常规预防,以减少或预防出血事件的发生,无论患者是否伴有凝血因子 VIII 或 IX 抑制物。
临床使用剂量及给药频率:由于抗凝血酶(AT)活性过高可能增加出血风险,过低则可能导致血栓,启动 Fitusiran 治疗前,须检测患者基础 AT 活性,仅当活性大于 60% 时,才能进行给药 —— 起始剂量为 50 mg,每 2 个月皮下注射一次。治疗期间需根据 AT 活性进行剂量和/或给药间隔调整;
对应的暴露量:MRHD 50 mg 下对应的 AUC 为 1290 ng·h/mL。
关于该产品上市历程的详细复盘请见往期文章他山之石-7丨siRNA 药物 Fitusiran 上市历程及临床开发路径总结。
Fitusiran 在小鼠、大鼠、恒河猴和犬中均具有药理活性,因为抗凝血酶 mRNA(来源于 SERPINC1 基因)的序列在各物种中高度保守。因此一般毒理和特殊毒理试验中动物种属的选择自由度较大,也无需为考察在靶毒性而制备替代分子。
Fitusiran 啮齿类动物一般毒理以及遗传毒理试验结果汇总见表 4[10],该结果为致癌性试验的剂量设计提供参考。Fitusiran 的啮齿类重复给药毒性试验中未见增生性或前肿瘤性病变,遗传毒理试验为阴性结果。但考虑到 Fitusiran 终生给药,故于 IND 获批后开展了 SD 大鼠和 CB6F1-TgN (RasH2)转基因小鼠致癌性试验。
表 4. Fitusiran 啮齿类动物一般毒和遗传毒试验结果汇总

SD 大鼠 2 年致癌性试验
1.1 方案设计
☆ 种属和周龄
SD 大鼠,给药开始时 8 周龄。
☆ 剂量设计依据
大鼠致癌性试验的给药剂量为:
雄性:0(0.9%氯化钠注射液),0.03、0.1 和 0.3 mg/kg;
雌性:0(0.9% 氯化钠注射液),0.1、0.3 和 1 mg/kg。
剂量选择依据:本试验的高剂量选择遵循了 ICH S1C(R2)指导原则的核心要求,综合考量了最大耐受剂量(MTD) 与药效学效应两大原则。
1)高剂量的确定(基于毒性终点与药理学放大效应):
雄性大鼠高剂量设为 0.3 mg/kg,雌性大鼠设为 1 mg/kg。该设定依据来自前期开展的慢性毒性试验:当雄性大鼠给药剂量升至 1 mg/kg、雌性大鼠升至 3 mg/kg时,观察到了因药理学作用过度放大而引发的严重不良反应,具体表现为出血性血栓相关事件,并直接导致了受试动物死亡。因此,本研究选择上述未见因药效过强直接致死的剂量作为高剂量。
2)中、低剂量的确定(基于暴露量):
中、低剂量组的设置主要依据药物在大鼠体内的系统暴露量(AUC)。通过选取覆盖不同倍数暴露水平的剂量,旨在探索剂量-暴露-效应关系,确保能够充分评估 Fitusiran 在从低到高暴露范围内的潜在的致癌性。
☆ 给药周期
溶媒对照组和供试品组皮下注射连续给药 104 周,每周给药 1 次(共计 104 次)。具体剂量和动物数见表 5。
☆ 观察指标
死亡/濒死、临床观察、体重、摄食量、大体观察、组织病理学检查
☆ 分析参数
生存率、肿瘤发生率。
表 5. SD 大鼠致癌性试验剂量与组别设计
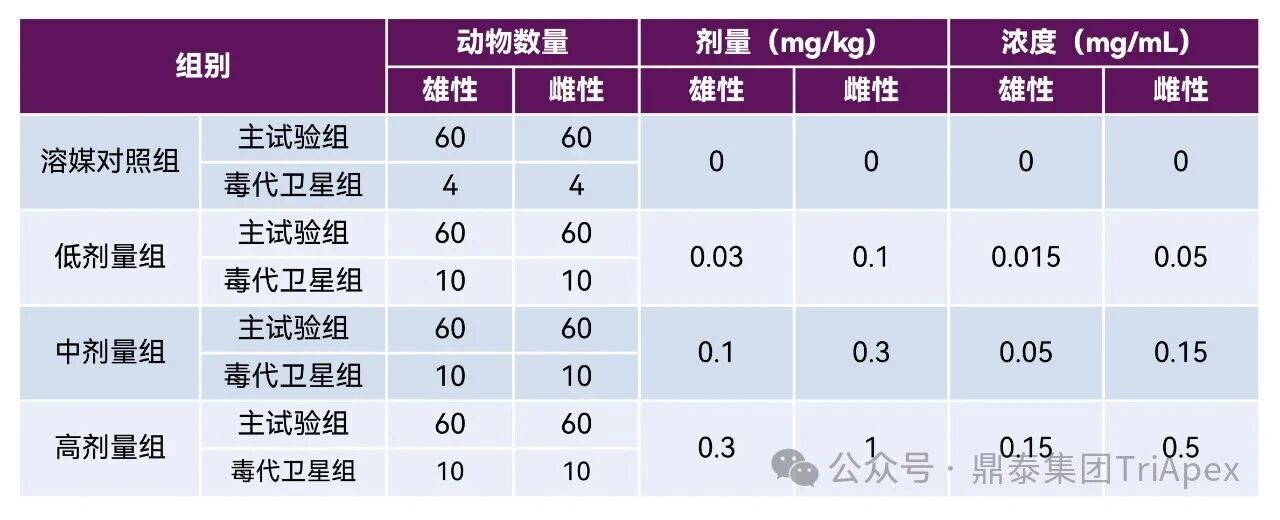
注:供试品配制采用的是 0.9% 的氯化钠注射液。给药体积为 2 mL/kg。
1.2 结果分析
1)死亡率
溶媒对照组与 Fitusiran 各剂量组均可见雌雄动物死亡,但与对照组相比,Fitusiran各剂量组死亡率均未见统计学差异及剂量反应关系。1 例中剂量组雄性动物和 1 例高剂量组雌性动物可见与 Fitusiran 相关的死亡(因血栓导致的大脑坏死,该效应与药理作用相关)。
表 6. SD 大鼠致癌性试验死亡汇总
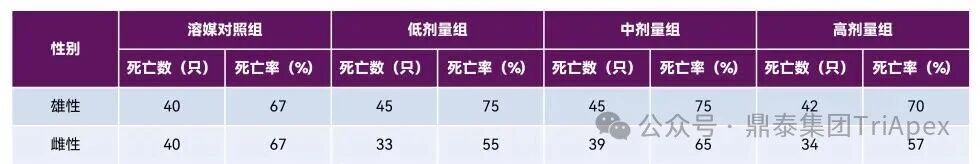
2)常规指标
临床观察、体重、摄食量、大体解剖均未见 Fitusiran 相关异常。
3)肿瘤发现
在非计划解剖和终末解剖中,在溶媒对照组及 Fitusiran 各剂量组动物观察到的肿瘤主要为雄性和雌性大鼠下丘脑垂体远端腺瘤,以及雌性大鼠乳腺肿瘤。上述肿瘤发现为此年龄段的 SD 大鼠常见的自发性肿瘤类型,其发生率与背景数据一致;且对照组与供试品组间的肿瘤发生率相近,故认为上述肿瘤发现与 Fitusiran 无关。
综上,Fitusiran 每周皮下注射给药,在雄性大鼠≤ 0.3 mg/kg、雌性大鼠≤ 1 mg/kg 剂量下未表现出致癌性。经 FDA 统计分析确认,大鼠致癌性数据中未观察到具有统计学差异的剂量-反应关系或组间差异。
4)毒代动力学
毒代动力学分析显示,在第 1 天(D1)和第 176 天(D176),大鼠体内的全身暴露水平(AUC)约为人类的 1-2 倍【以最大推荐人体剂量(MRHD)为基准计算】。
未进行 ADA 检测,可能与此前的试验已提示的免疫原性发生率较低有关。
1.3 提前终止
根据存活的动物数量,所有组别的雌性大鼠(含溶媒对照组)以及雄性大鼠低剂量组在 93/94 周终止;溶媒对照组(雄性)及雄性大鼠中、高剂量组在第 98/99 周终止。
表 7. 提前终止情况汇总
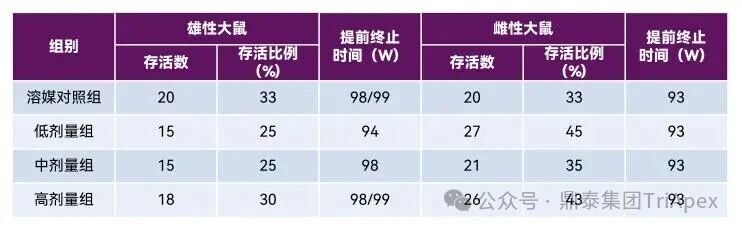
上述提前终止符合以下标准中的 ② 和 ③:
① 如果濒死/死亡有剂量相关性,当高剂量存活主试验动物数为 20 只时,停止高剂量组给药;如果低剂量存活 18 只,高剂量剩余 20 只时,继续给药,不认为是剂量相关;
② 如果对照组动物单性别的存活动物数剩余 20 只时,该性别所有剂量组动物均进行终末处理;
③ 当给药时间<100 周时,如果某个剂量组单性别存活动物数剩余 15 只,则仅将该剂量组该性别动物进行终末处理;
④ 当给药时间≥100 周时,如果某个剂量组单性别的存活动物数剩余至 15 只,则该性别所有组动物(包括对照组)均进行终末处理。
⑤ 当试验早期阶段发现动物生存率降低或动物有明显毒性反应时,可适当降低某个/全部供试品组剂量。
1.4 生存率和生存曲线
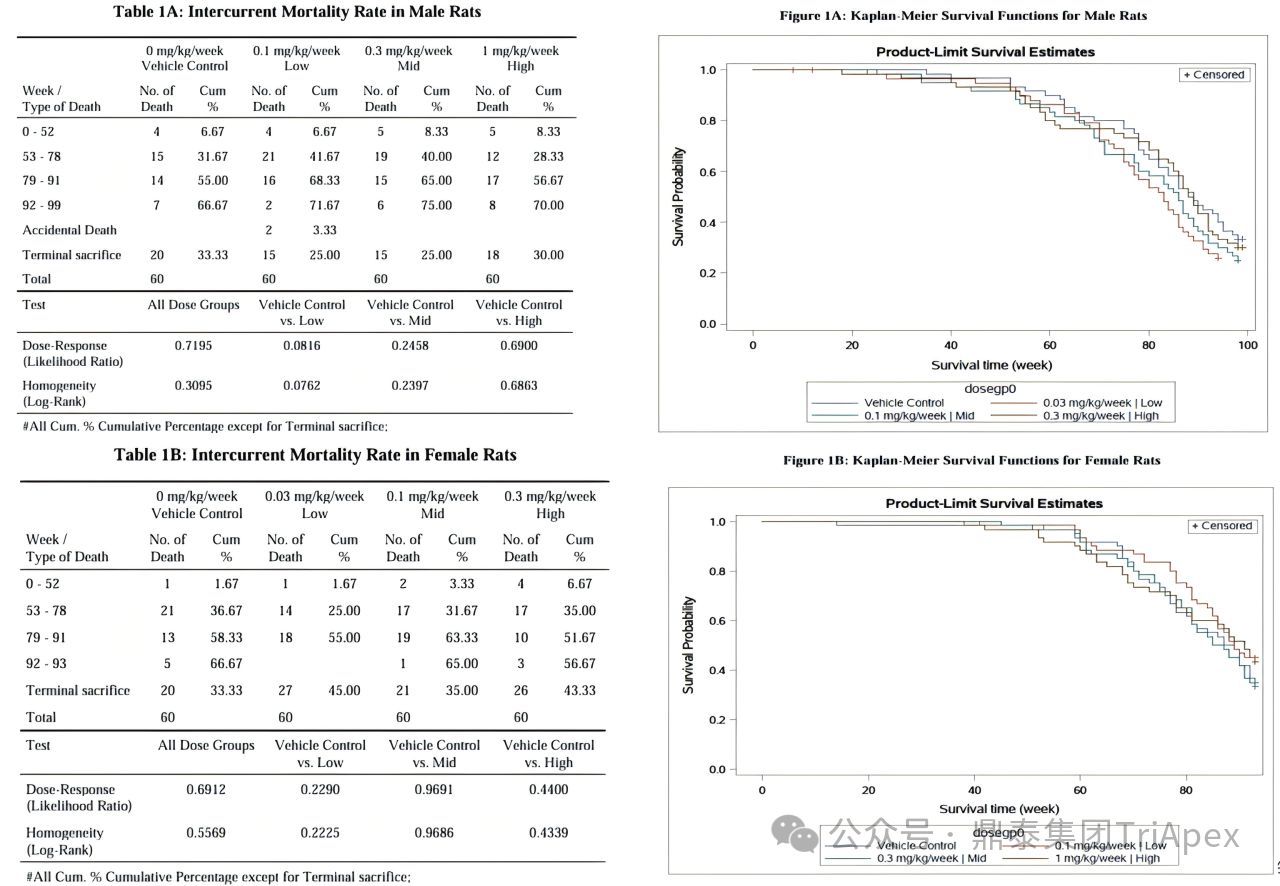
图 3. Fitusiran SD 大鼠致癌性试验生存率和生存曲线
(图片来源:Fitusiran Integrated Review)
1.4.1 分析方法
1)死亡数据合并与分析方法
将死亡时间相近的动物数据合并至同一观察区间内,并统一纳入生存分析统计。本试验采用 Peto 现患率法进行死亡率分析,按固定时间间隔(0-52 周、53-78 周、79-91 周、92-104 周及终末解剖期,或类似区间)划分观察期,该方法参考自 FDA 行业指南[11]。
2)生存率估计与曲线绘制
使用 Kaplan-Meier 乘积极限法估计各组的生存率与平均生存时间,并绘制生存曲线。在分析中,将明确与供试品不相关的死亡数据按截尾数据处理,而明确因供试品影响致死或濒死状态下安乐死的动物数据则作为完整死亡事件纳入。
3)统计比较与趋势检验
按性别分别采用对数秩检验比较各组生存曲线是否存在统计学差异。若检验显示差异显著(P ≤ 0.05),则进一步采用 Peto 双侧趋势检验分析死亡率的整体剂量相关性,并比较各给药组与溶媒对照组的差异。所有统计分析均在 5% 的显著性水平下进行。
1.4.2 结果
雄性大鼠低、中、高剂量组、溶媒对照组分别存活至终末解剖 20 只(33%)、15 只(25%)、15 只(25%)、18 只(30%),雌性大鼠分别存活至终末解剖 20 只(33%)、27 只(45%)、21 只(35%)、26 只(43%)。未见与 Fitusiran 相关的死亡率增加,亦未见死亡率统计学上的显著变化。
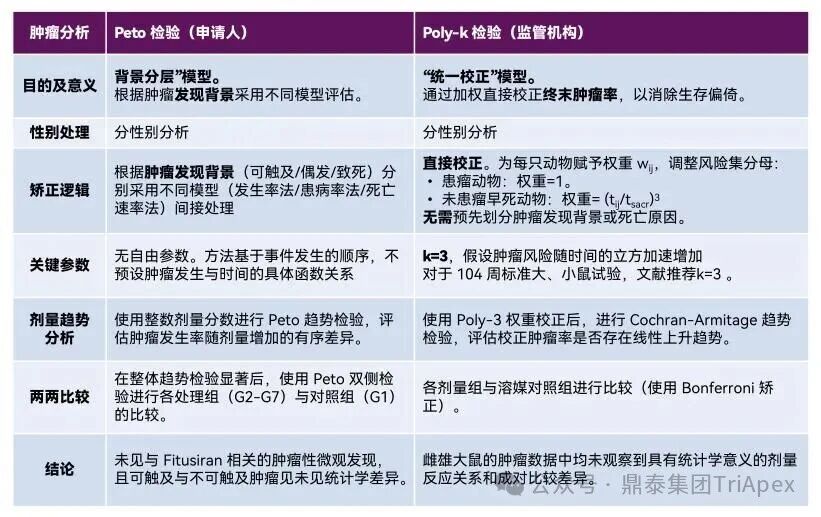
1.5 肿瘤发生率分析与对比
为验证申请人提交的分析结论,并应毒理审评要求进行补充分析,监管机构基于申请人提供的电子数据,对生存率及肿瘤发生率进行了独立统计分析。
在生存率分析中,采用 Kaplan-Meier 乘积极限法估计生存率、绘制生存曲线,并通过 Log-rank 检验比较各组差异。统计分析结果显示,监管机构的独立分析与申请人报告结论一致。肿瘤分析对比过程见表 8。
表 8. 申请人与监管机构肿瘤分析及对比过程
CB6F1-TgN (RasH2) 转基因小鼠致癌试验
2.1 方案设计
☆ 种属和周龄
CB6F1-TgN (RasH2) 小鼠,给药开始时 9 周龄[12]。
☆ 剂量设计依据
转基因小鼠致癌性试验的给药剂量为:
◆ 雄性:0(0.9% 氯化钠注射液),0.05、0.15 和 0.5 mg/kg;
◆ 雌性:0(0.9% 氯化钠注射液),0.025、0.08 和 0.25 mg/kg。
◆ 同时设置阳性对照组(MNU)75 mg/kg。
剂量选择依据:
与 2 年大鼠致癌性试验有所不同,转基因小鼠致癌性试验更关注的是动物的耐受性,即基于毒性改变来选择高剂量,而非体内特定暴露量倍数[13]-[16] ,这一思路与 ICH S1C(R2)中“需要采取灵活的方法选择剂量”的原则相呼应;
同时,ICH S1B(R1)增补文件也明确,在 RasH2-Tg 小鼠模型中,ICH S1C(R2)中列出的在剂量限制性毒性或其他标准不适用时,采用血浆暴露量(AUC)比值选择高剂量尚未被全球接受。
在血友病 A 型和 B 型以及野生型小鼠中,单次皮下注射 1-30 mg/kg futusiran后,可见 AT 被剂量依赖性的抑制(通过 mRNA、抗原水平和活性的下降来测量)。
Fitusiran 高剂量的设计基于 28 天重复给药剂量探索试验中出现的体重下降,而低、中剂量的设置是基于适当的剂量间隔。
☆ 给药周期
溶媒对照组和供试品组皮下注射连续给药 26 周,每周给药 1 次(共给药 27 次),阳性对照 MNU 在 D1 腹腔注射给药1次。详见表 9。
☆ 观察指标
死亡/濒死、临床观察、体重、摄食量、大体观察、组织病理学检查、毒代动力学。
☆ 分析参数:生存率、肿瘤发生率
表 9. CB6F1-TgN (RasH2) 转基因小鼠致癌性试验剂量与组别设计
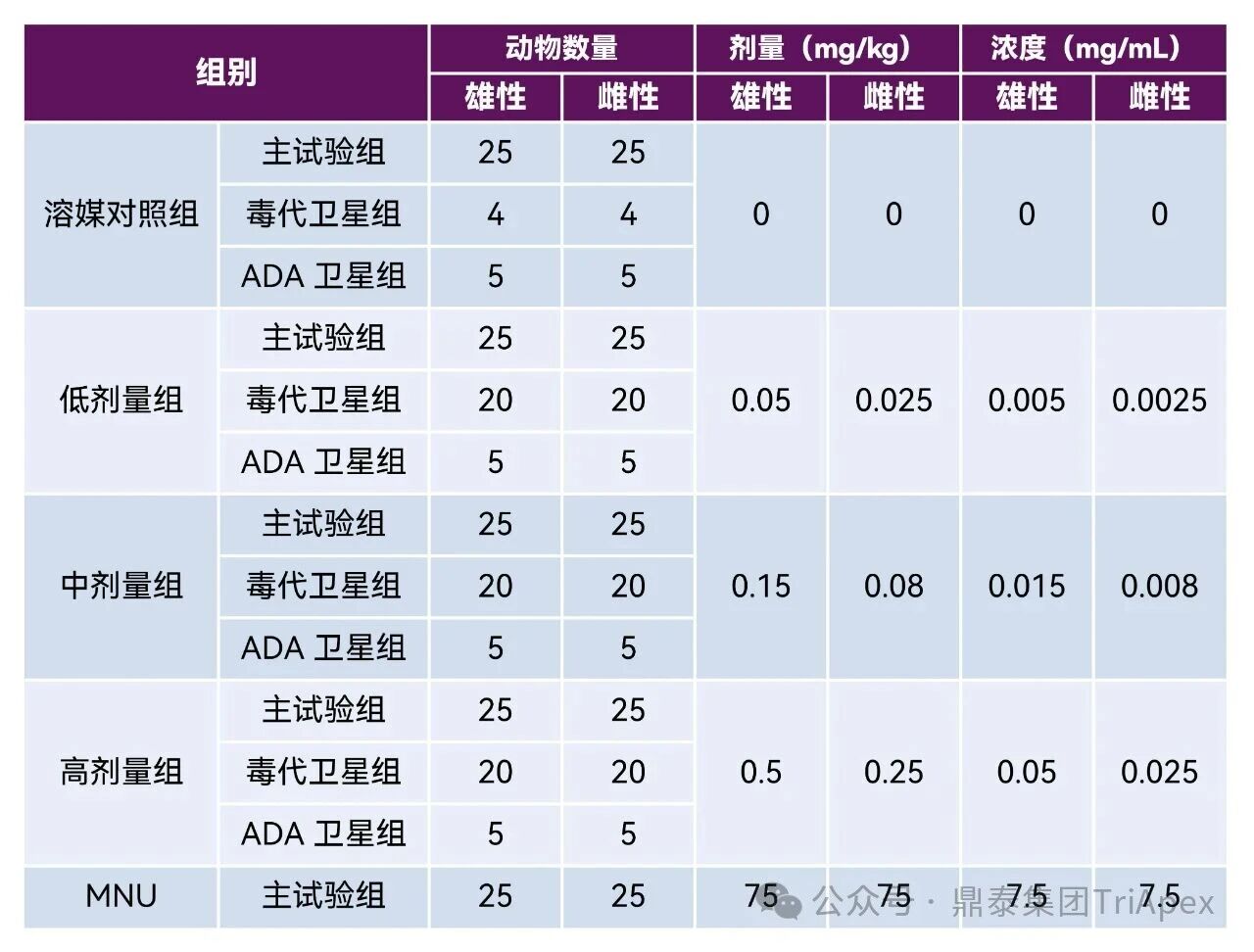
注:供试品配制采用的是 0.9% 的氯化钠注射液,MNU(N-甲基-N-亚硝基脲)配制采用的是柠檬酸缓冲液(pH 4.5)。给药体积为 10 mL/kg。
2.2 结果分析
1)死亡率
除了阳性对照组,各组雄性或雌性小鼠的死亡率在所有剂量组间均未见统计学上显著的剂量反应关系以及两两比较结果。
表 10. CB6F1-TgN (RasH2) 转基因小鼠致癌性试验死亡汇总
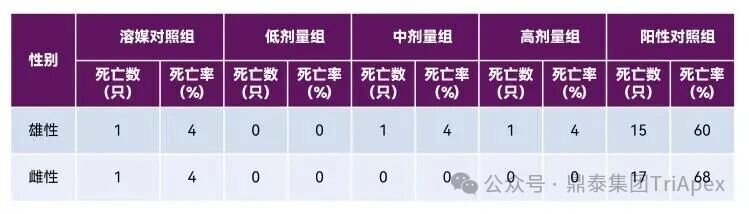
2)常规指标
临床观察、体重、摄食量均未见 Fitusiran 给药相关的异常。
大体观察:未见与 Fitusiran 相关的肉眼异常。对照组和 Fitusiran 各剂量组的小鼠胃中均可见凸起、结节和/或肿块,但发生率较低,与鳞状或腺体增生相关。观察结果总体上与该年龄段的 RasH2 Tg/WT 小鼠品系常见情况一致。
表 11. CB6F1-TgN (RasH2) 转基因小鼠致癌性试验大体观察结果汇总
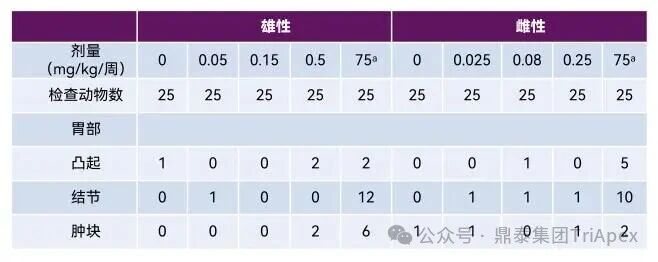
a:阳性对照组(MNU),D1 单次给药。
3)组织病理学
肿瘤相关:
肺脏细支气管肺泡癌和细支气管肺泡腺癌和脾脏血管肉瘤
◆ 肺脏:可见细支气管肺泡癌和细支气管肺泡腺癌,未见剂量相关性。考虑为自发性肿瘤;
◆ 脾脏:仅 Fitusiran 给药组可见血管肉瘤,且略高于机构历史对照数据,但未见剂量相关性亦未见统计学差异,为偶发性肿瘤。
非肿瘤相关:
胃部可见混合细胞浸润发生率增加,鳞状黏膜增生的严重程度增加。
表 12. CB6F1-TgN (RasH2) 转基因小鼠致癌性试验肿瘤相关组织病理学结果汇总
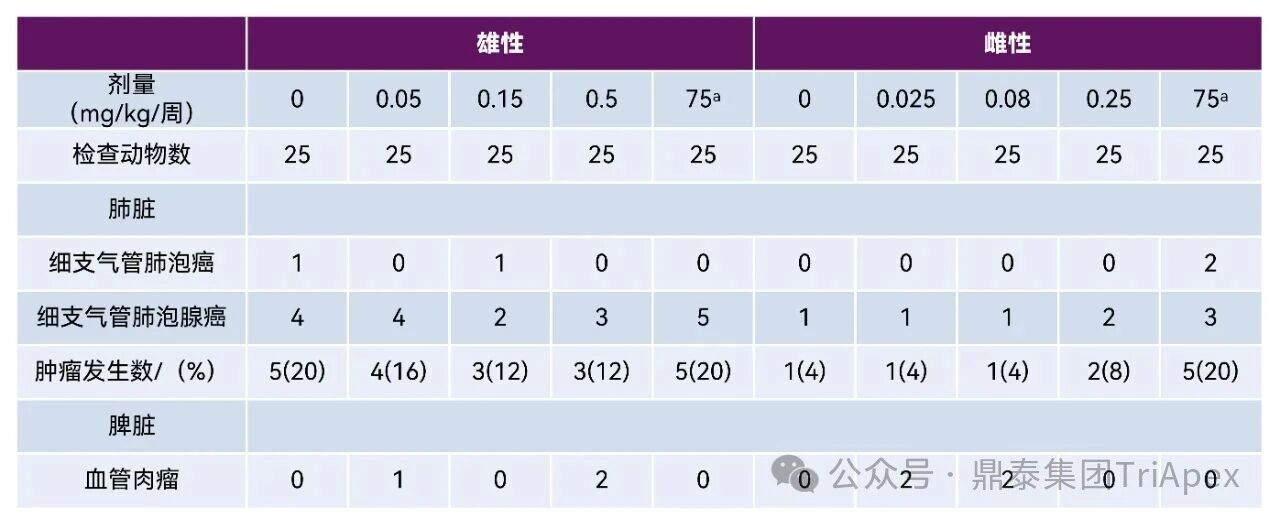
a:阳性对照组(MNU),D1 单次给药。
4)毒代动力学:
毒代动力学分析在给药后第 1 天(D1)和第 183 天(D183)进行暴露量测定,由于采血量不足,毒代动力学仅针对第 183 天的结果进行解释分析。以最大推荐人体剂量(MRHD)为基准,并将给药频率换算为双月剂量后,小鼠的系统性暴露量(AUC)低于人类(暴露倍数<1倍)。
Fitusiran 致癌性试验给予的启示
监管基于其分子特性(持续降低抗凝血酶,可能带来长期代偿性细胞增生的潜在风险)与适应症(血友病长期预防治疗>6 个月)进行风险研判,且缺乏同类 ONTs 针对该靶点的长期致癌性历史数据,因此无法豁免致癌性试验。
申请人于 IND 获批后分别向监管机构提交了大鼠和转基因小鼠的致癌性试验方案,并进行会议沟通。
试验设计上严格遵循 ICH S1C(R2)、ICH M3 及 ICH S6 等国际指导原则,体现了 ONTs 致癌性评价应“基于分子特性灵活适配现有监管框架”的基本思路。
剂量设计上以 MTD、药代动力学暴露量、药效学指标等为依据,试验结果结合 SD 大鼠与 CB6F1-TgN (RasH2) 转基因小鼠的背景肿瘤数据进行综合评估。
尤为值得关注的是,监管机构基于申请人提供的电子数据开展了独立验证分析,并得出与申请人一致的未见药物相关的致癌性的结论,这不仅增强了评价结论的公信力,也提示在后续 ONTs 开发中,高质量、可追溯的原始数据以及申请人与监管方的良性互动,将是推动致癌性评价科学认知积累的关键。
从 Avacincaptad pegol 经验看如何运用 WoE 证据进行致癌性评估
基于 WoE 的豁免案例
我们的观点回顾
随着药物安全评估对科学性和伦理要求的不断提高,国际协调会议(ICH)在 2022年修订的 S1B(R1)指南中,引入了基于 WoE 的安全性评价方法[17]。
WoE 的核心是六个互相关联的因素,分别为:
◆ 靶点生物学
◆ 次要药理学
◆ 慢性毒性试验组织病理学
◆ 对激素的影响
◆ 遗传毒性
◆ 免疫调节作用
依据 ICH S1B(R1) 及 FDA 发布的《寡核苷酸治疗药物:非临床安全性评价指南》,ONTs 的致癌性评价决策应当基于“WoE”进行。ONTs 若存在人类特异性的脱靶杂交依赖性活性,并可能带来致癌风险,则可采用 WoE 综合评估、临床监测、知情同意说明潜在风险以及合适的产品标签等策略,而非仅依赖动物实验数据。
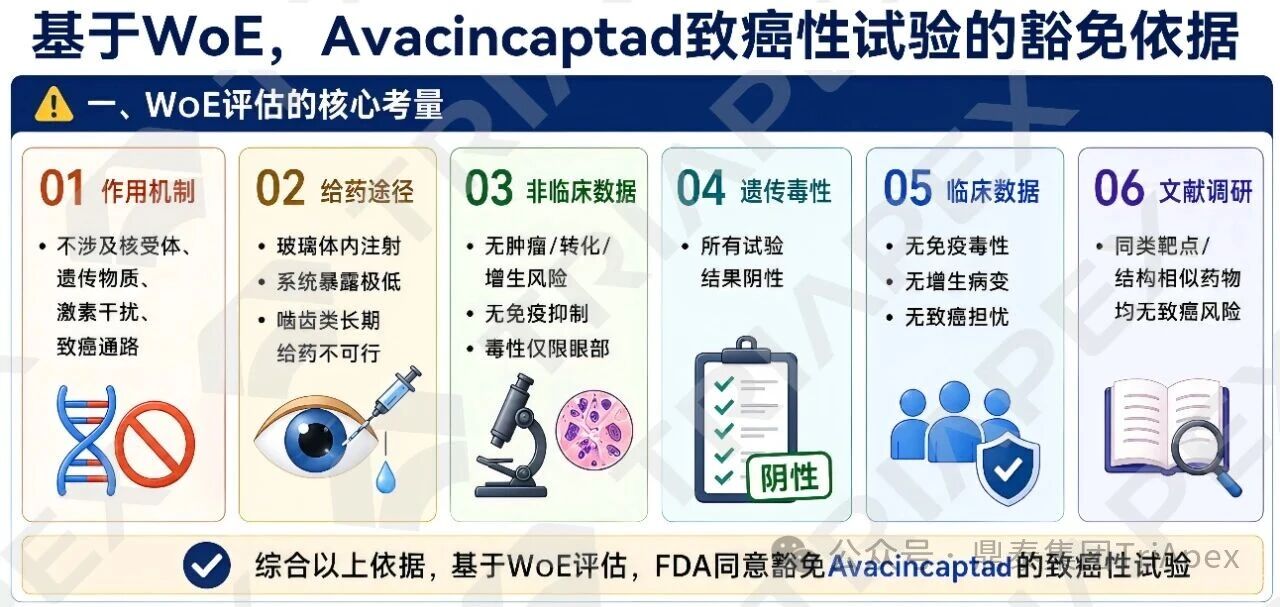
2023 年上市的 ONTs Avacincaptad pegol(玻璃体内注射,每月一次),根据指导原则,除非有明显的全身暴露或相关担忧,经眼给予的药物通常不需要进行致癌试验。申请人基于 WoE 证据申请豁免致癌性试验,并获得 FDA 认可。本文对其主要依据梳理如下:
1)作用机制
作为 C5 抑制剂,其作用机制不涉及核/激素受体结合、遗传物质相互作用、激素干扰或已知与人类癌症发展相关的细胞通路。
2)给药途径与系统暴露
临床采用玻璃体内注射,在 SD 大鼠和食蟹猴中系统暴露量远低于静脉给药,且该途径在啮齿类动物中长期给药不可行。临床推荐剂量下引发全身性药理/致癌效应的可能性极低。
3)非临床数据
未发现提示肿瘤形成、转化或增生性病变风险增加的迹象;未见免疫抑制,所有毒性改变均局限于眼部。
4)遗传试验
所有遗传毒性试验结果均为阴性。
5)临床数据
迄今为止的临床试验未观察到免疫毒性或增生性病变,无致癌风险担忧。
6)文献调研
同类药理学靶点或结构相似的药物均未提示致癌性风险。
综合以上证据,FDA 最终同意免除该药物在大鼠和小鼠中的致癌性试验要求。
未来方向
从“常规范式”到“科学化、个体化的整合性评估”
目前,ONTs 的致癌性评估通常仍需参照小分子药物标准思路,对于有必要开展致癌性试验的,通常建议开展两种啮齿类动物的长周期试验。虽然多数监管机构在实践中仍倾向于要求传统的致癌性试验,但随着对特定化学修饰结构安全性数据的积累,未来有望开发出更具针对性的补充方法[18]-[21]。
☆ 关键建议
1)早期规划:基于“证据权重”的评估框架;
2)科学设计:合理选择试验种属与剂量设计;
3)提前沟通:积极与监管机构沟通,提前预期并充分设计和评估潜在的致癌性风险或探讨试验豁免(WoE)的可能性;
4)深化理解:持续加强药物作用机制与潜在风险的理解。
☆ 常规范式基础上整合新思路
1)新工具:开发寡核苷酸特异性致癌风险预测模型
针对 ONTs 独特的分子结构与作用机制,开发基于机器学习/人工智能(ML/AI)的专属预测模型,整合序列特征、化学修饰、递送系统及免疫调节潜能等关键参数,为评价策略的早期设计提供科学依据。
2)新技术:推动基于 NAMs 与转录组生物标志物的辅助评价工具
一方面,发展人源 3D 类器官等模型,模拟药物在关键靶器官长期暴露后慢性炎症微环境的变化;另一方面,挖掘与致癌性早期事件相关的转录组生物标志物,构建基于分子标志物的辅助评价体系,实现致癌风险的早期识别。
3)新平台:利用数字病理与 AI 图像识别技术,建立跨项目数据共享平台
借助数字病理与 AI 图像识别技术,实现组织切片的高通量分析与微小病变的精准识别,提升检出灵敏度与判读一致性。同时,建立跨项目数据共享平台,整合历史对照数据与同类药物试验结果,为 WoE 评估提供更坚实的参考基准。
结语
ONTs 的致癌性评价正经历从“常规范式”向“科学化、个体化评估”的重要转变。随着 WoE 理念的逐步应用,传统的致癌性试验策略可能不能充分满足此类新型疗法的评价需求,更需要基于药物作用机制(MoA)、分子结构特征、药代动力学及平台安全性数据积累的整合性评估框架。未来,ONTs 致癌性评价的发展方向应聚焦于以下几个方面:
深入解析 ONTs 与致癌性风险相关的可能机制(如免疫调节、RNAi 脱靶、组织蓄积与慢性炎症等),为非临床评价策略的设计提供坚实的科学基础;
充分利用同类药物的安全性数据,探索 3R 原则下的优化和补充评估工具,如体外细胞转化模型、类器官及生物信息学预测等,与传统长期动物试验形成互补性证据;
申请人应积极与监管机构开展早期沟通,基于药物特性与研究基础,就致癌性试验的必要性、模型选择、剂量设置和给药方案等达成共识;并探索与自身项目整体开发进程、关键性临床试验和 NDA 申报进度相匹配、资源合理配置的致癌性试验研发策略。
总之,ONTs 致癌性的科学评估与监管考量,本质上是在新兴疗法快速发展与传统评价体系之间寻求动态平衡的过程。坚持以科学证据为基础、以作用机制为导向、以沟通为桥梁,有助于构建既符合监管机构安全性评价要求又契合药物技术特点的评价路径,最终推动 ONTs 这一药物创新“第三次浪潮”行稳致远。
参考资料: