
2021-09-28 15:36:49来源:新浪医药新闻浏览量:955
导读:2015年-2021年,中国创新药发展现状如何?与国际之间还存在哪些差距,预计什么时候能够实现追赶与超越?
数据显示,2021年上半年,我国批准创新药21个,超过了2020年全国审评通过的创新药数量,刷新了我国创新药审评记录。21个创新药包括新冠病毒疫苗、肿瘤、免疫系统疾病、罕见病等领域的临床急需治疗药物,其中多个为我国自主研发并拥有自主知识产权的产品。
我国创新药快速发展繁荣背后,源自2015年之后中国药品审评审批加速、ICH指导原则落地等一系列的综合改革,在此之下,我国药品监管体系逐步与国际接轨,趋于成熟。
2015年-2021年,中国创新药发展现状如何?与国际之间还存在哪些差距,预计什么时候能够实现追赶与超越?在中国药企热火朝天进行创新转型升级当中,同时也伴随来了一些棘手的问题,如靶点同质化、内卷,如何快速商业化等,中国创新药未来的路在何方,又该如何进行创新、定义创新?在2021年西普会上,结合创新药本土和国际发展的实际情况,业界大佬们是这样说的。
01 7年“脱胎换骨”中国创新药水平如何?
2015年前,外部政策环境因素与市场行为不规范因素严重限制了中国制药企业创新发展的积极性和动力,医药行业长期处于低水平仿制阶段。2015年开始,国家药品领域的一系列重大改革举措,中国医药产业迅速进入了快速跟跑的创新转型发展期。
2015年,可以说是中国医药创新元年。依此来算,中国创新药真正发展的历程,不过才短短7年。
在亚盛医药董事长兼CEO杨大俊看来,2015年之前,中国对于创新药的定义为“只要国内没有就是创新药,享受1.1类新药的待遇”。但是在2015年之后,这个定义发生变化,“国内外新”才能算得上是创新药。
百济神州总裁吴晓滨认为,2015年是中国创新药的元年,此后中国创新药研发速度非常之快。其中,可以看到由于创新药快速发展,也带来了大量的临床试验。2001年,全国的临床试验只有360个,其中一半是外企,十年以后已经发展到1700个临床试验在同时进行,而且1300多个都是本土创新企业在做,质量上已经发生了巨大转变。
“过去中国大量的临床试验是验证性的试验,重复以前的试验验证性的试验PK桥接的试验。现在中国有一千多个试验已进行临床一期,这些完全是探索性的试验,完全是基础式创新,这一点会大大改善中国以后的创新药格局。”他谈道。
2015年后,除了国家政策的支持,资本也在大力助推中国医药创新。2018年港股生物医药公司上市制度的改革与中国科创板的建立,医药产业创新发展的源动力得到了充分的释放。据了解,中国生物医药公司在港股已经融资1200多个亿,科创板迄今为止600多亿,两年时间已经远远超过了国家对三个十一五的计划,金融市场推动带来了巨大的红利,很多公司大力布局研发创新药。
在中康科技创新药数据产品负责人安淑兰看来,中国创新药企发展模式已从独自开荒拓土向多元化路径纵横发展。中国新生代创新药企已经完成0-1原始积累,接下来将由1-100+迈进。
其中,2010年代出生的创新药企的成长模式较上代更加灵活,他们通过独立自主的研发,合作等多种形式实现螺旋上升直至成熟,中国创新药企逐步将视野拓展至全球,并重视深度经营。
中国创新药技术迈入新台阶,这当中生物药领域或将迎来弯道超车。继贝达成为第一个破土的拓荒者后,我国创新药领域的技术发展也呈现快速迭代景象,从埃克替尼到安罗替尼,从PD-1到现在各种新靶点的fast-follow中国创新药技术发展已迈入新台阶,生物药领域或将弯道超车,中国的药物研发已脱胎换骨展现了新面貌。
中国药物开发进程演变

来源:中康FIC数据库
得益于2015年的改革,此后6年,我国已建立了一套相对完整地医药创新生态系统。这当中,我国获批的创新药品种数量高速增长,历经7年,从药品审评审批到临床试验管理,我国研发端的监管体系已逐步接轨国际,趋向成熟。
中康FIC数据库也显示,中国创新企甚至已开始朝向“全球新”迈进,数个“全球新”药物管线进入到了临床阶段,例如君实生物的J004,是全球首个特异性针对B和T淋巴细胞衰减因子(BTLA)的重组人源化IgG4K单克隆抗体。
在各类创新要素相互作用,良性循环,我国从医药创新全球第三梯队进阶到第二梯队前列,对全球的研发管线、产品数量的贡献约至14%,占全球排名第二。中国创新药市场将迎来蓬勃发展,运用前景广阔,未来可期。
从2015年的寥寥无几,到如今14%的占比,在吴晓滨看来,照这个速度发展下去,再过几年,中国创新药在全世界创新药的管线里若达到30%,这个世界局面将完全改变。
“创新药的逻辑是先从小的适应症有条件批准,逐渐到大的适应症推向全球,目前中国创新制药公司还处在早期阶段。”吴晓滨介绍道,但是随着中国创新药的不断发展,中国新药一定会向国外创新药一样,在全球开展临床试验,在大的适应症实现突破,这些创新硕果不仅会服务中国患者,也会服务于全球患者。
而行至2021年,中康科技副总裁肖淋表示,我国的医药产业创新发展将再次进入关键转折点,快速进入并跑期,在这一阶段,基于研发拥有全球知识产权的新药研发企业将成为我国医药产业创新发展的领跑者。
02 同质化、内卷严重...中国创新药迎新挑战
与此同时,中国医药营商环境整体在发生变化。随着带量采购、一致性评价等医药政策的推进,仿制药进入低利润时代,也在倒逼着中国药企做创新,进行转型升级。在这样的氛围下,中国创新药也正在面临着一些挑战。
据统计,中国有225家企业开展了超200余种靶点的国际化进程,而肿瘤领域占比超60%为主要趋势,其次为感染、代谢及呼吸系统疾病。不难看到,肿瘤治疗药物是中国新药研发的主要领域。
“大家都知道,第一个挑战就是一窝蜂的上。”吴晓滨指出,拿肿瘤药PD-1来说,在研的PD-1已经有几十家,靶点扎堆,研发同质化严重。
针对这一现象,CDE发布了一则剑指伪创新的指导性文件。今年7月,CDE关于公开征求《以临床价值为导向的抗肿瘤药物临床研发指导原则》意见的通知,引发行业热议,对市场带来巨大冲击。
该文件的出台可以说是一个转折的标志。王如伟分析称,可以说前十年,我国创新药研发都是在快速跟进。在这之后,后十年中国的医药创新将被重新定义。当然这当中也有变与不变,他指出,以患者为中心的核心一直没有改变。接下来,中国医药创新会是进一步落实以临床价值为导向,以患者需求为核心的方向上。
他指出,PD-1靶点扎堆,高水平浪费等现象出现,原因就是在创新过程中,我们没有真正去理解创新的要素。
“回到国际市场,我们可以看到全世界最大的药企PD-1两年保持100亿美金,O药也在80亿左右,全球前十位的药物销售加起来超过1000亿美金,但中国还远远达不到。生物药未来十年要诞生伟大的产品和伟大的企业,结合西药研发的特点,这里面需要我们用大量的技术、资金来支撑,还要思考如何提高效率等。”王如伟说道。
在他看来,政策方向和预期没有改变,持续向国际一流看齐。产业创新和升级是一个长期过程,不过度解读政策影响。该《原则》强调的是“临床价值”和精准医疗,这当中me-too同样具备临床价值,如降低患者负担和经济学价值。此外,CDE新政长期利好创新药头部公司及差异化公司,CXO赛道持续看好。
而扎堆的靶点也迎来了降温,今年已迎来可喜的变化。中康FIC数据库显示,在申报1类临床的新药靶点中,今年靶点布局集中度明显降低,紧有1家申报的靶点占比22%,由于PD-1、EGFR等靶点因市场的过渡饱和占比有所降,CDK4/6、VEGFR、CTLA-4等相对较新靶点也未呈现拥挤现象,相较于去年冷静许多。整体来看,创新药靶点布局集中度降低,对靶点的技术应用更加成熟。
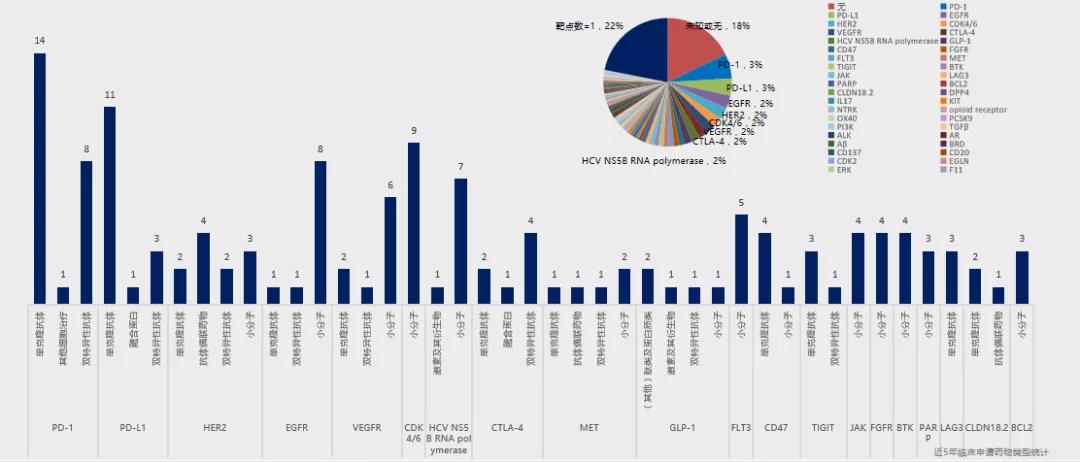
来源:中康FIC数据库
从靶点类型来看,CD家族占比较高,其中CD47、CD137、CD20等排名靠前:在技术类型上,小分子药物虽然是主力,但各个靶点下呈现了更加多样化的技术发展,预示当前中国创新药对靶点理解深度有所提升且对药物开发的技术运用更加成熟。
除了靶点同质化问题突出,另外,中国创新药在价格、进院等方面也面临挑战,价格走向何方,市场在哪里?创新药产业如何可持续发展,进院如何打通“最后一公里”等。
靶点扎堆、适应症竞争激烈的创新药弊端开始突显,用时下流行的词来说,首个表现就是内卷,广谱抗癌药PD-1价格下行,有沦为普药的迹象,恒瑞、百济神州、君实、信达等PD-1生产企业也开始瞄准更为广阔的市场,做全球多中心临床试验,出海拓展国际市场,推进商业化进程。
吴晓滨坦言,我们的创新价格已经把创新药欧美的价格降低到了十分之一,还能够降低多少?我们需要找到创新药的可支付性,和老百姓可以负担的能力,以及产业持续发展之间的一个平衡点,后续还有许多的创新药需要进入国家医保,这一系列的问题都是中国创新药发展在推进当中面临的直接挑战。
创新药,尤其是医保谈判之后的创新药如何进入医院,这一问题也在开始被逐步解决。今年,国家医保局会同国家卫健委出台《关于建立完善国家医保谈判药品“双通道”管理机制的指导意见》,确保国家医保谈判药品顺利落地,提升其保障供应水平。
安淑兰对此也有见解,她认为,创新药通过国谈进入医保的时间急速缩短,但也面临价格大幅下降问题。因此,“双循环”发展成为创新药企业发展的必经之路。
国内市场中,创新药通过国谈进入医保的时间极大缩短,商业化效率迅速提升,价值得以快速体现,“内循环”的效果已经显现;国际市场,创新药管线从几年前的高额引进到近两年的高额授权,亦充分体现了国际市场对中国创新药的价值认可,“外循环”效益明显。
杨大俊也指出,未来中国创新药会有两条路,一个是专利保护,一个是按照国际标准去竞争全球的市场。他表示,在生物药竞争激烈的背景下,药企占领先机非常重要。因此,一方面是早期要有引进,在时间差上占领中国市场;另一方面,最重要的是不断地有中国本土的研发企业做出产品,通过海外合作加强中国医药研发以及提高市值。
值得一提的是,2018年中国创新药企开始大量引进海外品种以快速建立管线格局,进而加速产品的上市;经历了2019年的快速过渡后,这些国内生产的大批创新药走出国门,快速、高效的实现了商业化目标。随着国际化监管体系接轨,产品授权的的交易价格快速提升,中国创新药也已初步受到国际认可。
7年蝶变,中国创新药已经迎来不少硕果,进入新的转折时期,阵痛在所难免。但中国医药创新的黄金时代已至,创新加速、差异化创新和全球创新的趋势势不可挡。
声明:本文系药方舟转载内容,版权归原作者所有,转载目的在于传递更多信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除内容!