
2022-12-26 14:33:14来源:药智网浏览量:643
导读:THR-β激动剂有望首次登顶NASH“珠峰”!
我国脂肪肝患者约1.5亿,且在不断增加,NASH(非酒精性脂肪性肝炎)是脂肪肝中比较严重的类型。
据悉,有1.1亿轻度脂肪肝患者,可以通过饮食及锻炼好转,但是上千万中度重度NASH患者不能通过该方法恢复。且NASH需要终生用药,市场规模大。
然而,面对如此庞大的患病人群,人类却无计可施。
40年来,药企在NASH新药领域的研究几乎全军覆没,NASH的复杂性是这个时代最困难的医学挑战之一。
好在,经过全球制药企业的不断努力,40年研发“坟场”终见曙光。
THR-β激动剂有望
首次登顶NASH“珠峰”
近日,位于美国宾夕法尼亚州的Madrigal Pharmaceuticals宣布,瑞美替罗(resmetirom)达到了3期临床MAESTRO-NASH活检试验的主要终点和关键次要终点。
受此消息影响,Madrigal股价暴涨268%,市值超过40亿美元,足以证明市场对NASH药物的渴望。
据悉,MAESTRO-NASH试验在经活检证实的非酒精性脂肪性肝炎(NASH)患者中评估了80毫克和100毫克剂量的甲状腺激素受体激动剂瑞美替罗与安慰剂的对比。NASH是脂肪肝疾病的一种晚期形式。在两种剂量水平上,与安慰剂组的个体相比,resmetirom治疗的患者在后期试验中表现出显着更高水平的NASH消退和肝纤维化改善(该研究的共同主要终点)。两种剂量的效果都轻松优于安慰剂。值得注意的是,该药物在两种剂量下都显得安全且可耐受。
此外,口服药物治疗还显着改善了LDL-C胆固醇水平(“坏胆固醇”),这是该研究的一个关键次要终点。
Madrigal的管理层在新闻稿中指出,在研究参与者中,resmetirom在两种剂量水平下都是安全且耐受性良好的。Madrigal的高层打算2023年上半年,向FDA申请resmetirom的加速批准,作为治疗非肝硬化NASH伴肝纤维化的药物。
在服用resmetirom一年后,接受最高剂量治疗的患者中有30%在八分制量表上的症状至少改善了两分。同时,他们的纤维化没有恶化。
另一项指标着眼于肝纤维化缓解,它分五个阶段进行测量。结果26%的患者表现出至少一个阶段的纤维化改善,并且他们的症状没有恶化。
总体而言,56%的患者达到了临床试验研究的目标之一。
2023年,该药有望成为美国市场上第一个FDA批准的NASH药物。
THR-β选择性激动剂研发难点
安全性一直是NASH药物开发的痛点。在众多治疗NASH的药物靶点中,THR-β选择性激动剂终于取得成功。
先来看一下这个靶点的背景。
众所周知,甲状腺激素(THs)对许多生理过程产生显着影响,例如生长、发育和新陈代谢。缺乏甲状腺激素会引发多种疾病。大多数TH效应由两种不同的甲状腺激素受体(THR)亚型介导,即THR-α和THR-β,已知THR-β亚型负责TH对肝脏的有益作用。
因此,在过去的二十年里,人们付出了很多努力来开发能够将对肝脏(降低甘油三酯和胆固醇)和中枢神经系统(减少突胶质细胞增生)的有益作用与对心脏、肌肉和骨头有害副作用有选择性的甲状腺激素类似物。
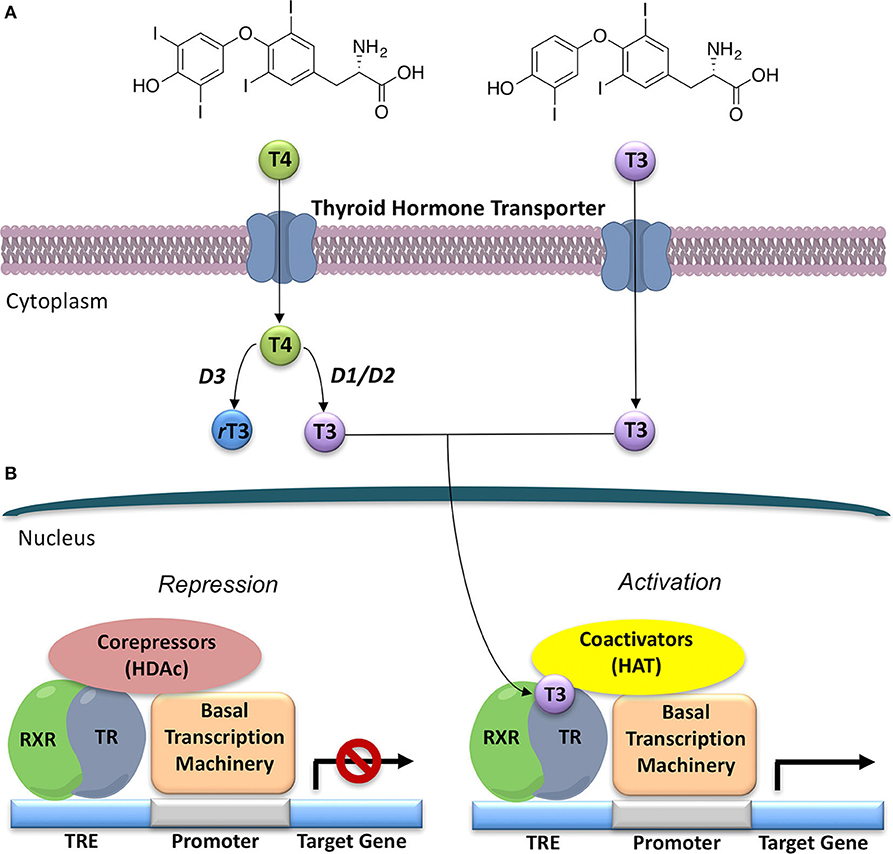
甲状腺激素(T3)在细胞核中产生和作用的模型
图片来源:参考资料3
甲状腺素(T4)是甲状腺产生的甲状腺激素(TH)的主要形式,一旦释放,就会通过脱碘酶1和2(D1和D2)转化为T3,即TH的主要形式。脱碘酶3(D3)将T4转化为无活性的rT3。(二)甲状腺激素受体(TR)作为调节多种基因的转录因子。Unliganded TR,通常作为与视黄酸X受体(RXR)的异二聚体,与DNA上的甲状腺激素反应元件(TRE)结合,然后募集共阻遏物及其相关的组蛋白乙酰转移酶(HAT)。辅因子结合的这种改变导致聚合酶III的募集和基因转录的开始。
Sobetirome(GC-1)2和随后的Eprotirome(KB2115)5是THR-β选择性激动剂的早期例子,Sobetirome与甲状腺素的结构不同,因为它没有卤素、联芳基醚氧和氨基酸侧链。尽管这两种拟甲状腺素都显示出令人鼓舞的抗高胆固醇血症、非酒精性脂肪性肝炎(NASH)和刺激肝细胞增殖的作用,但它们分别在1期和2-3期临床试验后宣告失败。
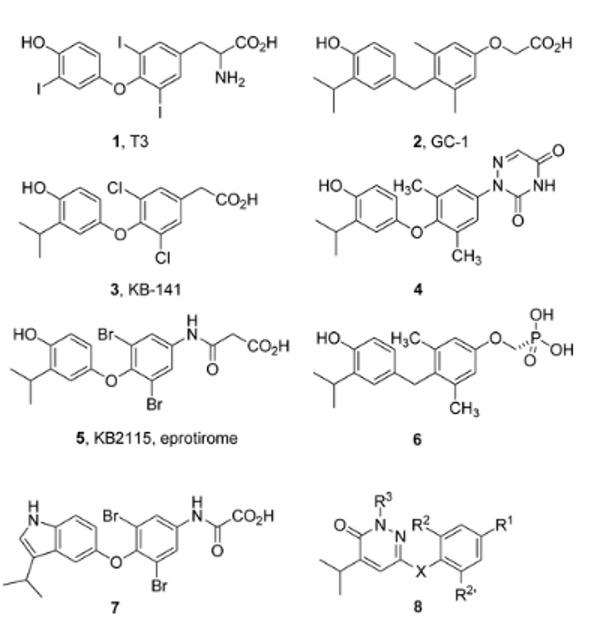
几款THR激动剂小分子的结构
图片来源:参考资料2
近年来,分子和结构生物学的进步,促进了新的选择性甲状腺激素模拟物的设计,这些模拟物表现出THR亚型选择性结合和/或肝脏和组织选择性摄取,Resmetirom(MGL-3196)和Hep-Direct前体药物VK2809(MB07811)代表了两种最有前途药物。

Resmetirom和Eprotirome的结构
图片来源:参考资料3
来看一下Madrigal公司在早期研发中,如何通过药物化学优化提高安全性:
在核激素受体激动剂领域,很难预测配体结构的细微改变如何影响其生物学特征。为了鉴定更具THR-β选择性且可能更安全的化合物,基于药物代谢和安全性的考量,Madrigal公司把精力主要集中于不含富电子的苯酚环的T3类似物。
在早期临床试验中,化合物5的酚环与亚硝酸盐在胃强酸性环境下通过自由基硝化形成的毒性化合物在血浆中能被检测到,从而造成药物安全性的问题。而拜耳公司一系列基于吲哚结构的THR激动剂,如化合物7,证明了T3的酚环可以被杂环取代。在Madrigal公司研究的几种缺电子杂环修饰中,由化合物8为代表的哒嗪酮类似物被证明是最有希望的,这种新型杂环为化合物提供了改进的THR-β选择性,构成了resmetirom这款药的结构基础。
根据Madrigal发布的Resmetirom安全性数据(图5)所示在80mg和100mg剂量下都是安全且耐受性良好的,严重不良事件的频率在治疗组中相似因不良事件而中止研究的比率很低。这些数据与之前的临床数据一致,与安慰剂组相比,服药组最常见不良反应是治疗开始时轻度和短暂性腹泻以及轻度恶心。
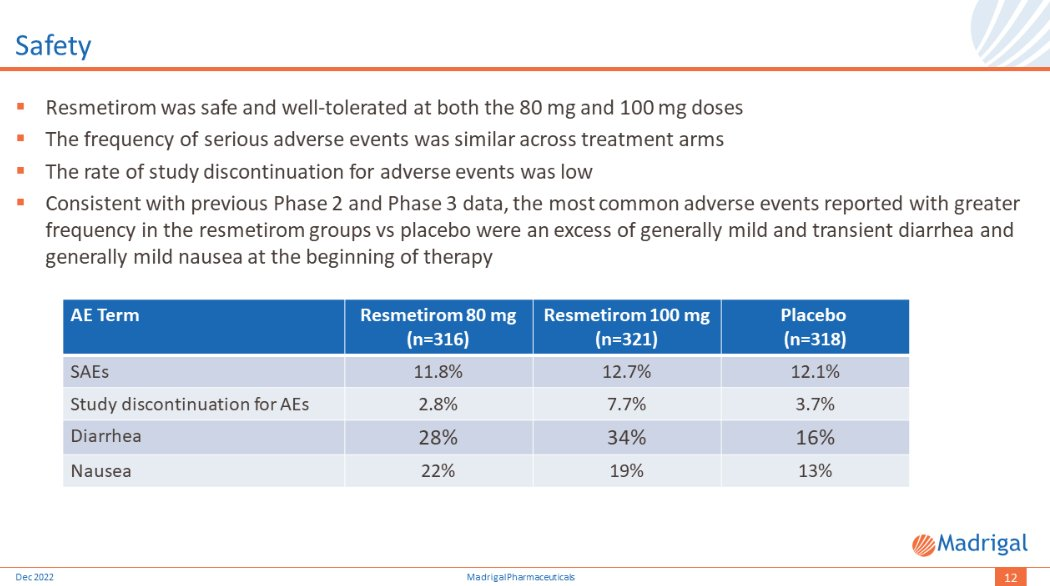
Resmetirom安全性数据
图片来源:公司官网
小结
NASH是生物制药中最热门的研究领域之一,正在进行300多项临床试验。此前,Intercept Pharma公司看起来很有可能赢得将NASH药物推向市场的竞赛,但在FDA于2020年拒绝其奥贝胆酸(OCA)的上市申请并被迫撤回其申请后,希望破灭。
而凭借THR-β选择性激动剂3期临床的成功,行业专家判断Madrigal公司可能已经成为各大药企2023年最想并购的候选者,若收购成功,可能获得高达90亿美元的收入。
未来,随着NASH药物研发进展,也会有更多脂肪肝患者收益。道阻且长,行则将至;行而不辍,未来可期。
参考资料:
1.Madrigal公司新闻稿宣布三期临床成功
https://ir.madrigalpharma.com/news-releases/news-release-details/madrigal-announces-positive-topline-results-pivotal-phase-3
2.Resmetirom药物化学论文
https://pubs.acs.org/doi/10.1021/jm4019299#
3.THR-β药物开发综述
https://www.frontiersin.org/articles/10.3389/fmed.2020.00331/full
4.谢博士NASH评论文章
https://ibook.antpedia.com/x/523197.html
5.万字闲谈NASH新药研发
https://mp.weixin.qq.com/s/4Zuutih8xsJUHONIlVzTfA
声明:本文系药方舟转载内容,版权归原作者所有,转载目的在于传递更多信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除内容