2023-10-25 09:53:55来源:CDE浏览量:635
为丰富完善中医药理论、人用经验和临床试验相结合的中药注册审评证据体系,指导申请人在“三结合”中药审评证据体系下研发用于小儿便秘的中药新药,药审中心起草了《小儿便秘中药新药临床研发技术指导原则(征求意见稿)》,经中心内部讨论并组织专家研讨,已形成征求意见稿。现在中心网站予以公示,以广泛听取各界意见和建议。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个月。
您的反馈意见请发到以下联系人的邮箱:
联系人:杨娜,yangn@cde.org.cn
褚新颖,chuxy@cde.org.cn
王熙熙,wangxx@cde.org.cn
感谢您的参与和大力支持!
药品审评中心
2023年10月24日
附件1















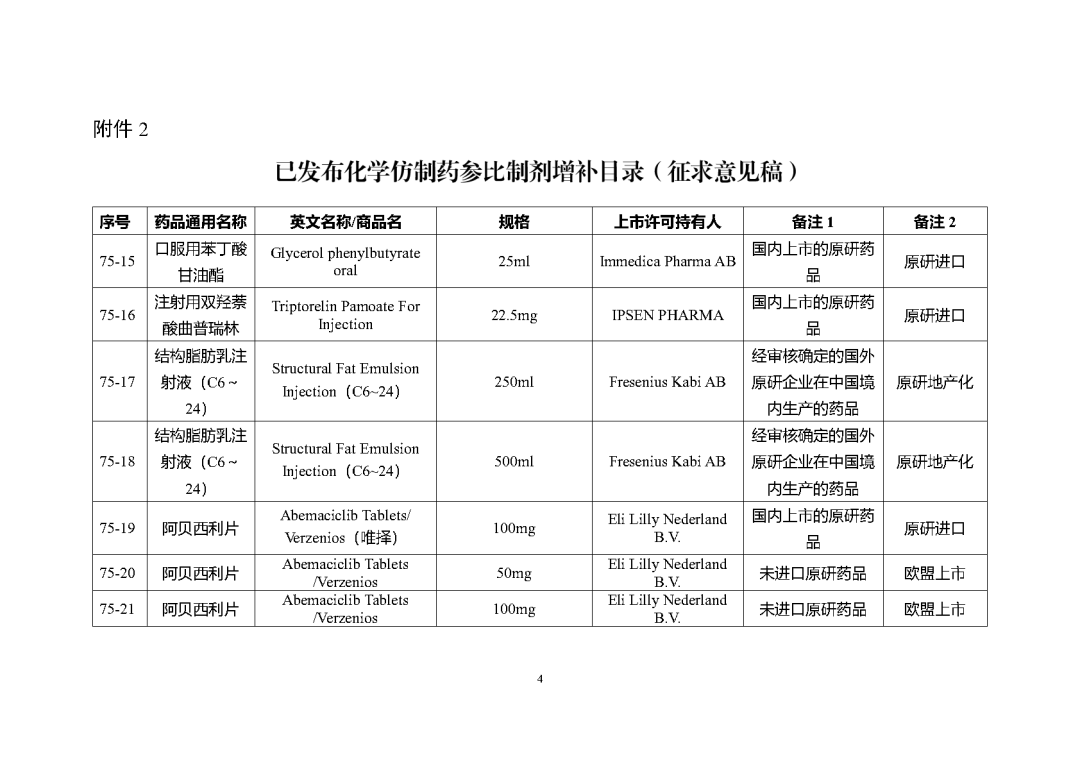
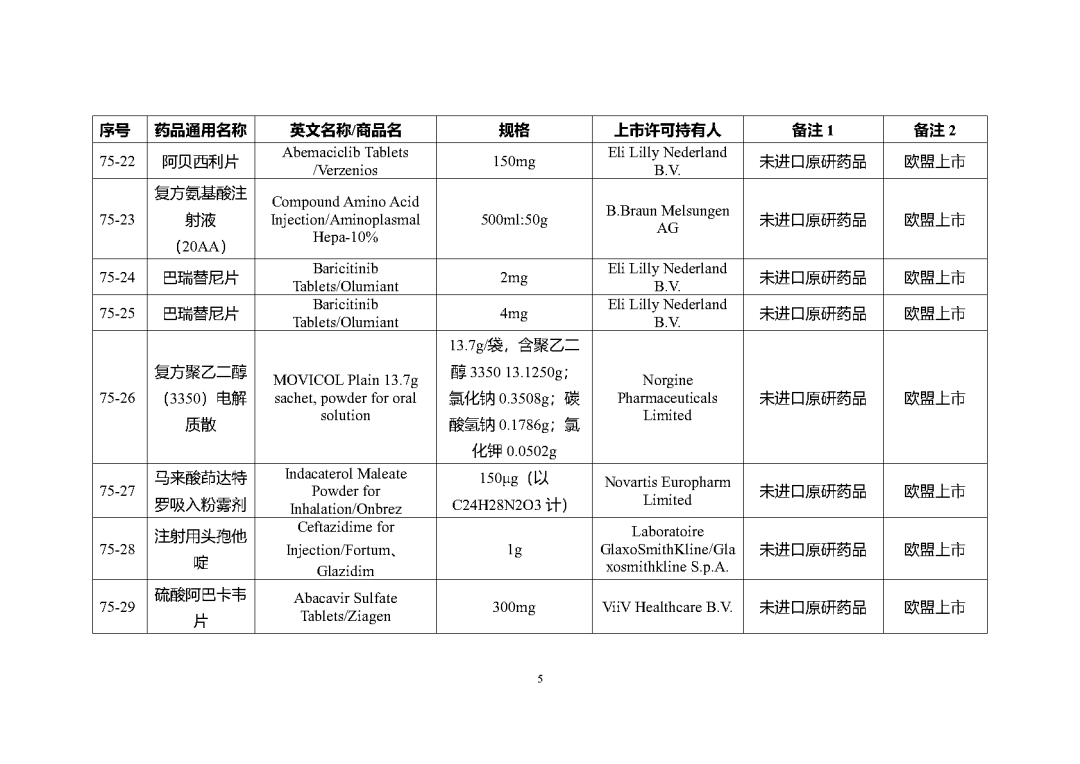
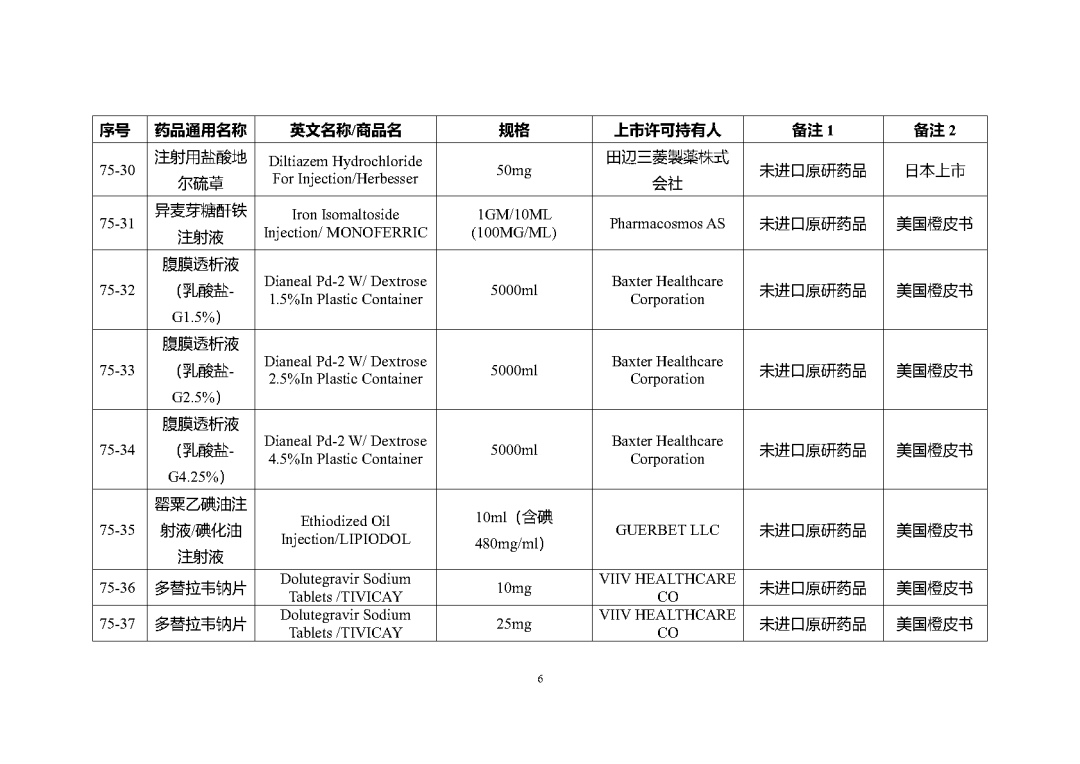
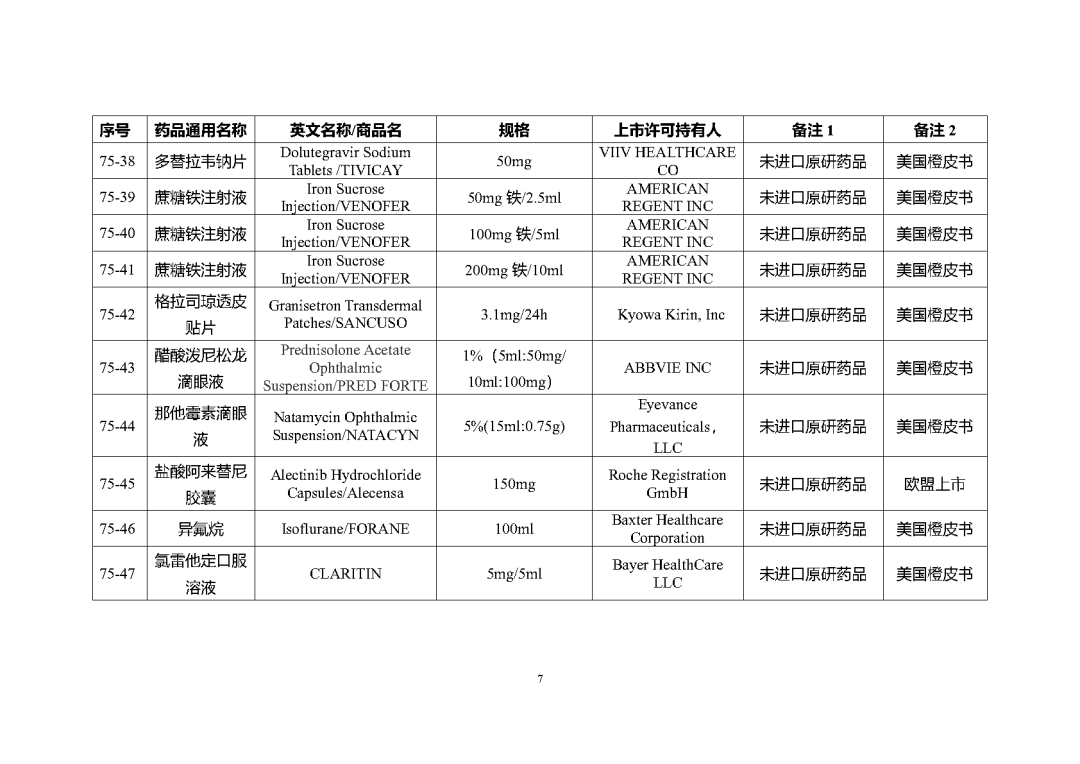
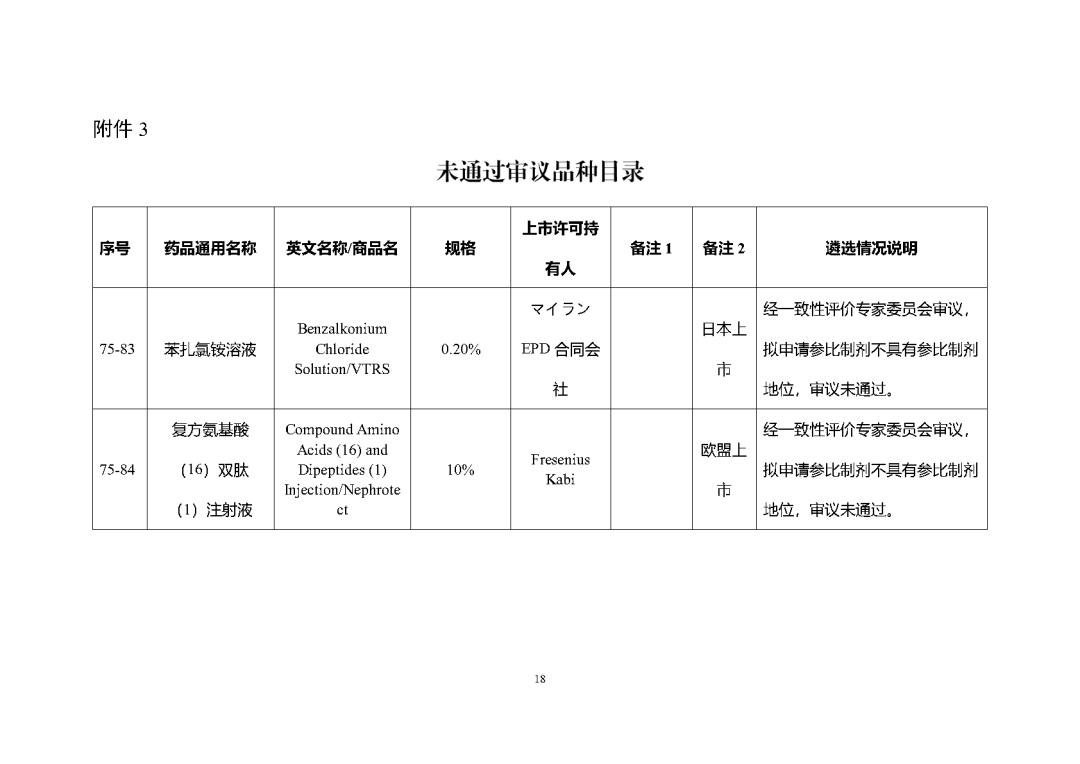
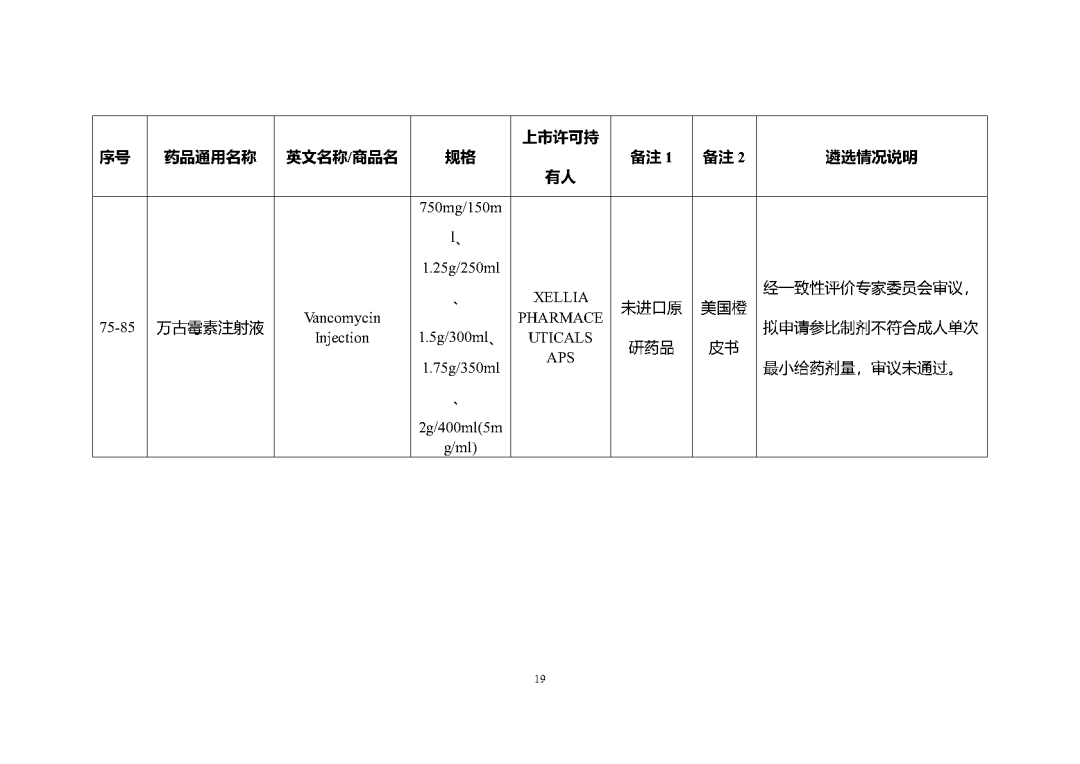
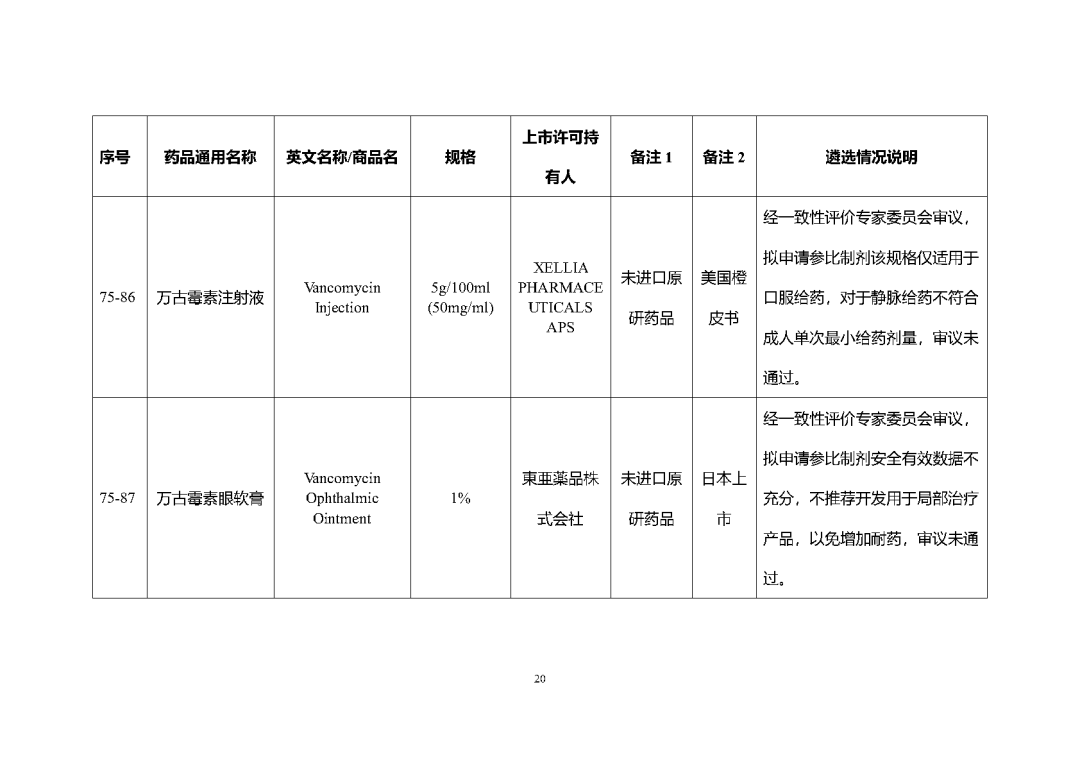
附件2






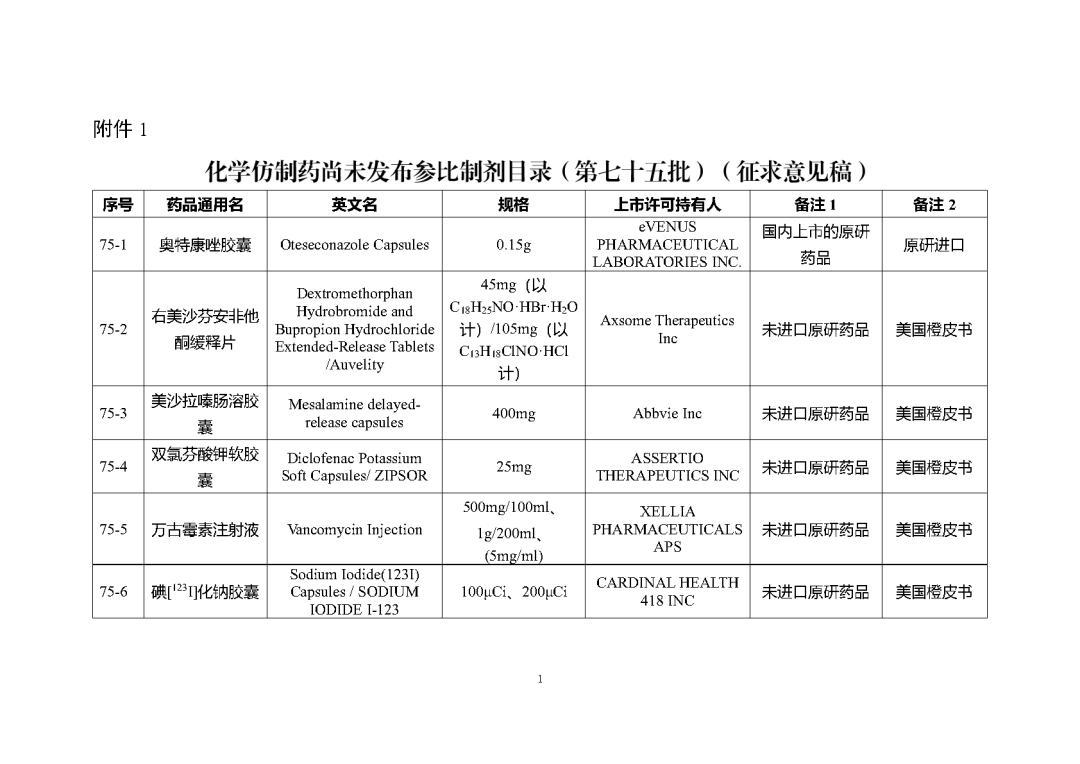
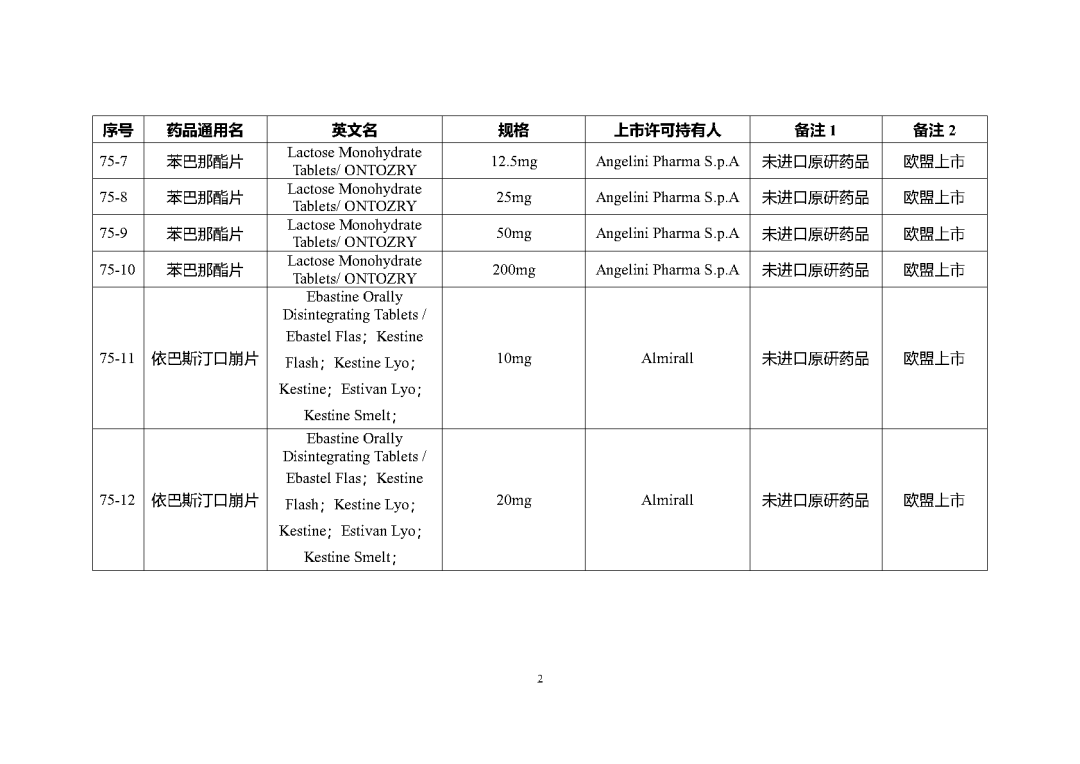
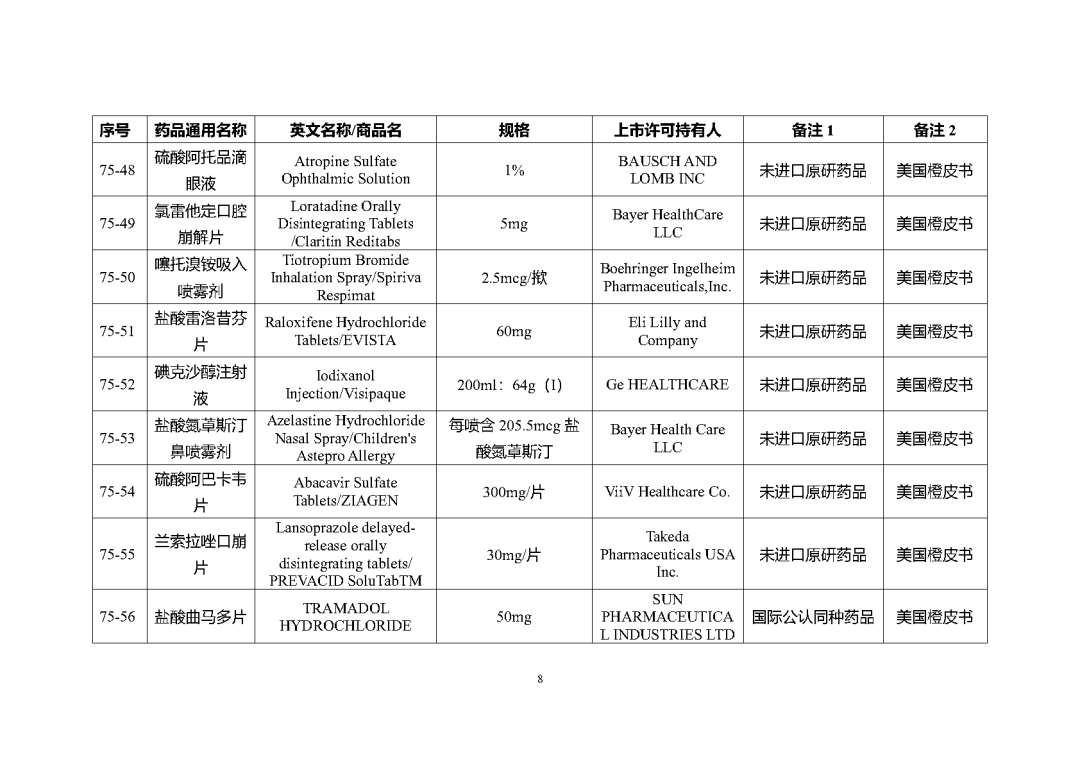
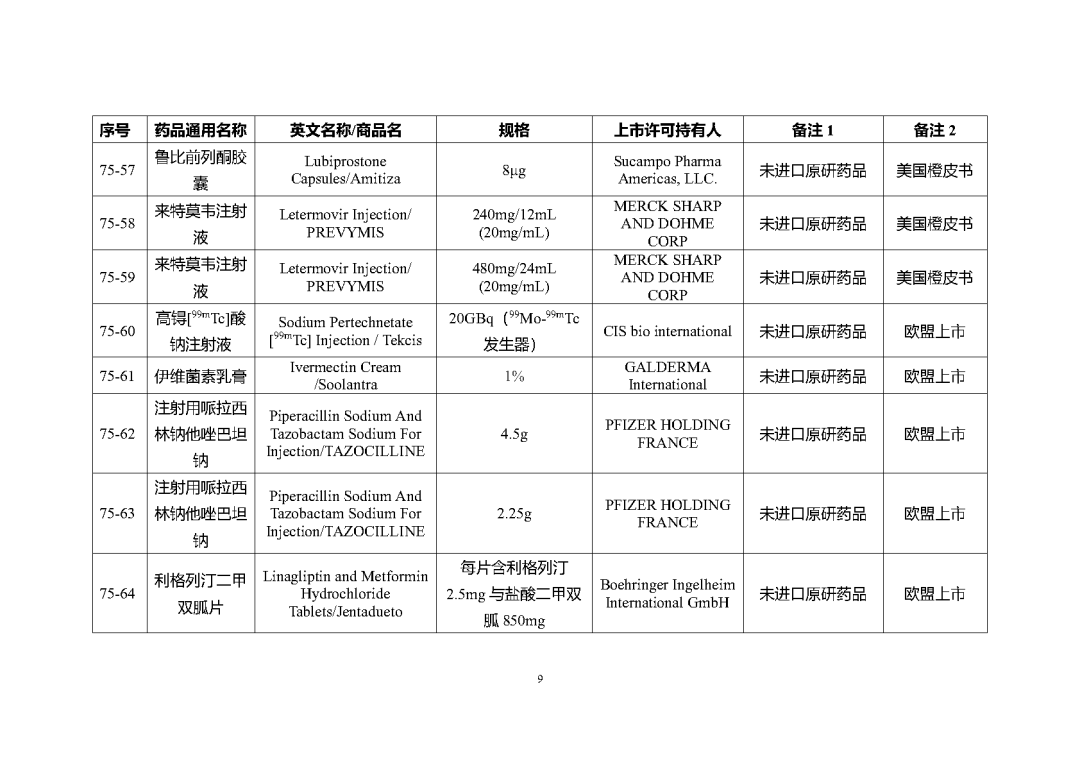
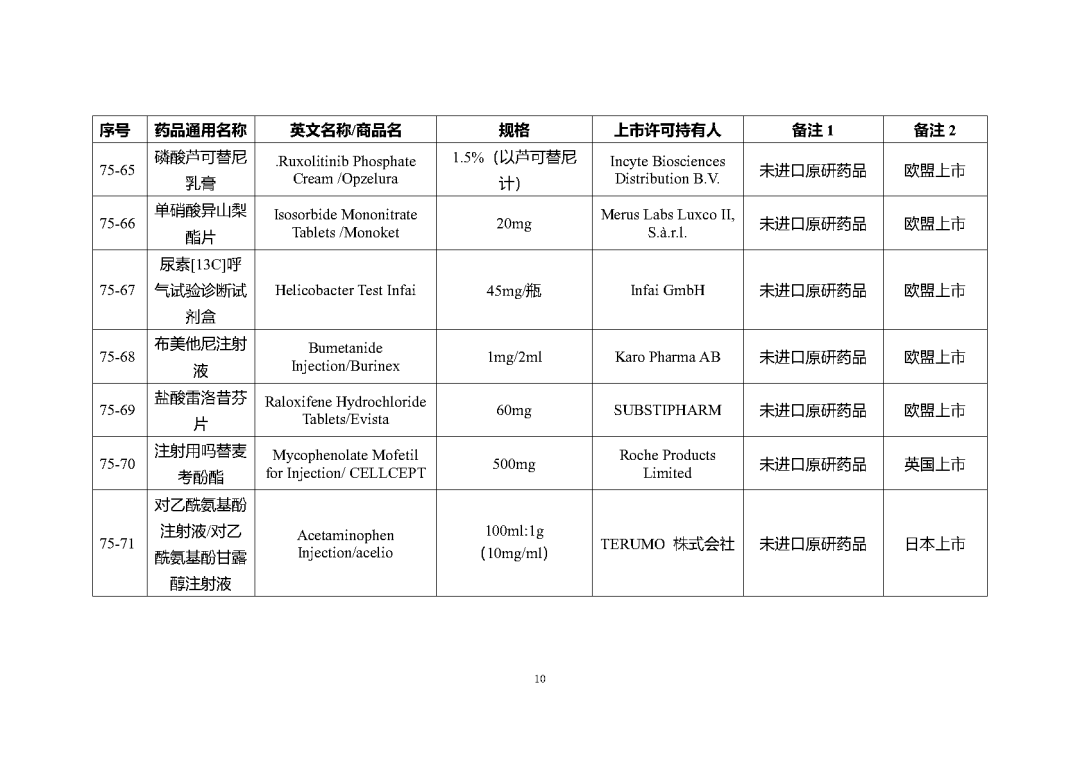
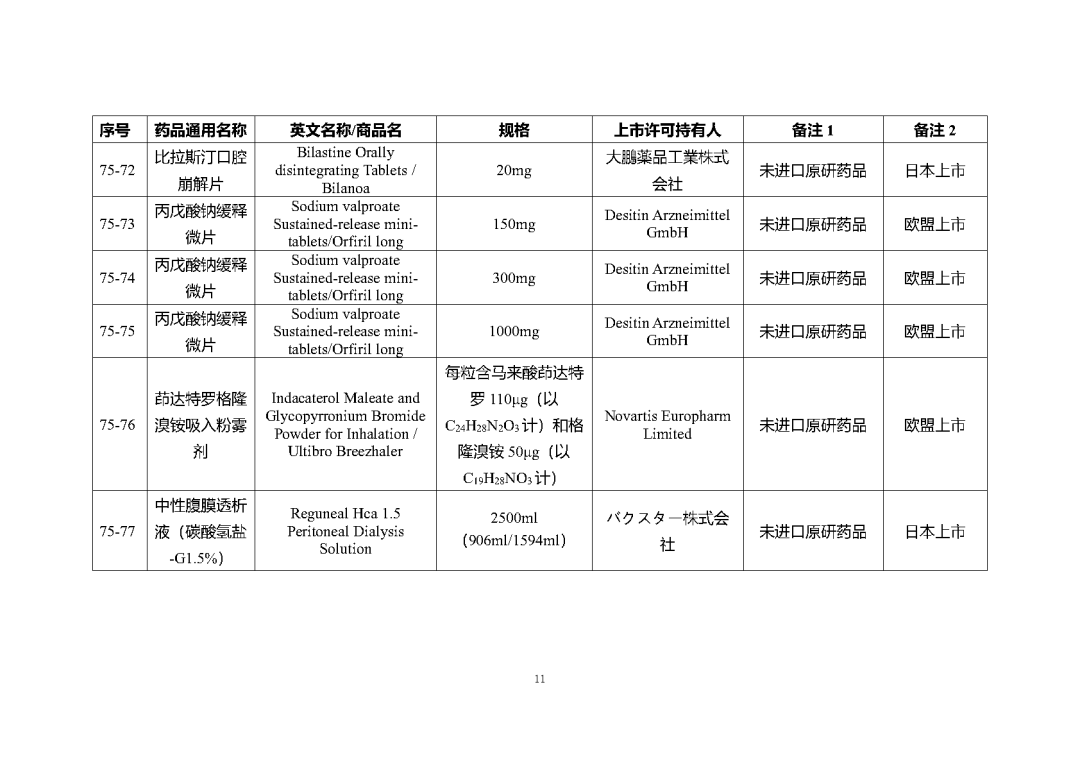
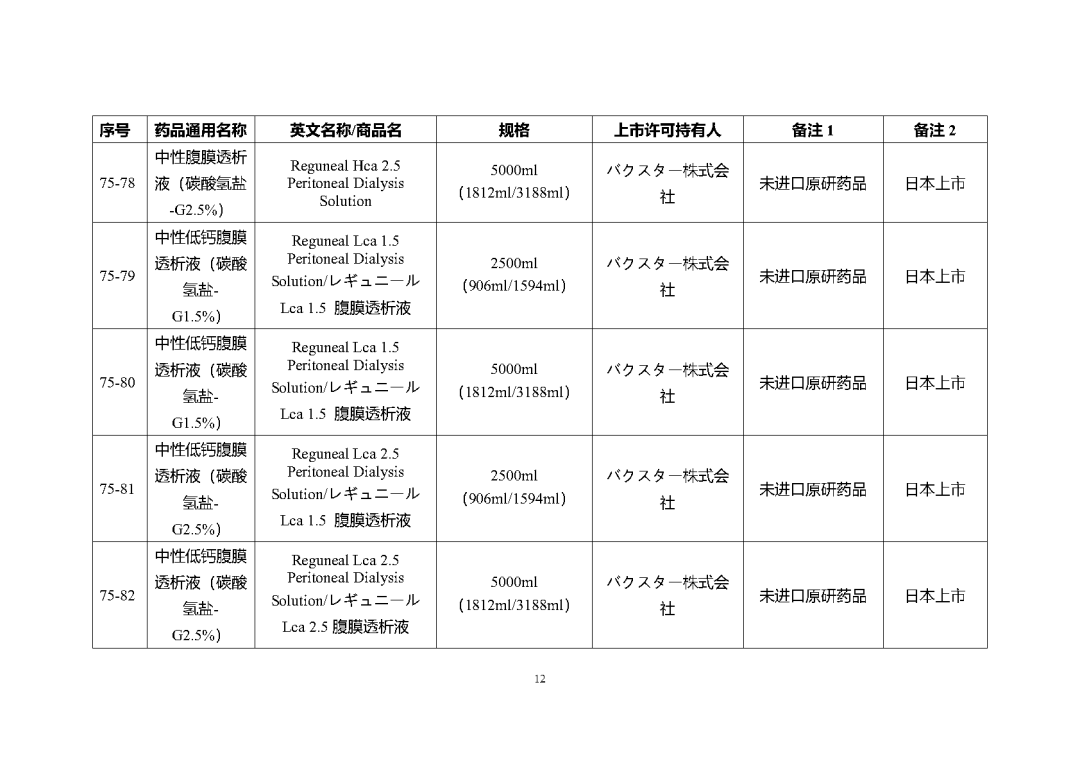
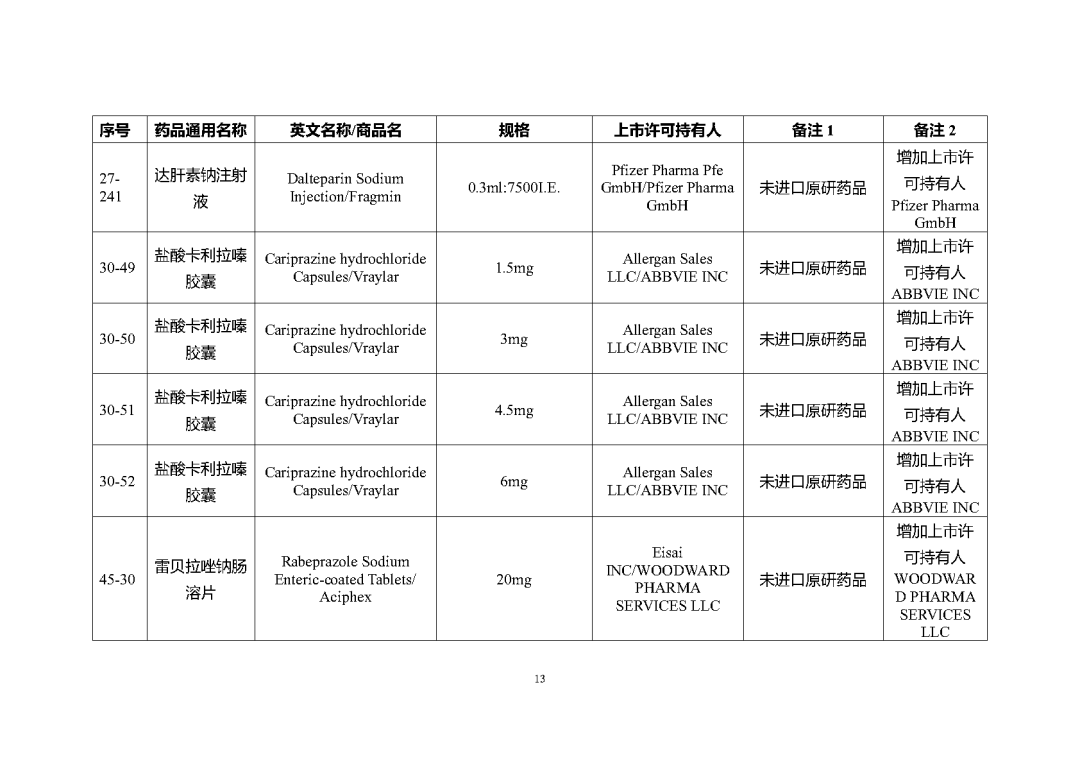
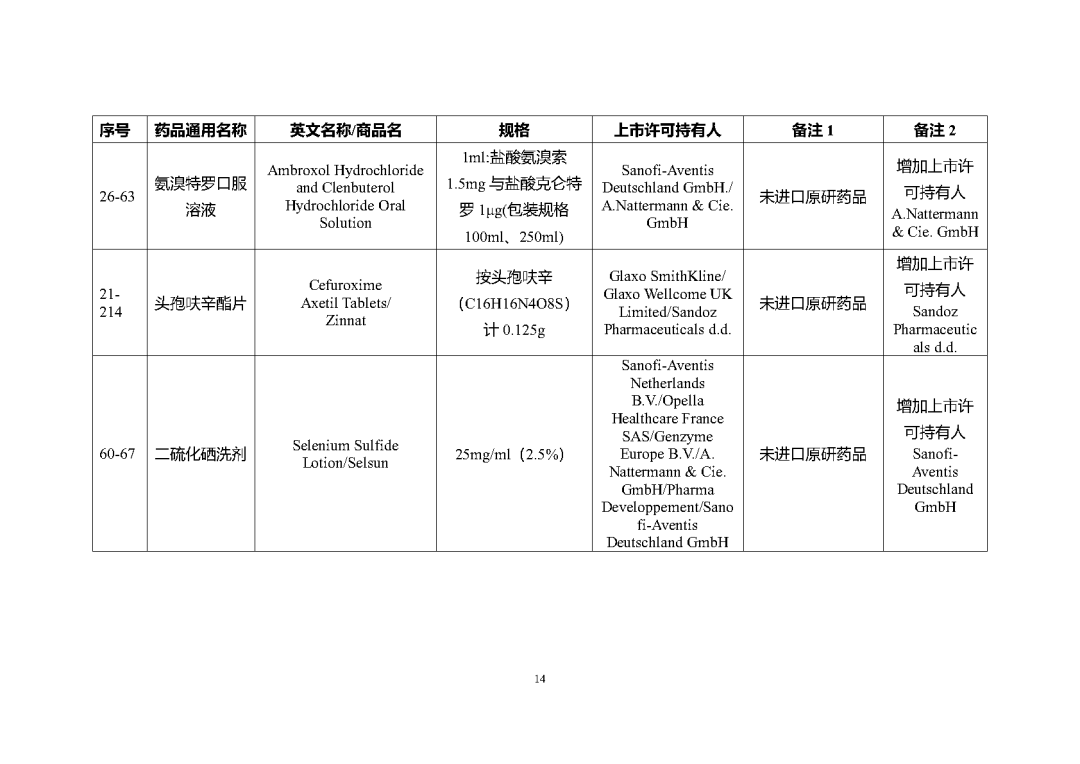
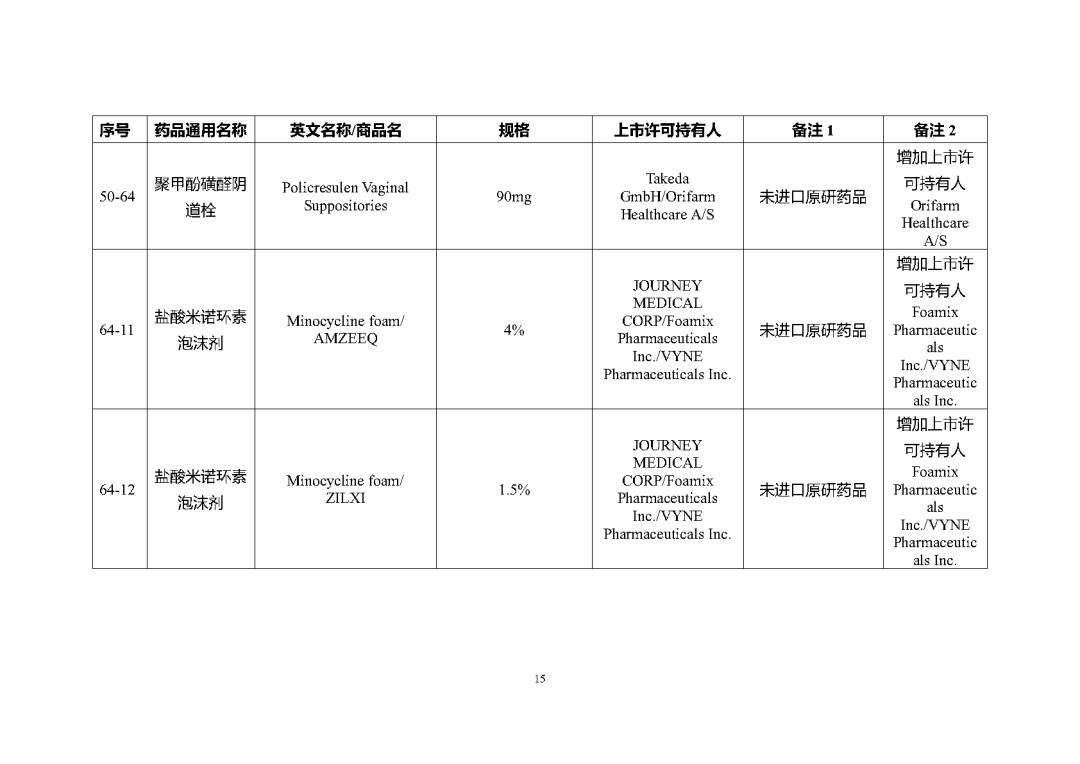
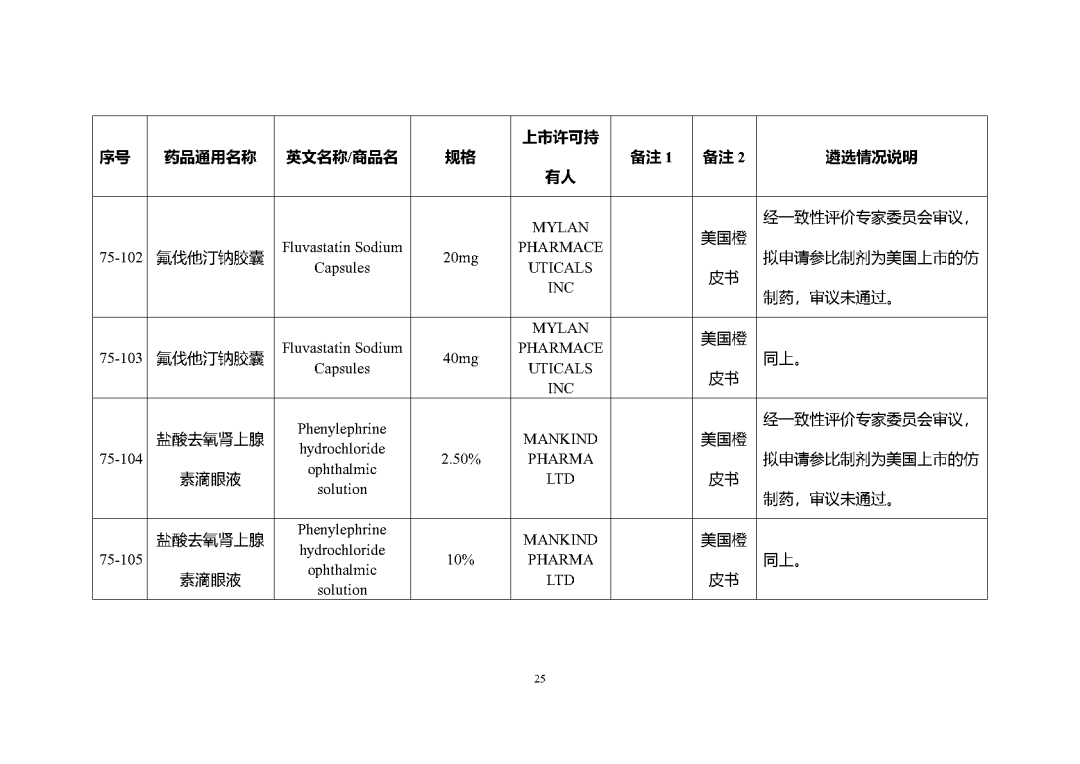
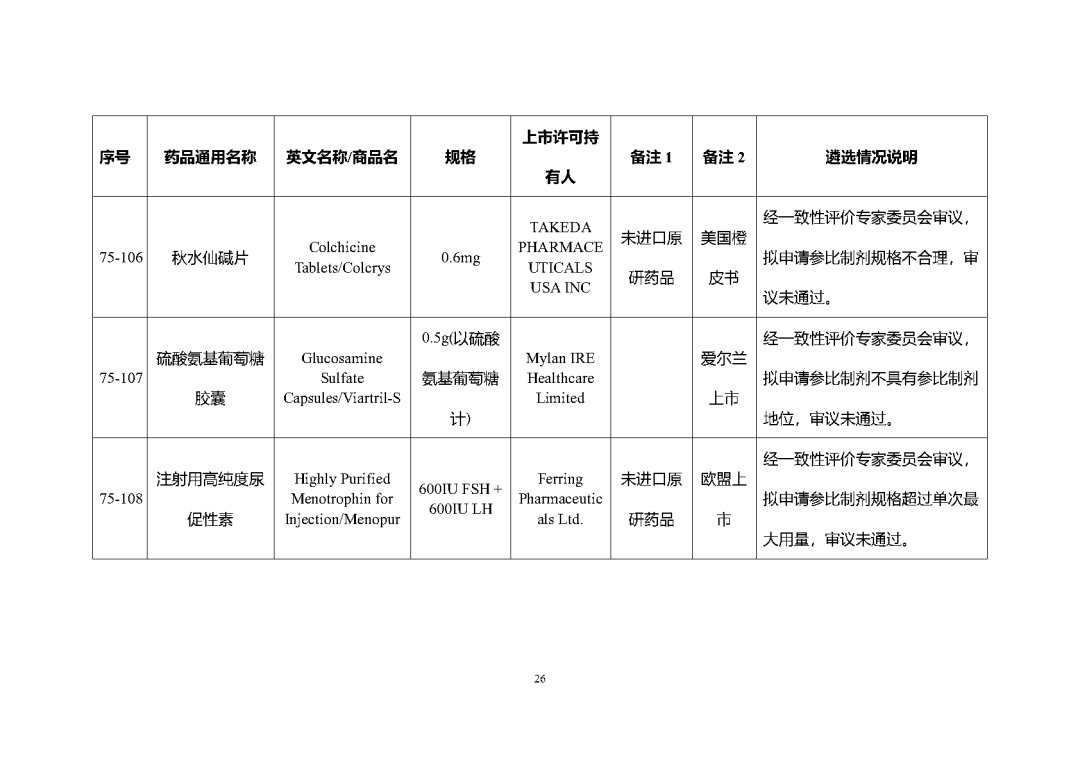
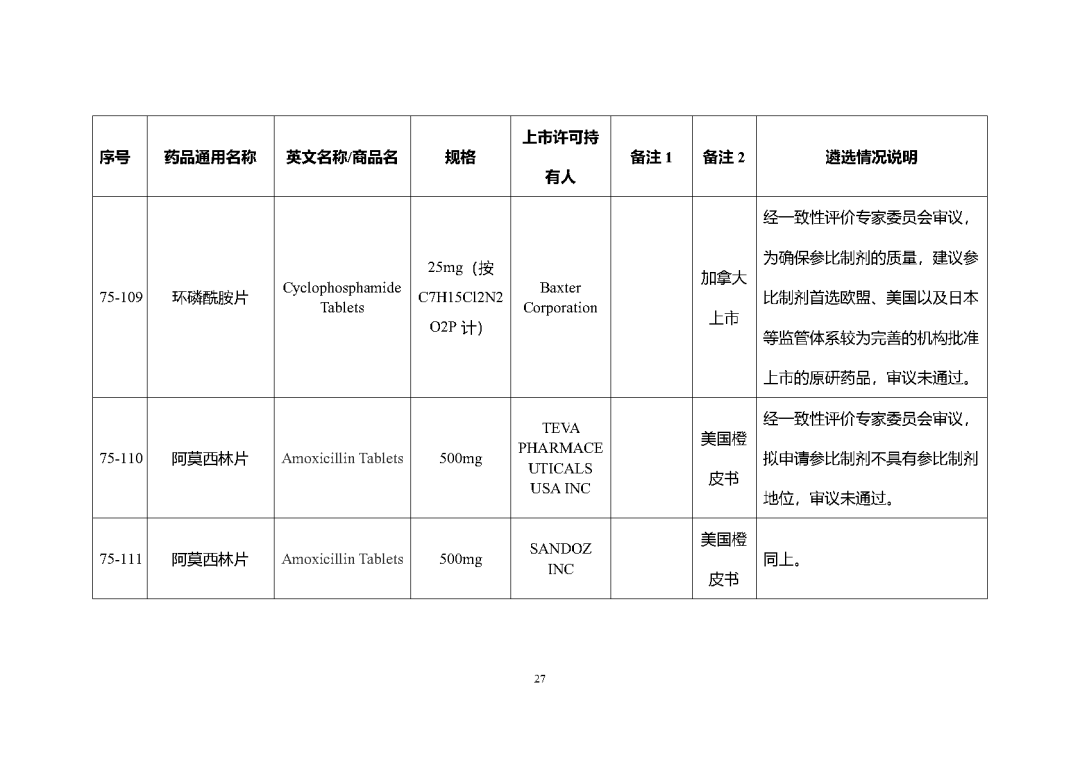
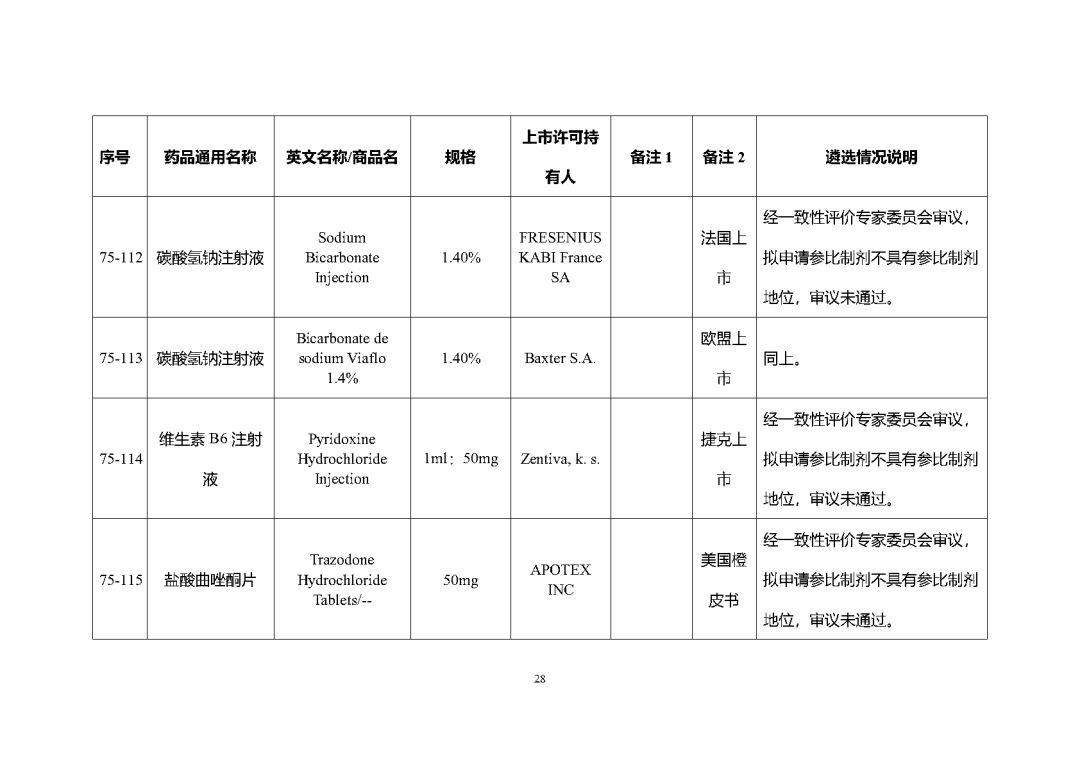
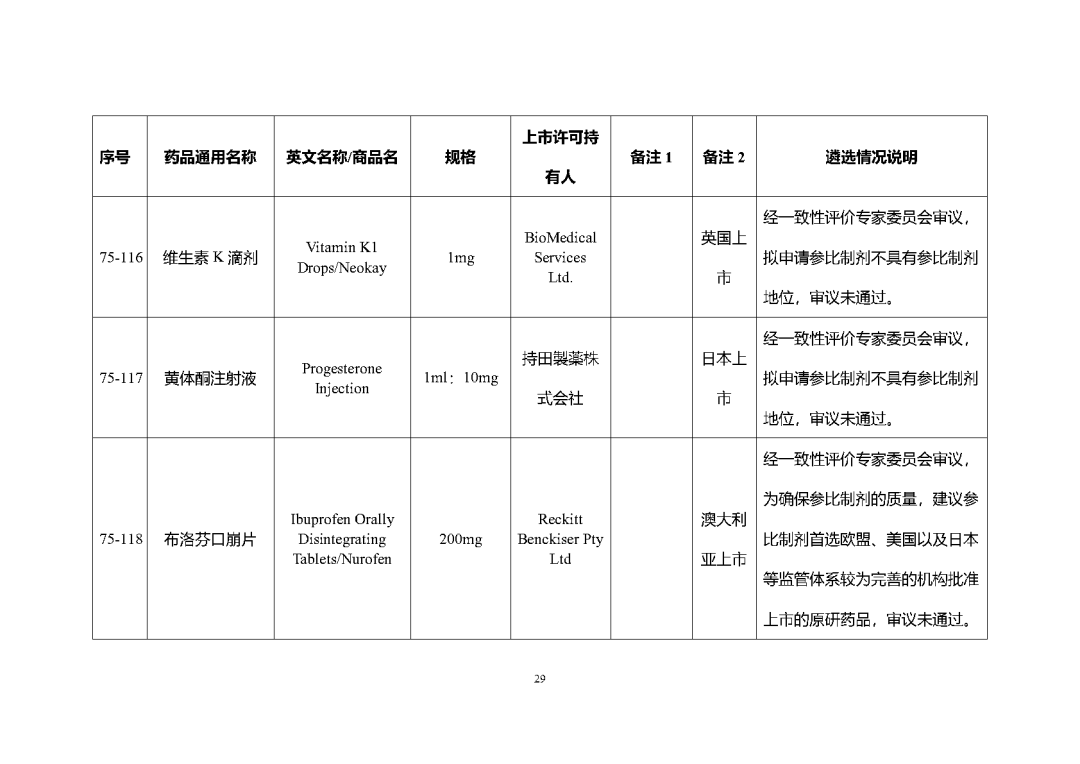
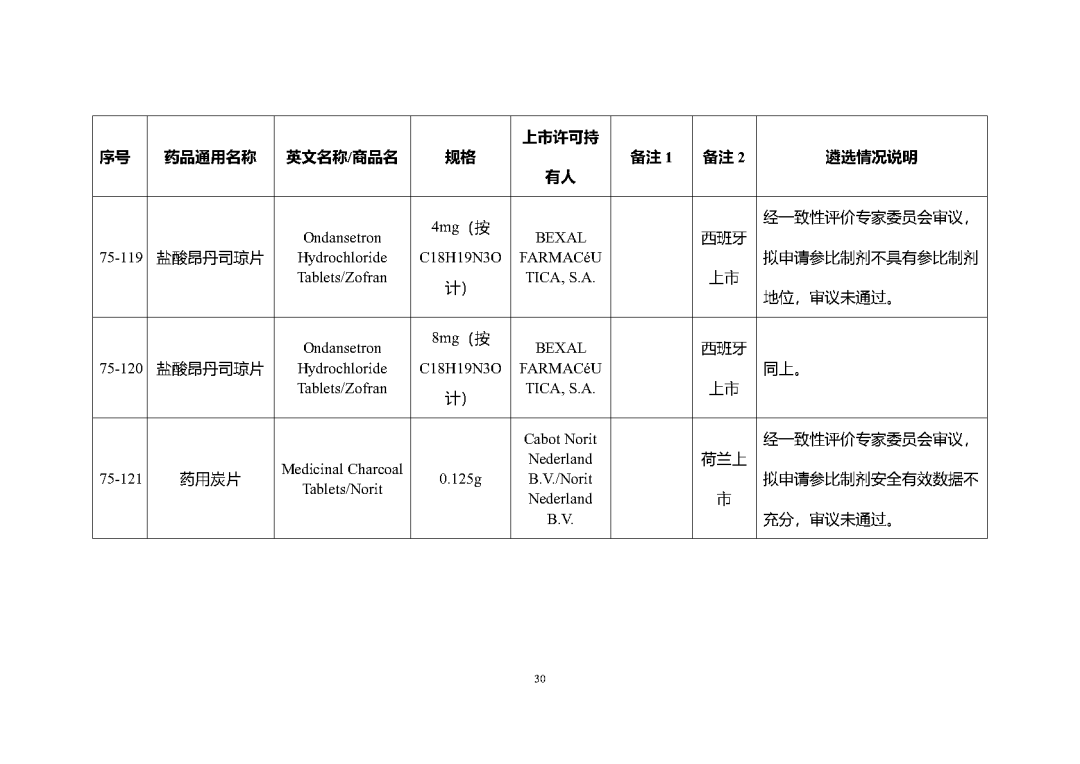
根据国家局2019年3月28日发布的《关于发布化学仿制药参比制剂遴选与确定程序的公告》(2019年第25号),我中心组织遴选了第七十五批参比制剂(见附件),现予以公示征求意见。
公示期间,请通过参比制剂遴选申请平台下“参比制剂存疑品种申请”模块向药审中心进行反馈,为更好服务申请人,反馈意见请提供充分依据和论证材料,反馈材料应加盖单位公章,并提供真实姓名和联系方式。
公示期限:2023年10月24日~2023年11月6日(10个工作日)。
国家药品监督管理局药品审评中心
2023年10月24日
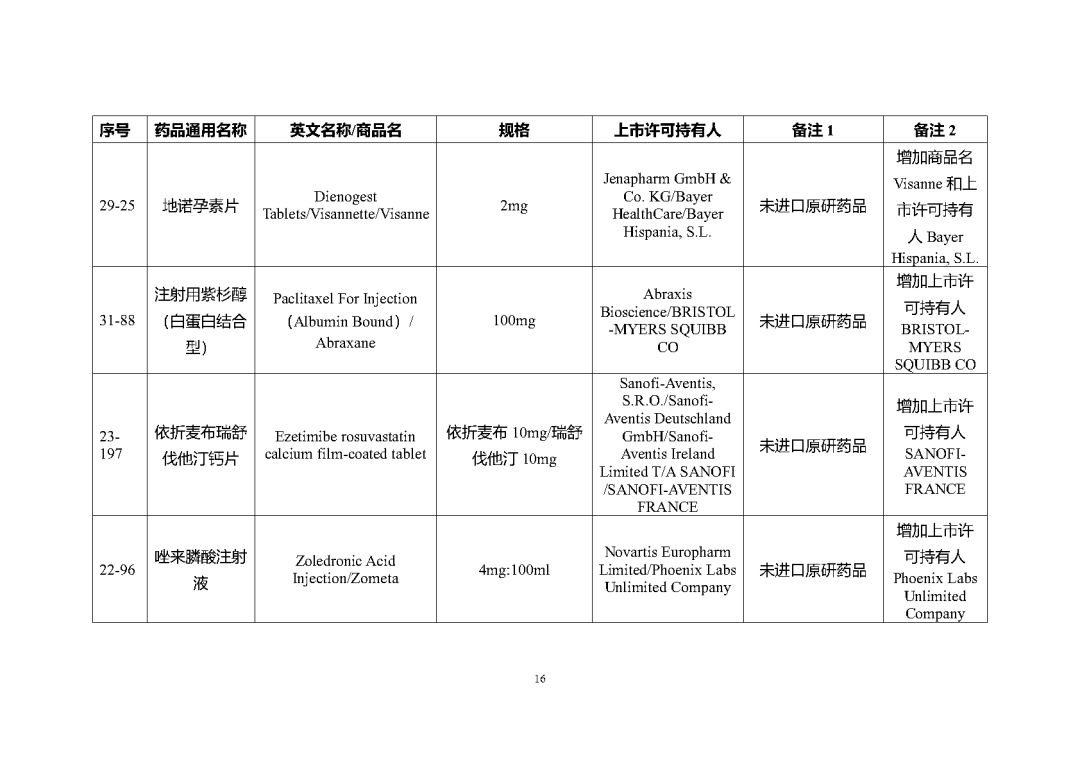
附件1


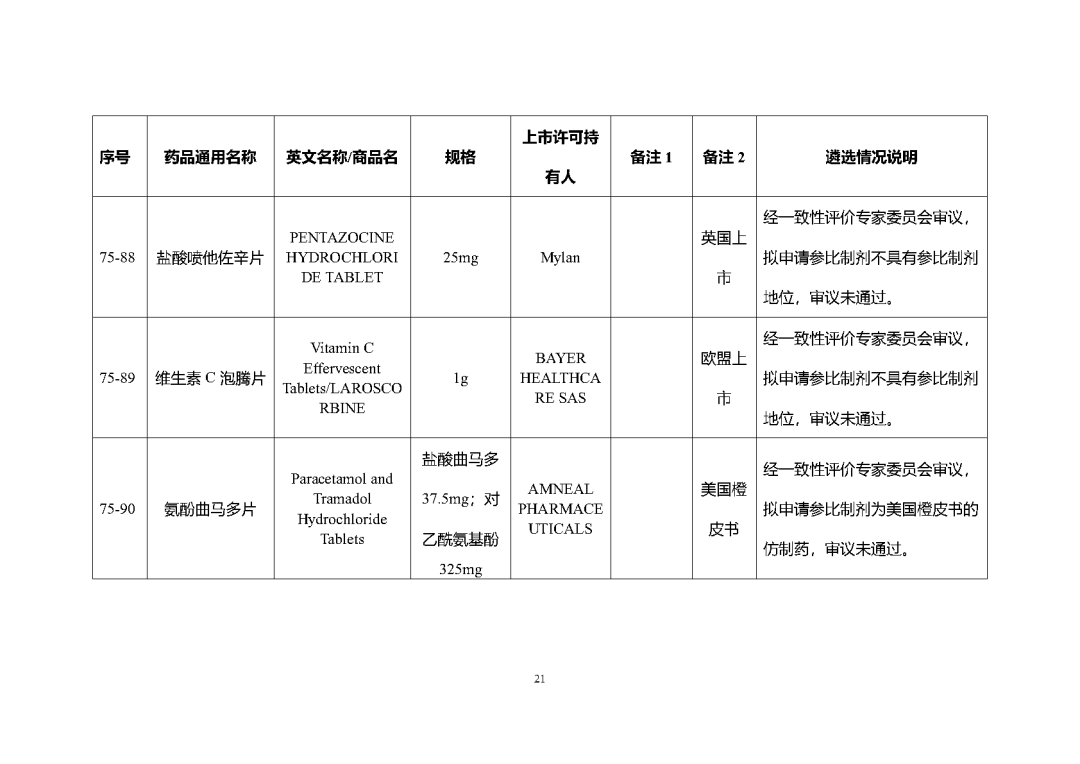
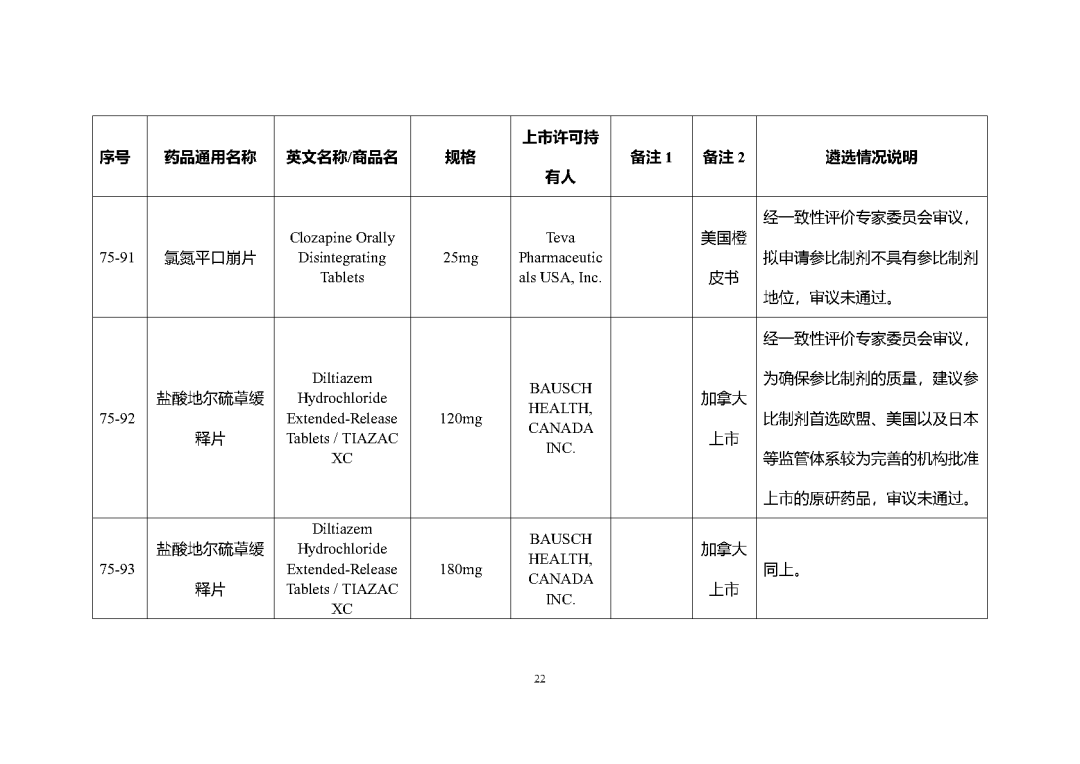
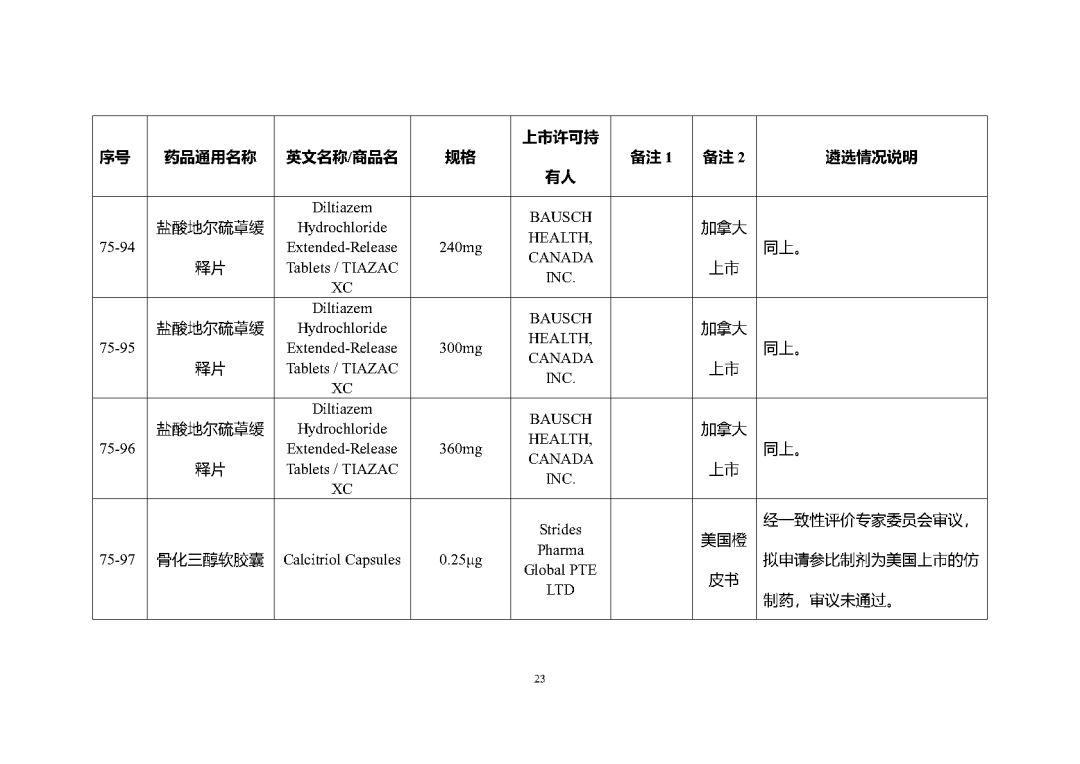
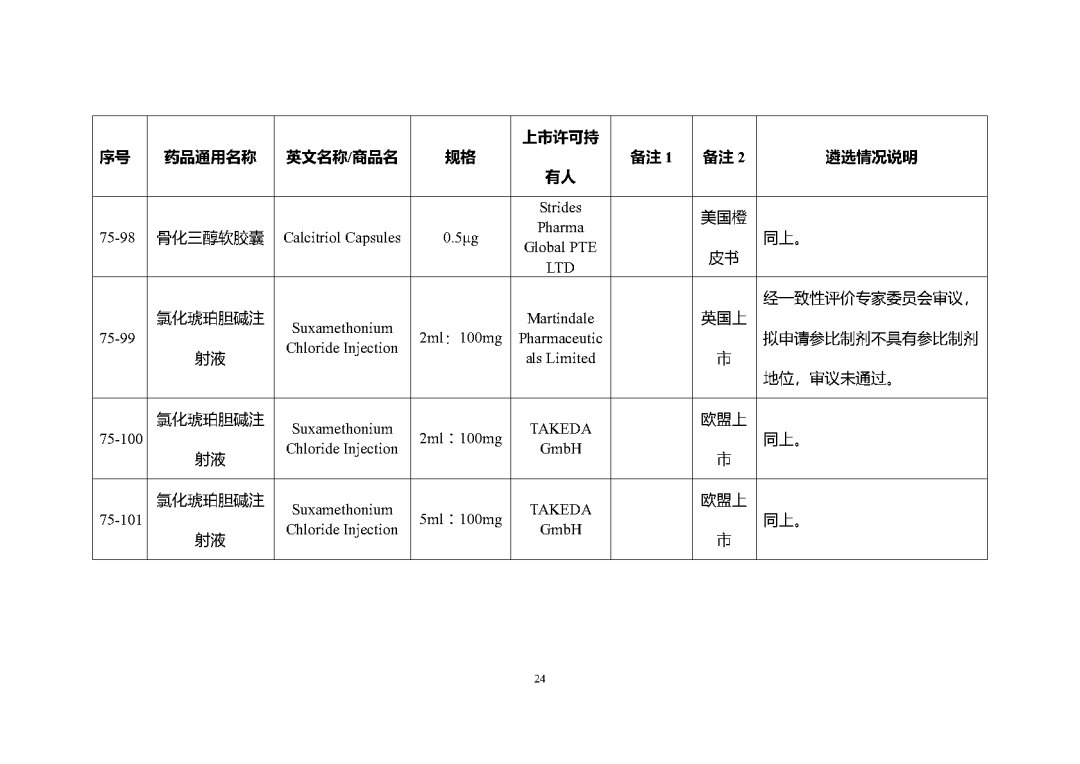
附件2