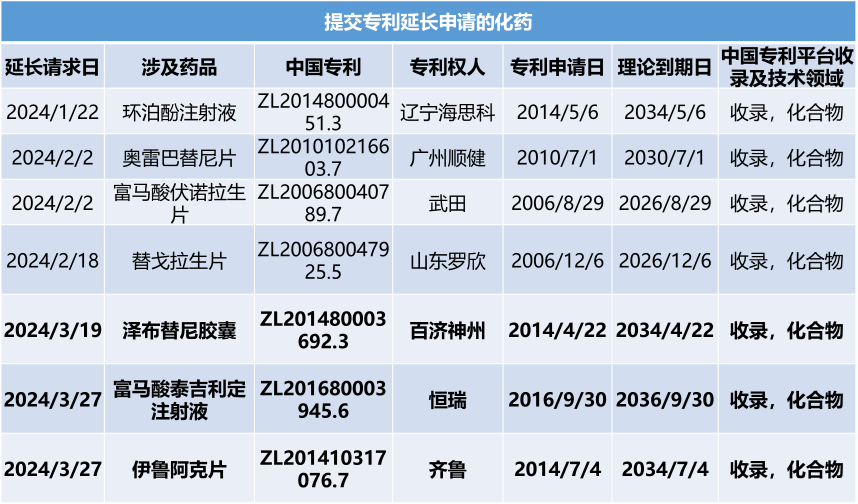
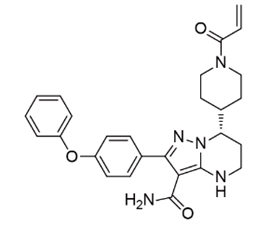
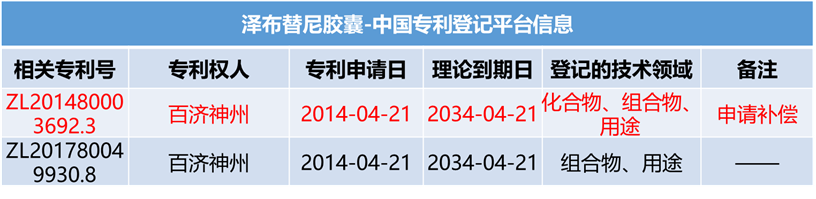
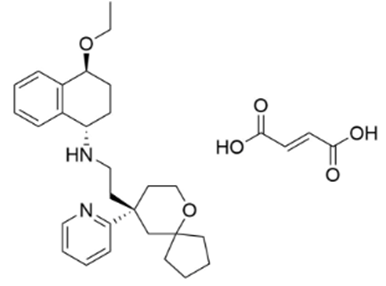
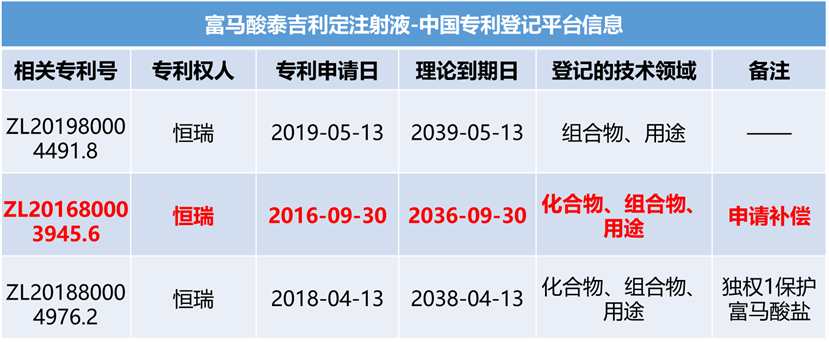
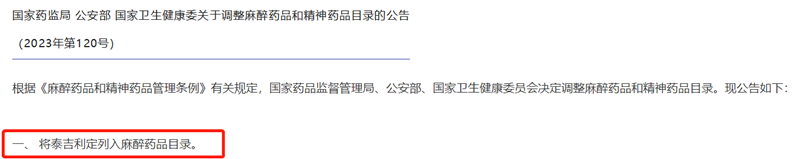
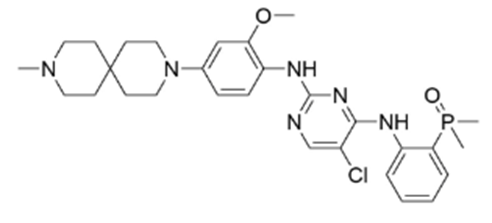
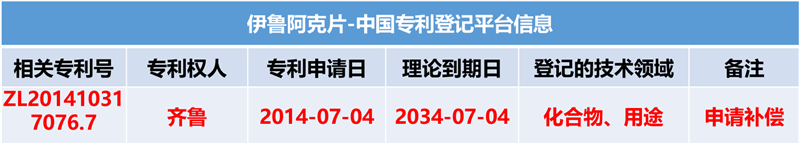
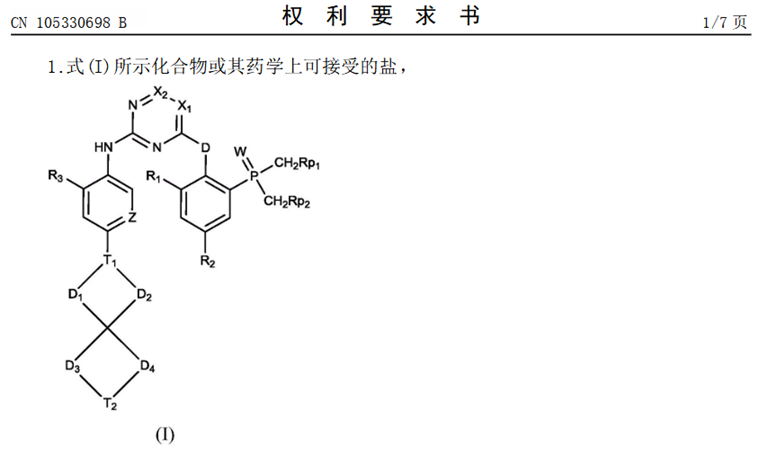
制药行业,药品专利的作用不必多说。对于制药人,专利期限的具体到期日是非常值得关注的内容。本文盘点了2024年第一季度已明确提出“专利权期限及药品专利期限补偿申请书”的相关企业及药品情况,以供行业参考。本文作为下篇,主要简介泽布替尼胶囊、富马酸泰吉利定注射液、伊鲁阿克片情况,具体从基本信息、专利信息及注册、竞品情况进行呈现。值得注意的是,以上三个品种均是国产1类新药。值得说明的是,截止目前,尚无公开途径检索到补偿审查决定,相关企业需要密切关注及跟踪。图:提交专利补偿申请的化药(自行整理,图形自制),信息来源:国家知识产权局、中国专利登记平台等泽布替尼是由百济神州研发的一种小分子BTK抑制剂。该药为中国化药一类。目前该药物最高研发阶段为批准上市,用于治疗滤泡性淋巴瘤、慢性淋巴细胞白血病、边缘带B细胞淋巴瘤、华氏巨球蛋白血症和套细胞淋巴瘤。泽布替尼胶囊在中国专利登记平台上登记2项专利信息,技术领域涉及化合物、组合物和用途。其中,ZL201480003692.3理论于2034年4月21日到期,并且原研针对该专利于2024年3月提交延长申请。图:泽布替尼中国专利登记平台收录情况,信息来源:中国专利登记平台经查看,专利ZL201480003692.3保护包含泽布替尼的通式化合物。图:信息来源:ZL201480003692.3(CN104884458B)专利泽布替尼在2019年11月14日首次在美国批准上市,而后分别进入中国及欧盟,批准进入中国时间是2020年6月2日,批准进入欧盟时间是2021年10月20日。泽布替尼在中国按照1类申报上市,CDE承办日是2018年8月29日,此时美国尚未批准。在竞品方面,截止2024年4月7日,中国尚无仿制企业提交上市申请情况。而在同靶点赛道上,泽布替尼还需要应对来自其他企业发起的专利狙击,比如引发业内关注的其中一项专利案件——2023年6月艾伯维旗下Pharmacyclics公司在美国特拉华州地区法院提起诉讼,指控泽布替尼侵权了其US11672803专利,而百济神州也在同年11月向美国专利审判和上诉委员会递交了PGR(美国专利无效的授权后审查程序),对艾伯维进行专利无效反击。而作为创新药企的百济神州,仅仅当被告是不够聪明的,2024年3月8日,百济神州在美国分别对山德士及MSN提起了专利侵权诉讼。富马酸泰吉利定是由恒瑞研发的一种小分子MOR1激动剂。该药为中国化药一类。目前该药物最高研发阶段为批准上市,用于治疗术后疼痛。富马酸泰吉利定在中国专利登记平台上登记3项专利信息,技术领域涉及化合物、组合物和用途。其中,ZL201680003945.6理论于2036年9月30日到期,并且原研针对该专利于2024年3月提交延长申请。图:富马酸泰吉利定中国专利登记平台收录情况,信息来源:中国专利登记平台经查看,ZL201680003945.6保护包含富马酸泰吉利定在内的通式化合物。图:信息来源:ZL201680003945.6(CN107001347B)专利富马酸泰吉利定首次于2024年1月30日在中国批准上市,该产品是中国首个自主研发的1类阿片类镇痛创新药。截止2024年4月7日,暂无仿制企业提交上市申请记录。从恒瑞已上市创新药来看,截止2024年4月公司已在国内获批上市1类创新药达16款。从恒瑞镇痛麻醉领域来看,2019年12月公司创新药注射用甲苯磺酸瑞马唑仑上市,此次富马酸泰吉利定注射液的上市,标志着恒瑞在镇痛麻醉领域上市1类创新药增至2款。值得注意的是,中国对麻醉药物进行管制,泰吉利定已经于2023年9月列入调整后的麻醉药品和精神药品目录,如有企业想进行仿制需要考量这一因素。图:信息来源:国家药监局 公安部 国家卫生健康委关于调整麻醉药品和精神药品目录的公告(2023年底120号)伊鲁阿克是由齐鲁研发的一种小分子药物,是一种ALK和ROS抑制剂。该药为中国化药一类。目前该药物最高研发阶段为批准上市,用于治疗非小细胞肺癌。伊鲁阿克在中国专利登记平台上登记1项专利信息,技术领域涉及化合物、用途。其中,ZL201410317076.7理论于2034年7月4日到期,并且原研针对该专利于2024年3月提交延长申请。图:伊鲁阿克中国专利登记平台收录情况,信息来源:中国专利登记平台经查看,ZL201410317076.7保护包含伊鲁阿克在内的通式化合物。图:信息来源:ZL201410317076.7(CN105330698B)专利伊鲁阿克首次在中国于2023年6月27日获批上市,暂未批准进入其他主流国家。伊鲁阿克已获批适应症:2023年6月27日,NMPA批准伊鲁阿克上市,用于既往接受过克唑替尼治疗后疾病进展或对克唑替尼不耐受的ALK融合基因阳性局部晚期或转移性NSCLC患者的治疗;2024年1月16日,NMPA批准伊鲁阿克用于ALK融合基因阳性局部晚期或转移性NSCLC患者的一线治疗。截止2024年4月7日,暂无仿制厂家提交该品种的上市申请记录。值得注意的是,为了帮助临床医师更好地了解伊鲁阿克的疗效和安全性,使伊鲁阿克得到更合理的临床应用,中国医疗保健国际交流促进会肿瘤内科学分会和中国医师协会肿瘤医师分会组织专家编写了《伊鲁阿克治疗间变性淋巴瘤激酶融合基因阳性局部晚期或转移性非小细胞肺癌中国专家共识(2024版)》。参考资源:
1、国家知识产权局、中国专利登记平台
2、注册信息:FDA、NMPA、EMA、PMDA及中国CDE等;
3、专利具体信息:相关专利授权文本
4、国家药监局 公安部 国家卫生健康委关于调整麻醉药品和精神药品目录的公告(2023年底120号)
声明:本文系药方舟转载内容,版权归原作者所有,转载目的在于传递更多信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除内容