
2024-06-19 09:59:28来源:细胞与基因治疗领域浏览量:601
日前,Mustang Bio公司公布其在研CAR-T细胞疗法MB-106进行中的1/2期临床试验最新数据。分析显示,接受该疗法的华氏巨球蛋白血症(WM)患者的总缓解率(ORR)高达90%,其中一位患者持久完全缓解达31个月,这些患者在治疗前均接受过大量前期治疗。受消息面影响,Mustang股价盘后暴涨477%,报0.75美元/股。

试验中的所有十例患者均曾接受过布鲁顿酪氨酸激酶抑制剂(BTKi)的治疗,并且在接受BTKi治疗期间病情持续恶化。患者之前接受过中位9线疗法,只有一例患者在接受MB-106治疗后开始接受额外的抗WM治疗。总体而言,接受MB-106治疗的患者中有90%(9/10)对治疗产生应答,包括3名患者达完全缓解、2名达非常好的部分缓解和4名部分缓解。此外,1例患者的病情稳定。其中一名获得完全缓解的患者已持续缓解31个月,该患者的免疫球蛋白M(IgM)水平在接受MB-106治疗后迅速降至正常范围,此后一直保持正常。
安全性方面,9例患者发生了细胞因子释放综合征(CRS):5例患者为1级,4例患者为2级。一例患者经历了1级免疫效应细胞相关神经毒性综合征(ICANS)。尽管剂量增加,但并未观察到3级或4级CRS或2、3或4级ICANS。
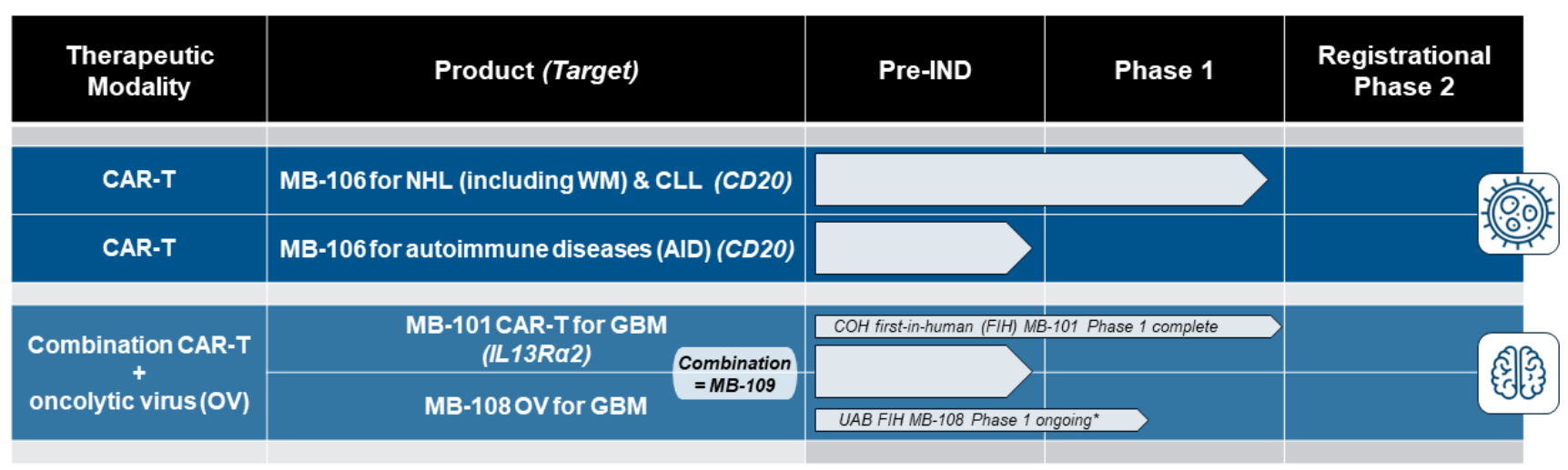
MB-106是一款靶向CD20的自体CAR-T细胞疗法,可通过门诊给药。MB-106由Mustang Bio和Fred Hutchinson癌症中心合作开发,用于治疗复发或难治性B细胞非霍奇金淋巴瘤(B-NHL)和慢性淋巴细胞白血病(CLL)患者。
[1] Mustang Bio Announces Favorable Efficacy and Safety Data from Complete Waldenstrom Macroglobulinemia Cohort of Phase 1/2 Clinical Trial of MB-106, CD20-Targeted Autologous CAR-T Therapy. Retrieved June 18, 2024 from https://ir.mustangbio.com/news-events/press-releases/detail/180/mustang-bio-announces-favorable-efficacy-and-safety-data
声明:本文系药方舟转载内容,版权归原作者所有,转载目的在于传递更多信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除内容