
2021-02-26 18:01:43来源:药智网浏览量:1392
导读:李天泉科普作品。
平常,我们都习惯了用原研药、仿制药来对药物进行划分,但近年来“生物类似药”热了起来,相关报道层出不穷,2020年新的《药品注册管理办法》专门将“生物类似药”分为一类。为何叫“生物类似药”,而不叫“生物仿制药”呢?所有的仿原研的生物药都叫生物类似药吗?生物药类似药的发展趋势如何?笔者带您走进生物类似药的世界。

生物类似药是一个相对较新的名词,是指在质量、安全性和有效性方面与已获准注册的参照药具有相似性的治疗用生物制品。
欧盟在2005年发布《生物类似药指南》,并于次年4月批准首款生物类似药,诺华开发的生长激素(somatropin,商品名Omnitrope)参考对象是IpsenPharma公司的生长激素(商品名NutropinAq)。
而一向引领风骚的美国却直到2010年才推出《生物药价格竞争及创新法案》,之后又过了五年,FDA才批准了首款生物类似药Zarxio(诺华山德士开发的非格司亭生物类似药)。
中国药监局则等到FDA批准第一个类似药的半年后,也就是2015年12月才出台《生物类似药研发与评价技术指导原则》;在2019年2月批准首个生物类似药(复宏汉霖公司的利妥昔单抗注射液);在2020年的《药品注册管理办法》才确认生物类似药的分类。
为何不用仿制药,要造出一个新名词“类似药”呢?而且这个新名词所带的研发注册要求也完全与仿制药不同呢?这就要谈到生物药与化学药的区别:化药通常又称小分子药物(大分子占比很小),化学结构式简单,只要是化学结构式一致,一般情况下我们就认为活性成份相同。而生物药通常又称为大分子药物,分子量通常大于5000,由若干个氨基酸序列组成,如果要求“仿制”得完全一样,不仅氨基酸序列这个一级结构相同,还要求高级结构(二级/三级/四级)相同,甚至糖基化也相同。好比去仿制一根绳子所挽成的疙瘩,不仅要求绳子上每根纤维一样,而且疙瘩的立体结构也要完全一样,这简直就是一个不可完成的任务。不信,看下图这个单抗生物药,您能造出丝毫不差的仿制品吗?
所以,为了保持严谨,没有用“仿制药”,而使用“生物类似药”的概念。不仅生物药如此,考虑到中药的成份复杂性,在2020年的药品注册法规中也放弃了“中药仿制药”的概念,而是用“同名同方药”来代替。
那是不是所有仿已上市的生物药都是生物类似药呢?非也,药品注册分类中对应“生物类似药”(3.3类)还专门设了一个类别:“其他生物制品”(3.4类),也就是说有部分生物药不按生物类似药的技术要求申报和监管,甚至像免疫球蛋白、人血白蛋白还可以免临床试验。
美国FDA指出:生物类似药与参照药高度相似,活性成分有细微差别,但在产品的安全性、纯度和有效性方面没有临床意义的差别。
另外,“类似药”与“仿制药”的区别可谓一字值千金,仿制药可以做到和原研药相同,因此,只需做生物等效性(BE)试验,花几百万元就可以证明二者的等效性。但类似药,不论怎么做都只能做到类似或者一致,而不是相同,而且生物药的质量与生产工艺息息相关,要想证明与原研药的一致性,就不是这么简单了。除了药学研究外,还需要免疫原性研究、有可能需要毒性研究,而对于临床试验,则不仅需要做药代动力学/药效动力学(PK/PD)试验,还需要在患者身上开展临床试验,通过大临床试验判断类似药在安全性和有效性与原研药有无差别,轻微的差别是必然的,只要没有临床意义的差别就行。
法规对生物类似药注册要求高,有其科学性与逻辑必然性,可是药厂为啥愿意投入上亿的经费去研发一个生物类似药呢,这笔钱做10个化学仿制药绰绰有余,在中国差不多可以做一个创新药了。药企领导人可都是聪明人,这笔帐要从销售市场上来算。
2019全球畅销药排行榜TOP10中就有8个是生物药,主要是单克隆抗体,简称单抗,排名第一的阿达木单抗(修美乐)已经蝉联榜首8年了,年销售额达1320亿人民币,这个销售金额相当于中国前三大药厂的药品销售总额了。
2019全球畅销药排行榜TOP10
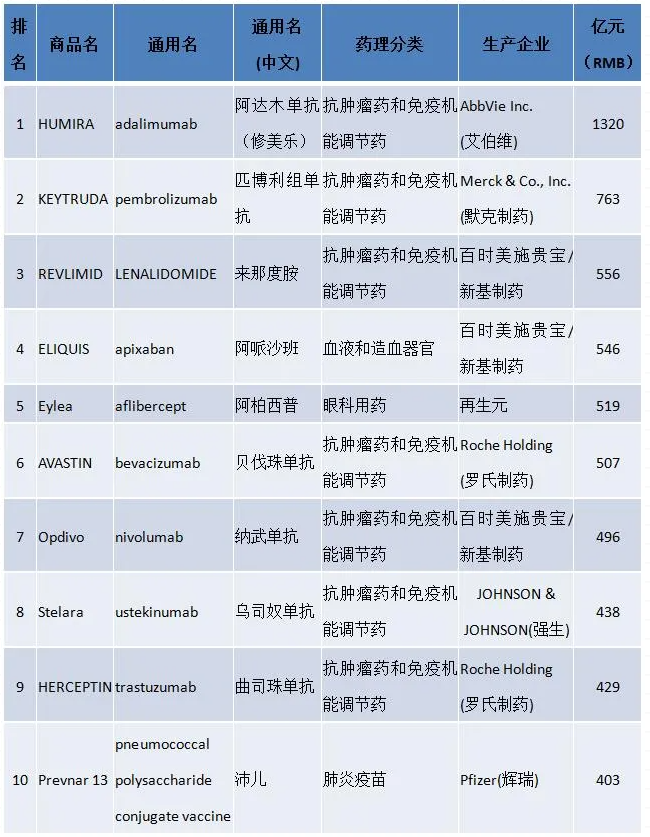
数据来源:药智全球畅销药品数据库
榜单上的这些单抗品种正是目前生物类似药的香饽饽,让我们以阿达木单抗和利妥昔单抗为例,来感受一下中国生物类似药的研发热情:全球畅销药冠军阿达木单抗注射液,中国已经批了四个厂家,还有更多的厂家走在申报的道路上。
阿达木单抗生物类似药申报情况
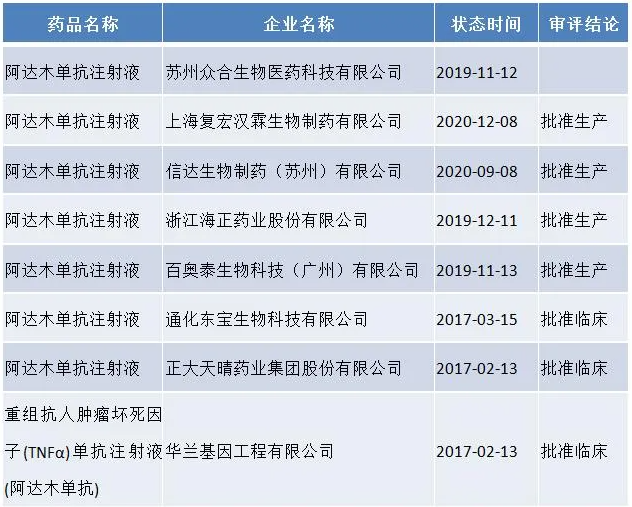
数据来源:药智数据
利妥昔单抗生物类似药申报情况
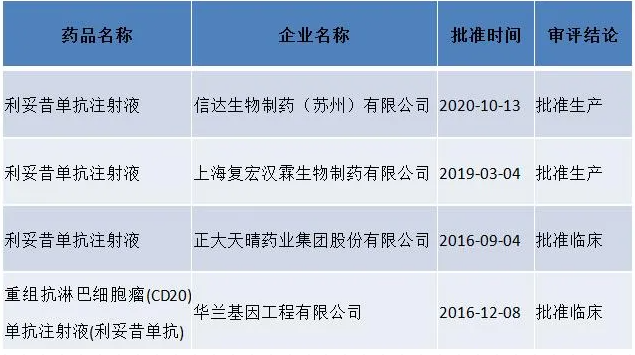
数据来源:药智数据
有人说,再好的赛道到了中国也会变得拥挤,生物类似药也是如此,目前中国布局生物类似药的企业近200家,在研的生物类似药多达400个,涉及50余款原研药物,所以未来的生物类似药的竞争将非常激烈。那生物药的价格是否也会像仿制药一样降为地板价呢?
生物类似药的定价逻辑和仿制药不同,仿制药竞争是相同产品之间的制造边际成本竞争,药物价格反映边际成本,通俗讲就是打价格战,纯价格竞争;而生物类似物则由于研发成本高、边际制造成本高,专利界限模糊,另外仿制药是没有商品名的,只有通用名,而生物类似药则国家药监局会授予商品名,从而在多个层面形成竞争壁垒,在一定程度保证了生物类似药的高价格,如齐鲁的贝伐珠单抗1266元/瓶(原研1998元)、复宏汉霖的阿达木单抗1398元/支(原研2418元)。
所以产业界、投资者对生物类似药都充满了期待,据相关预测中国的生物类似药的市场将会迅猛增长,见下图:
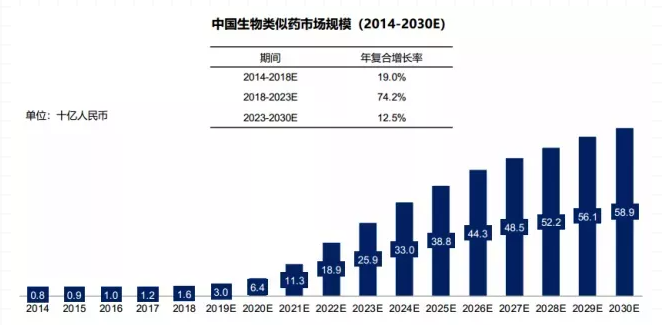
来源:弗若斯特沙利文报告
话虽如此,但是在中国政策导向特别明显,国家医保局已放出风来,生物类似药也会纳入全国带量采购,一旦进入集采,竞争厂家过多,生物类似药的高定价逻辑是否还可行就不好说了。希望相关部门在制定集采政策时,充分考虑生物类似药的特点,让这个新事物在中国走地更稳健,甚至走在世界的前列。
来源:药智网
声明:本文系药方舟转载内容,版权归原作者所有,转载目的在于传递更多信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除内容!