2024-12-18 00:00:00来源:微谱生物科技浏览量:1035
一:CHO重组表达上市申报前为什么要关注遗传稳定性?
CHO细胞因为其特殊的性能占据生物治疗性重组蛋白质应用方面的全球市场89%。CHO细胞能够适应无血清培养基的条件,可以悬浮培养利于生产放大;同时CHO细胞是可进行基因操作的,容易得到高产的单克隆细胞株,也可以进行类似的翻译后修饰。尤其值得注意的是,CHO细胞对于人类病毒的敏感性较低,非常利于生物制药的应用。但CHO的基因可塑性同样会表现为细胞的遗传不稳定性,如基因的重排、目的基因的突变、表观遗传学的基因沉默、以及基因扩增系统的多拷贝表达压力等。为了药品生产的持续稳定,监管机构对于CHO细胞的表型稳定性与遗传稳定性均提出了相应要求。
二:中美法规或指南对于遗传稳定性(CHO重组表达)是如何规定的?
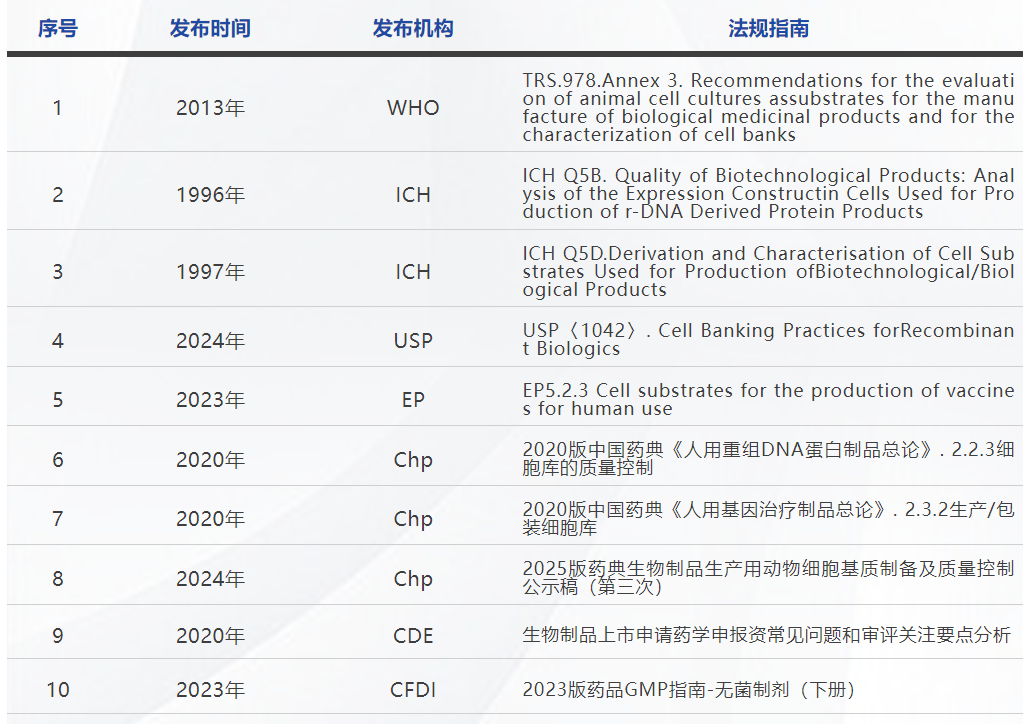

三:遗传稳定性考察的项目有哪些?

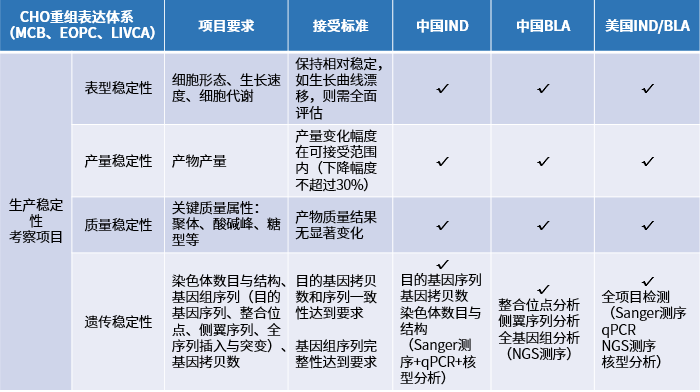
四:生产稳定性考察内容与接受标准
生产稳定性的考察会体现在表型稳定性、产量稳定性、质量稳定性与遗传稳定性等4个方面,随着CHO的代次不断增加,其生产表型以及产量会发生一定程度的变化,一般要求产量下降超过30%作为限定代次。
五:微谱生物科技:遗传稳定性检测整体解决方案
根据现行法规与指南要求,要求对目的基因序列、基因拷贝数、整合位点分析、侧翼序列分析以及表达载体的突变或缺失分析,其中欧美对目的基因的RNA水平确认有要求,同时关于染色体数目与结构方面推荐为可选项目。