
2025-02-17 09:08:01来源:郑在说药浏览量:2444
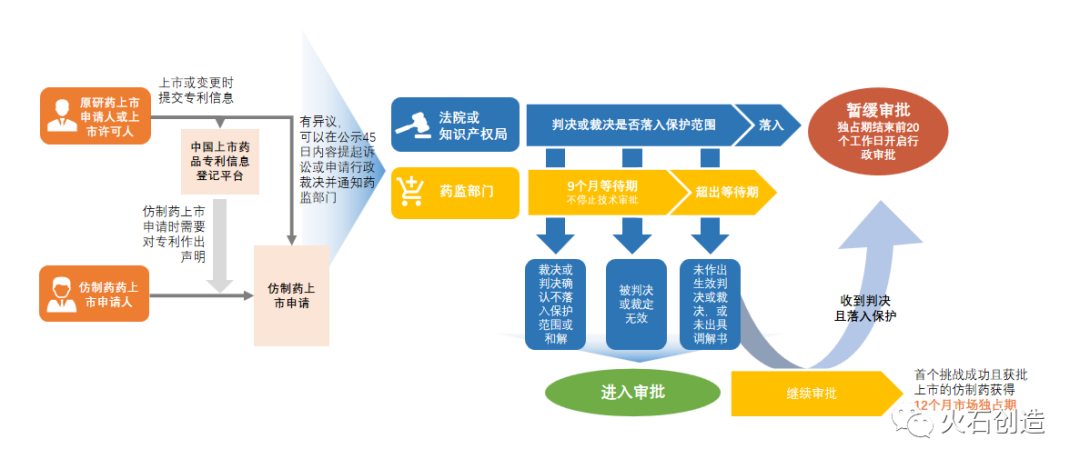
一、专利制度基础理论 1.1 专利制度简介 专利制度指国家依法授予发明人或其合法受让人在一定期限内对其发明创造享有独占权的一种法律制度。这里的“发明创造”通常包括发明、实用新型和外观设计等多种形式。 专利权的授予,意味着发明人或其受让人在专利有效期内,有权禁止他人未经许可实施其专利,即享有专利的排他性使用权。同时,专利制度还要求将发明创造的内容向社会公开,以促进技术信息的交流与传播。 专利制度的起源可以追溯到中世纪欧洲,早期的专利制度并非现代意义上的知识产权保护,而是更多地与封建王权、特权授予以及皇家垄断有关。例如,13世纪的英国,国王开始授予某些工匠或商人独占制造某种产品的权利,以换取税收或忠诚。这些早期的“专利”往往具有浓厚的封建色彩,缺乏现代专利制度所强调的公开性和普遍性。 然而,随着资本主义的兴起和科技进步的加速,专利制度逐渐摆脱了封建特权的束缚,开始向现代知识产权保护体系演变。17世纪,英国率先颁布了现代意义上的专利法——《垄断法案》(Statute of Monopolies),该法案明确规定了专利权的授予条件、保护期限以及专利权的限制,为现代专利制度的形成奠定了基础。 随后,欧美各国纷纷效仿英国,建立了各自的专利制度。18世纪末至19世纪,随着工业革命的深入发展,专利制度在推动技术创新、促进经济发展方面的作用日益凸显。 进入20世纪,随着全球化进程的加速和知识产权保护的国际化趋势,专利制度也开始向国际层面拓展。世界知识产权组织(WIPO)、世界贸易组织(WTO)等国际组织在推动专利制度的国际化、标准化方面发挥了重要作用。同时,各国政府也开始加强专利制度的国际合作与交流,共同应对跨国专利侵权、专利纠纷等挑战,以维护全球创新生态的平衡与稳定。 1.2 专利制度的核心内涵 专利制度就像是科技世界里的一把保护伞,它用法律和经济的力量,为那些动脑筋、搞创新的人们撑起了一片天。 这个制度的核心,就是要确认和保护那些发明家的智力成果,让他们的努力和创意得到应有的回报。同时,它还要促进这些技术的有偿转让和交流,让好的点子能够像种子一样,播撒到更广阔的田野上,推动整个社会的经济发展。 当谈及专利制度时,有两个理论经常被拿出来讨论,那就是自然权利论和利益平衡论。 自然权利论认为创新是发明家们与生俱来的权利,这些聪明的脑袋瓜儿想出来的点子,就像他们自己的孩子一样,应该得到天然的、不可剥夺的保护。专利制度,就是为了让这些发明家们的劳动得到承认,让他们的创新成果能够独占一方,得到应有的回报。 但利益平衡论认为,虽然这些创新成果确实凝结了发明家的智慧和劳动,但是知识的生产可不是一个人的事儿。在创造的过程中,发明家们也会借鉴和利用前人的智慧成果。所以,专利权的独占性不能太过头,得有个度,得平衡好发明家和社会公众之间的利益关系。这样,既能保护发明家的合法权益,又能让社会公众能够合理、合法地利用这些创新成果,大家一起推动科技进步和社会发展。 在专利法的实践中,这两种理论就像两个拔河队,一直在较着劲儿。而《专利法》就像是一个公正的裁判,它的宗旨就是要找到一个平衡点,让个人利益和社会公众利益都能得到满足。一方面,它要赋予发明家们对他们创新成果的独占权,激励他们投入更多的研发资源,去搞更多的创新。另一方面,它也要通过设置专利保护期限、强制许可等制度,对专利权的独占性进行一定的限制,防止发明家们一家独大,阻碍了技术的进步。 专利制度还有一个很重要的功能,那就是激励技术创新,只要你能搞出点新花样,就能得到一份丰厚的奖励。这份奖励不仅能让个人发明家们心动,也能让企业、科研机构等创新主体心动。在专利制度的保护下,他们可以更加自信地投入研发资源,去探索新技术、新产品和新方法,推动科技的进步和社会的发展。 但是,这个激励也不能太大,专利权的独占性太强,就可能导致市场垄断。就像是一个大胖子堵住了小巷子,别人都走不过去。 如果专利权人滥用他们的市场优势地位,通过高价许可、拒绝许可等方式来排挤竞争对手,就会限制市场竞争,损害消费者和社会公众的利益。所以,专利制度在激励技术创新的同时,也得对市场垄断进行调控。 为了实现这个目标,专利法及相关法律法规设置了一系列制度规则。比如,专利保护期限的限制,就像是一个定时炸弹,到时间了就会爆炸,让创新成果进入公共领域,供大家一起使用。 还有强制许可制度,为了保护公众利益,让专利权人在特定情况下必须许可他人实施他们的专利,推动技术的推广和应用。 除了这些,反垄断法也在对专利权滥用行为进行规制。我国也非常重视保护知识产权与反垄断之间的平衡和协调,通过修改反垄断法、制定相关指引和规定等措施,不断完善知识产权领域的反垄断制度规则,确保市场的公平竞争和消费者的利益。 最后,专利法体系建立过程中存在两个互斥的原则:先发明制和先申请制。 先发明制认为真正的发明者应该享有对其创新成果的独占权,不管他们申请专利的时间早晚。但是,这个原则在实践中有点麻烦,因为发明的完成时间很难界定,容易引发争议和纠纷。而且,它还可能鼓励发明家们保密他们的创新成果,等待合适的时机再申请专利,这样就阻碍了技术的交流和推广。 相比之下,先申请制更加注重申请的先后顺序,只要你能先提出申请,你就能得到专利权。这个原则的好处在于,它能够鼓励发明家们在完成发明创造后尽快提出申请,避免被他人窃取研究成果。同时,它也有利于促进技术的交流和推广,因为一旦发明成果被公开申请专利,其他人就可以了解并借鉴这个成果,推动相关领域的科技进步。 我国和大多数国家一样,遵循的是先申请制。这个原则在专利法的实践中得到了广泛应用。当然,先申请制也不是万能的。在某些情况下,它可能导致真正的发明者因为没有及时申请专利而丧失他们的创新成果的独占权。但是,总体来说,先申请制在促进技术创新、保护发明人权益和推动社会经济发展方面还是发挥了重要作用。 1.3 专利的类型与特性 1.3.1 专利的类型 在我国,专利法所保护的发明创造主要包括发明、实用新型和外观设计三种类型。(美国没有实用新型,但是有植物专利;欧洲没有实用新型) 发明专利是指对产品、方法或者其改进所提出的新的技术方案,它主要包括产品发明和方法发明两种类型。 产品发明是指创造出包含新技术方案的物品,例如对机器、设备、工具、用品等物品进行改进而做出的发明创造。例如,一款全新的汽车发动机,或者一种改进后的医疗设备,都属于产品发明的范畴。 而方法发明则是指利用规律使用、制造或测试产品的新的步骤和手段,例如适用于某种物品的加工方法、测试方法、制造工艺等。 发明专利的保护期限为20年,自申请日起,下同。 实用新型专利则是对产品的形状、构造或者其结合所提出的适于实用的新的技术方案。 与发明专利相比,实用新型专利更注重产品的形状和构造的改进,而不涉及方法层面的创新。例如,一种改进后的水杯设计,或者一种新型的手机支架,都可能获得实用新型专利的授权。实用新型专利的新颖性、创造性和实用性要求与发明专利相似,但其审查过程相对简化,授权速度更快。 实用新型专利的保护期限为10年。 外观设计专利则是对产品的整体或者局部的形状、图案或者其结合以及色彩与形状、图案的结合所作出的富有美感并适于工业应用的新设计。 外观设计专利主要关注产品的外观美感,要求设计必须是对产品的整体或局部所作的设计,必须富有美感,必须是适于工业上的应用,并且必须是新设计。例如,一款新的手机外观设计,或者一种独特的包装盒设计,都可能获得外观设计专利的授权。 外观设计专利的保护期限为15年。 1.3.2 专利的授权标准 发明专利的新颖性、创造性和实用性是其获得授权的重要条件。 第二十四条 申请专利的发明创造在申请日以前六个月内,有下列情形之一的,不丧失新颖性: (一)在国家出现紧急状态或者非常情况时,为公共利益目的首次公开的; (二)在中国政府主办或者承认的国际展览会上首次展出的; (三)在规定的学术会议或者技术会议上首次发表的; (四)他人未经申请人同意而泄露其内容的。 1.3.3 专利的特性 独占性、时效性和地域性是专利的三大特性。 独占性 是专利最为显著的特征,它赋予专利权人在一定期限内对发明创造的排他性使用权,禁止他人未经许可的制造、使用、销售或进口。这种排他性权利,有效保护了创新者的智力劳动成果,激励了持续创新,同时也为专利权人带来了经济收益,为研发活动提供了资金保障。 时效性 专利权的授予并非永久,而是具有一定的期限,旨在平衡专利权人利益与社会公共利益。随着专利权的到期,相关技术进入公有领域,为社会公众所共享,促进了技术的广泛传播与应用,推动了科技进步与经济发展。 地域性 专利权仅在授予该专利权的国家或地区内有效,体现了各国专利制度的独立性。若要在其他国家或地区获得专利保护,必须向相应专利局提出申请。 二、我国药品专利制度介绍 1984年 我国首部《专利法》正式颁布实施,标志着我国知识产权保护制度的初步建立。然而,在这部具有里程碑意义的法律中,药品并未被纳入专利保护的范围。这一决策的背景复杂,既反映了当时我国医药产业的实际情况,也体现了国家对药品可及性的关注。 彼时,我国医药产业尚处于起步阶段,新药研发能力薄弱,仿制药占据市场主导地位。将药品排除在专利保护之外,一方面可以减轻国内医药企业的研发压力,另一方面也有助于降低药品价格,提高药品的可及性。然而,这一决策也在一定程度上限制了我国新药研发的积极性,影响了医药产业的创新活力。 1992年 随着改革开放的深入和市场经济体制的确立,我国医药产业迎来了快速发展的黄金时期。为了适应这一变化,1992年,我国对《专利法》进行了首次修订,将药品、用化学方法获得的物质等纳入了专利保护的范围。这一修订标志着我国药品专利保护制度的初步建立,为新药研发提供了法律保障。 2002年 《药品注册管理办法(试行)》首次就药品注册审批涉及的专利问题制定了相关规则,其第十三条明确规定:针对已在中国取得专利权的药品,有意申请者有权在专利保护期结束前的两年内提交注册申请。只要申请满足所有既定条件,相关部门将在专利权到期之后,正式颁发药品批准文号,允许该药品上市。 2008年 我国对《专利法》进行了再次修订,规定了在行政审批流程中,为了提供必要的信息而制造、使用或进口专利药品及专利医疗器械的行为,并不构成对专利权的侵犯(Bolar例外)。 这一规定旨在确保行政审批流程的顺利进行,同时平衡公共利益与专利权人的合法权益。它允许在特定情境下,即为了行政审批目的,可以合法地使用专利药品和医疗器械,而无需担心专利侵权的风险。这既保障了行政审批的准确性和有效性,又避免了因专利侵权纠纷而可能导致的行政审批延误或受阻。 2020年 经过多年的酝酿与准备,我国新修订的《专利法》正式实施,其中第七十六条新增了药品专利链接制度的具体规定。这一制度的本土化构建,标志着我国药品专利保护制度迈上了新的台阶。 药品专利链接制度的实施,对于我国医药产业具有深远影响,一方面它有助于保护专利权人的合法权益,激励新药研发的积极性;另一方面,它也有利于仿制药申请人更容易地获取相关药品信息,从而更好地做出战略规划,防止低端仿制、无效仿制、扎堆仿制。 2021年 2021年6月1日起施行的专利法第四次修正案中引入了药品专利保护期延长制度。该制度规定,对于在中国获得上市许可的新药相关发明专利,可以给予专利权期限补偿,补偿期限不超过五年,且新药批准上市后的总有效专利权期限不得超过十四年。 2.2 现行制度的核心机制 专利登记与仿制药声明制度 其设计理念深受美国橙皮书制度的启发,旨在构建一个透明、高效的专利信息平台,以平衡创新激励与仿制药竞争之间的关系。这一制度要求所有在中国上市的原研药品企业,必须在中国上市药品专利信息登记平台上详尽地登记其持有的与药品直接相关的专利信息。这些信息覆盖广泛,从药品的通用名称、商品名称到具体的剂型、规格,再到上市许可持有人以及最为关键的专利号等,每一项信息都是仿制药研发和申请过程中不可或缺的参考基准。通过这样的登记制度,不仅为仿制药企业提供了清晰、准确的专利信息指引,避免了盲目研发可能带来的专利侵权风险,同时也确保了原研药企的专利权益得到应有的尊重和保护。 在仿制药申请人提交上市许可申请时,他们必须对照已公开的专利信息,针对每一件与被仿制药相关的专利,谨慎地作出四类声明之一。这些声明类型多样,从确认相关专利不存在,到专利已到期或被宣告无效,再到承诺在专利有效期内暂不上市,以及主张相关专利应被宣告无效或未落入其保护范围,每一种声明都反映了仿制药申请人对专利状态的不同理解和应对策略。这样的制度设计,既为仿制药申请人提供了明确的行动指南,也促使他们在研发初期就充分考虑专利因素,从而有效降低了潜在的专利侵权风险。 专利纠纷早期解决程序 其存在意义在于将潜在的专利纠纷扼杀在萌芽状态,该程序赋予了专利权人或利害关系人在仿制药上市申请阶段提出异议的权利,并允许他们请求人民法院或国务院专利行政部门进行裁决。 这一机制的创新之处在于,它将仿制药上市后可能发生的专利纠纷提前到了仿制药申请上市阶段进行解决,从而有效避免了因专利纠纷而导致的市场混乱和消费者利益受损。 同时,该程序还设置了“45日”的异议期限,以及随后的诉讼或行政裁决请求期限,为双方提供了充足的时间来准备和提交相关证据材料,确保了裁决的公正性和准确性。虽然实践中对于“45日”期限的性质存在一定的争议,但普遍观点认为,这一期限的设置旨在鼓励双方通过协商和调解的方式解决纠纷,减少诉讼成本和时间成本。 在9个月的等待期内,国家药品审评机构将暂停行政审批流程,但技术审评工作仍将继续进行。这一制度设计既确保了药品审评审批的连续性和高效性,也为专利权人和仿制药申请人提供了充足的时间来解决专利纠纷。在等待期内,双方可以通过协商、调解、诉讼或行政裁决等多种方式来解决专利纠纷。 如果等待期内诉讼或行政裁决结果确认仿制药不落入专利权保护范围,或者双方达成了和解协议,或者相关专利被宣告无效,那么仿制药注册申请将顺利转入行政审批环节,继续其上市之路。这样的制度设计,既保护了专利权人的合法权益,也为仿制药申请人提供了合法的上市路径,确保了药品市场的公平竞争和有序发展。 专利期补偿制度 在药品研发领域,从提交专利申请到最终获得批准往往需要经历一个漫长而复杂的过程。这段等待时间内,专利权人可能无法充分行使其专利权,从而面临经济损失。为了平衡这一不公平现象,我国法律引入了专利期补偿制度。根据该制度,当专利权人因行政审批等原因导致专利权有效期限缩短时,可以申请专利期补偿。 专利权人提出请求时药品及其专利应当满足以下条件: 1)一个药品同时存在多项专利的,专利权人只能请求对其中一项专利给予药品专利期限补偿; 2)一项专利同时涉及多个药品的,只能对一个药品就该专利提出药品专利期限补偿请求; 3)该专利尚未获得过药品专利期限补偿; 4)请求给予药品专利期限补偿的专利剩余保护期限不少于6个月。 三、典型案例的启示意义 吉列德在丙肝领域的崛起始于2011年的一次战略性并购。 彼时,市值仅300亿美元的公司以110亿美元高价收购未上市的生物医药公司Pharmasset,押注其丙肝候选药物sofosbuvir(索磷布韦)。这一决策起初备受质疑,但2013年sofosbuvir作为首个无需干扰素即可治愈丙肝的药物获FDA批准后,立刻改写行业格局。 2014年,仅该药物一季度销售额即达22.7亿美元,全年销售额突破百亿美元,推动公司总营收从2013年的110亿美元跃升至2014年的250亿美元。 次年,第二代产品Harvoni(索磷布韦/雷迪帕韦复方)凭借99%的治愈率进一步巩固市场地位,与Sovaldi共同贡献191亿美元年销售额,使吉列德跻身全球药企十强。 专利布局层面,吉列德构建了严密的知识产权网络,其核心策略围绕化合物专利展开,例如sofosbuvir的基础化合物专利在中国等地持续生效,即使前药专利被驳回,仍能阻止仿制药上市。 通过连续推出四代丙肝药物(Sovaldi→Harvoni→Epclusa→Vosevi),吉列德实现技术迭代与专利生命周期管理的结合。Epclusa作为首个泛基因型疗法,Vosevi针对耐药患者,均在不同细分市场延长独占期。 知识产权出版社的分析显示,吉列德在抗丙肝领域专利申请覆盖化合物、制备工艺、适应症扩展等多个技术主题,并通过PCT国际专利体系布局全球主要市场,形成竞争壁垒。 然而,Sovaldi单片定价高达1000美元,全疗程8.4万美元的定价体系,虽在商业层面取得短期暴利,却引发公共健康伦理争议。这种“高价收割”策略的逻辑建立在对丙肝患者池快速缩水的预判上——治愈性药物本质上消灭自身市场。 2015年起,随着存量患者减少及竞品入场,吉列德丙肝药收入逐年下滑,2017年推出的第四代药物Vosevi虽将治愈率提升至96-97%,仍难阻业务萎缩趋势。 此时,竞争对手如艾伯维(AbbVie)通过Viekira Pak等产品发起价格战,与渠道商Express Scripts签订排他协议,迫使吉列德转投CVS以维持市场份额。这种竞争不仅压缩利润空间,更凸显专利悬崖临近的危机——吉一代专利将于2024年到期,届时仿制药冲击将彻底改变市场格局。 中国市场成为专利博弈的特殊战场。中国约有1000万丙肝患者,传统疗法依赖干扰素联合利巴韦林,治愈率仅60%且副作用显著。吉列德虽在中国申请索磷布韦前药专利,但基础化合物专利仍是制约仿制药生产的关键。 这种策略导致中国患者长期无法获得低价仿制药,而原研药价格远超普通民众承受能力。相较之下,印度通过强制许可制度允许本土仿制,形成鲜明对比。这种差异既反映各国专利制度的弹性,也暴露全球药品可及性议题的结构性矛盾。 吉列德的案例揭示医药创新的悖论:革命性疗法既拯救患者,又因商业逻辑导致可及性困境;专利制度虽激励研发投入,却可能异化为市场垄断工具。其丙肝药物定价策略引发全球范围内关于药品定价机制、专利伦理与公共卫生政策的持续辩论。世界卫生组织将丙肝列为2030年消除目标,但实现这一愿景需要突破专利壁垒与价格障碍的双重束缚。 3.2 PD-1单抗专利战 涉案的核心专利可追溯至小野制药与百时美施贵宝(BMS)联合布局的专利体系,其中最为关键的是欧洲专利EP1537878,该专利权利要求覆盖了“通过抑制PD-1、PD-L1或PD-L2信号通路治疗癌症的方法”,明确将“抗PD-1单抗治疗癌症”纳入保护范围。 此外,BMS与小野制药在美国、日本、澳大利亚等地也拥有同族专利,例如美国专利US8728474B2和日本专利JP4711727B2,这些专利在诉讼中成为对抗默沙东Keytruda的核心武器。 值得注意的是,小野制药的专利申请策略具有前瞻性,其权利要求不仅涵盖具体的抗体结构,还扩张至治疗方法的专利化,这种“大包围”式的布局为后续的全球专利战埋下伏笔。 2014年BMS发起专利诉讼时,默沙东曾对EP1537878提出异议,但欧洲专利局于2014年6月驳回异议,英国高等法院更在2015年10月判定该专利有效。 这一判决直接导致2017年的和解协议:默沙东需支付6.25亿美元首付款,并按Keytruda销售额的6.5%(2017-2023年)和2.5%(2024-2026年)支付分成。 值得深思的是,尽管BMS的Opdivo在非小细胞肺癌(NSCLC)适应症竞争中失利,但凭借专利壁垒仍可长期分享竞品的市场收益,这凸显了药物专利超越产品实际疗效的战略价值。 该案例有两点启示: 第一,揭示了“专利丛林”策略的威力,BMS通过早期布局涵盖治疗机理、抗体结构、适应症扩展等多维度的专利组合,构建了难以绕过的技术壁垒。即使竞争对手开发出结构不同的PD-1抗体,只要落入治疗方法权利要求范围仍需支付许可费。这种策略在生物医药领域愈发普遍,如安进在PCSK9抑制剂专利战中同样通过表位专利限制竞品。 第二,专利地域性差异导致市场格局分化,BMS的专利网络虽覆盖欧美日等主要市场,但中国因未申请对应专利而形成“安全区”,国内超80家企业得以自由开发PD-1单抗。这种地域性缺口既为中国药企赢得发展窗口,也暴露了跨国药企专利布局的盲点。 更深层的启示在于专利制度对创新的双向影响,一方面,BMS通过专利许可获得持续收益,证明强专利保护能激励原研投入;但另一方面,过宽的专利范围可能抑制后续创新,如EP1537878将PD-1通路机制专利化,客观上提高了后来者进入门槛。 中国专利审查中强调“技术方案需得到说明书支持”的原则,实质是在平衡保护范围与创新空间的关系。例如基石药业CTLA-4单抗联用方案因给药间隔特征无法与制药过程关联,难以在中国获得专利保护,而欧美则允许此类权利要求。这种制度差异提示,中国在借鉴国际经验的同时,建立了适应本土创新生态的专利审查标准。 PD-1专利战印证了三个趋势: 其一,生物药专利战焦点从化合物结构转向治疗方法与应用场景,这要求企业加强机理研究和适应症专利布局; 其二,联合疗法成为规避专利风险的突破口,如恒瑞医药引入CTLA-4单抗构建联用方案; 其三,专利攻防从单一产品扩展至全产业链,默沙东在双抗领域的新布局正是为应对PD-1专利到期后的市场冲击。 对于中国药企而言,既要利用专利地域性差异加速追赶,也需警惕未来出海时可能遭遇的专利狙击,百济神州与伊布替尼的专利纠纷便是前车之鉴。 3.3 新冠疫苗专利豁免争议 新冠疫苗专利豁免的争议本质上是知识产权保护与公共健康权益的动态博弈。支持豁免的一方援引《TRIPS协定》第31条关于公共健康例外的条款,主张在疫情紧急状态下应突破专利壁垒,扩大疫苗生产规模。 印度和南非提出的豁免提案(IP/C/W/669)涵盖疫苗、治疗药物及生产材料的专利权,主张豁免期限至少三年。这一立场得到包括中国在内的部分发展中国家支持,认为此举有助于弥合全球疫苗分配鸿沟,例如非洲国家的接种率在2021年底仅为8%,远低于发达国家的70%。 中国作为兼具疫苗研发能力和制造产能的国家或地区,在WTO框架下提出“双轨策略”:一方面通过专利池授权技术转移,另一方面协助发展中国家建立本土生产能力,如科兴疫苗在埃及、巴西的本地化生产。 反对豁免的阵营则强调专利制度对创新的基石作用,以瑞士、德国为代表的发达国家指出,mRNA疫苗的快速研发本身依赖专利保护下的高额研发投入(辉瑞-BioNTech疫苗研发成本约20亿美元),若豁免专利可能削弱企业应对未来疫情的创新动力。 更有实证研究表明,专利信息的公开披露对技术扩散效果有限——即使公开专利文本,疫苗生产仍受制于技术秘密(如细胞培养工艺参数)和供应链壁垒(如脂质纳米颗粒的专用脂质体供应)。例如,莫德纳曾宣布不强制执行疫苗专利,但截至2022年全球仍无企业能独立复制其生产工艺,证明专利豁免无法单方面解决技术壁垒。 新冠危机暴露了现有强制许可机制的局限性,尽管《多哈宣言》明确了公共健康危机下的强制许可路径,但程序繁琐(平均耗时18个月)且易引发贸易报复,导致其实际使用率极低。 中国虽在《专利法》第55条中规定强制许可条款,但至今未有实施案例,凸显法律框架与实操需求的脱节。未来改革可借鉴加拿大《COVID-19应急响应法》的“快速通道”机制,允许在疫情等紧急状态下简化申请流程,同时建立补偿金预存制度以减少专利权人诉争风险。 四、总结 专利制度作为现代知识产权体系的核心组成部分,其本质是通过法律手段赋予创新主体在一定期限内对技术成果的排他性权利,以此平衡私权保护与公共利益的关系。 这一制度的雏形可追溯至15世纪威尼斯颁布的《专利法》,后经英国《垄断法》的体系化演进,逐步形成以公开换保护、先申请制为核心的现代专利框架。 中国的专利制度虽起步较晚,但自1984年首部《专利法》颁布以来,历经四次修订,构建了涵盖发明、实用新型、外观设计的三类专利体系,并确立了行政与司法双轨保护机制,体现了从“被动接轨”到“主动创新”的制度转型。其核心特征在于通过审查授权程序甄别技术创新价值,同时以地域性、时间性限制保障技术传播与公共福祉。 在药品领域,专利制度具有特殊性: 一方面,药品研发的高投入与长周期特性使得专利保护成为激励创新的关键机制,例如PD-1单抗技术通过专利布局形成技术壁垒,推动肿瘤免疫治疗领域的突破。 另一方面,专利垄断可能加剧药品可及性矛盾,这在新冠疫苗专利豁免争议中尤为凸显——国际社会围绕TRIPS灵活性条款展开博弈,折射出创新激励与公共健康权保障的深层冲突。 我国药品专利制度的演进正逐步平衡这一矛盾:从早期单纯的技术保护,发展到引入药品专利链接制度、Bolar例外等特色规则,并在2020年《专利法》修订中首次确立药品专利期限补偿制度,既强化了原研药企权益,也为仿制药合规上市预留通道。 吉列德丙肝药专利博弈中,企业通过全球专利布局与定价策略实现超额收益,但发展中国家以强制许可为谈判筹码,迫使权利方调整授权政策,印证了“契约论”下利益再平衡的必然性。 而PD-1单抗领域的专利混战,则暴露出生物医药领域权利要求书撰写质量、创造性判断标准等制度细节对产业竞争格局的深远影响。 这些案例共同表明,专利制度不仅是技术确权的工具,更是国家创新战略的载体,其运行效果取决于立法设计、司法实践与产业政策的协同效能。




声明:本文系药方舟转载内容,版权归原作者所有,转载目的在于传递更多信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除内容