一、2025年3月3日中药品种保护受理公示
https://www.nmpa.gov.cn/zwfw/zwfwgggs/zypzbhslgs/20250303152654142.html二、国家药监局关于批准注册188个医疗器械产品的公告(2025年2月)(2025年第24号)网址:https://www.nmpa.gov.cn/xxgk/ggtg/ylqxggtg/ylqxpzhzhcchpgg/20250307150221145.html2025年2月,国家药监局共批准注册医疗器械产品188个。其中,境内第三类医疗器械产品150个,进口第三类医疗器械产品26个,进口第二类医疗器械产品11个,港澳台医疗器械产品1个(具体产品见附件)。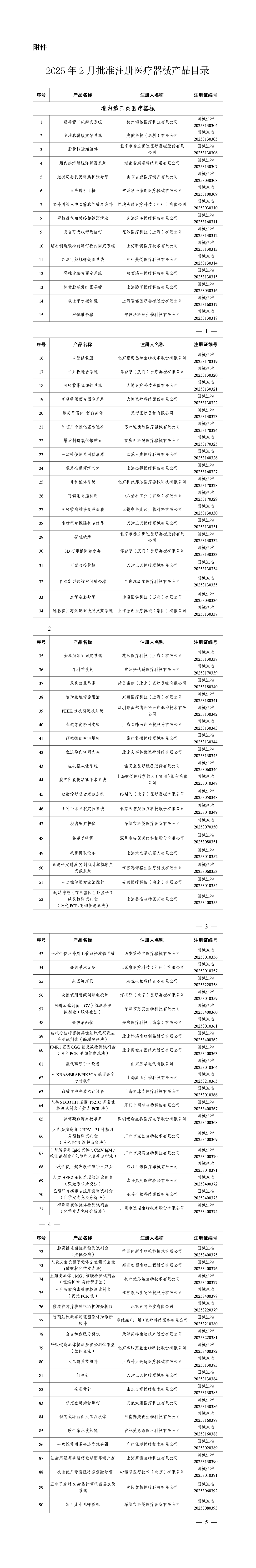
......
https://yjj.beijing.gov.cn/yjj/zfxxgkzl17/fdzdgknr80/tjxx74/nb83/743554166/index.html
本报告所用数据来源于本局向国家药品监督管理局报送的《药品监督管理2024年定期统计报表制度》中的月报、季度报表及年报表,数据统计时间为2024年1月1日至2024年12月31日。报告分别对药品、医疗器械、化妆品的相关行政受理、审批、监管等情况进行了汇总分析,供药品监管系统参考使用。
截至2024年12月底,全市药品监管行政机构共有编制231名,实际到岗225人,其中:综合部门92人,药品监管64人,化妆品监管21人,医疗器械监管45人,其他3人。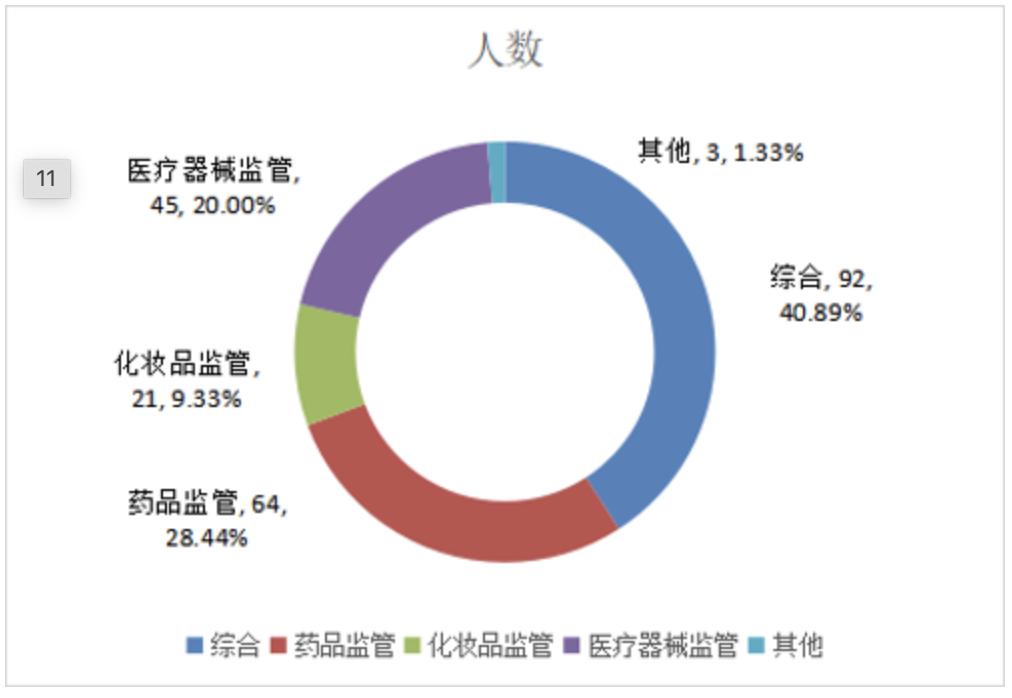
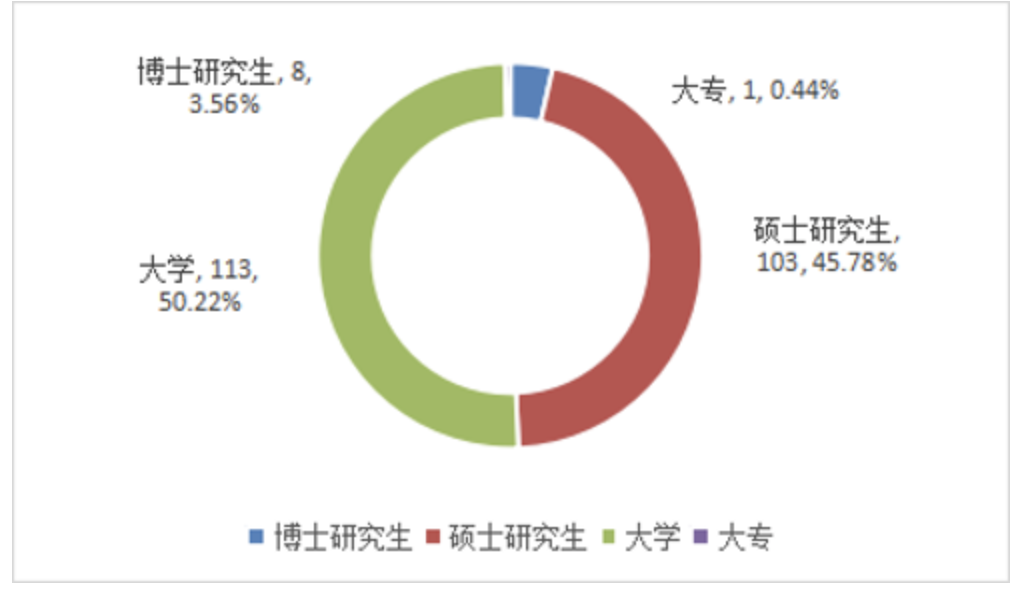
图1 2024年行政机构各部门到岗人员情况 单位:人从学历看,大学及以上学历占99.55%。博士研究生8人,硕士研究生103人,大学113人,大专1人。图2 2024年行政机构到岗人员学历情况 单位:人从专业结构看,药学、医学、医疗器械、食品、公共卫生、法律、管理与经济专业占75.55%。药学专业43人,医学专业33人,医疗器械及相关专业8人、食品、公共卫生及相关专业16人,法律专业25人,化学专业15人,管理与经济专业45人,信息技术相关专业15人,其他专业25人。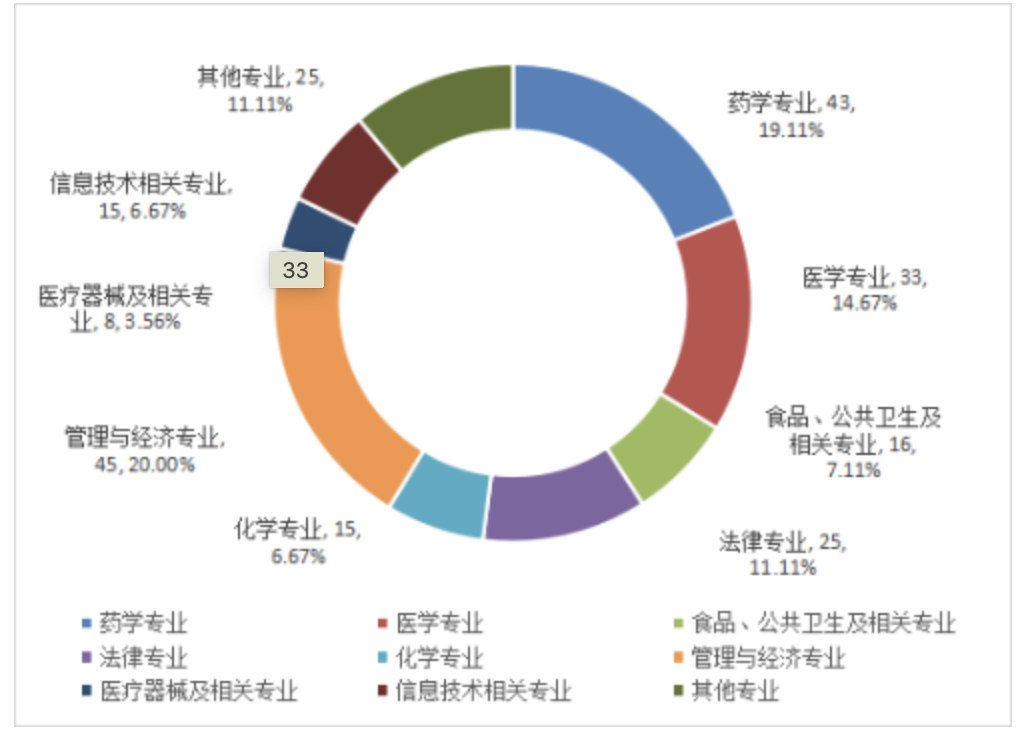
从年龄结构看,45岁以下人员占65.77%。35岁以下30人,36-40岁41人,41-45岁77人,46-50岁30人,51-54岁27人,55岁及以上20人。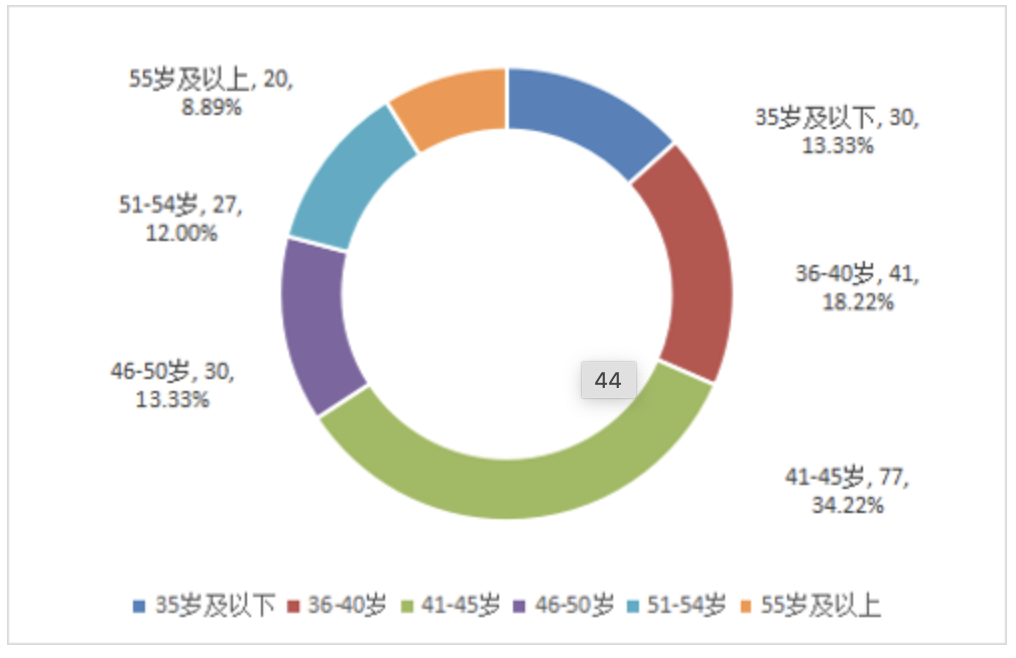
图4 2024年行政机构到岗人员年龄情况 单位:人2024年药品监管系统行政机构领导班子应配备职数26名,现有领导28人。从学历看,全部为大学及以上学历。其中:博士研究生1人,硕士研究生16人,大学11人。从专业结构看,药学专业7人,医学专业4人,法律专业3人,化学专业2人,管理与经济专业8人,医疗器械及相关专业1人,其他专业1人。从年龄结构看, 41-45岁7人,46-50岁8人,51-54岁8人,55岁及以上5人。截至2024年12月底,各区药品监管行政机构共有编制1456名,实际到岗1399人,其中:药品监管824人,化妆品监管273人,医疗器械监管302人。截至2024年12月底,全市药品监管事业单位共有编制808名,实际到岗834人。到岗人员中,具有专业技术职称的占总人数的67.99%,其中:具有高级职称人员(170人)占职称人数比29.98%,中级职称人员(150人)占职称人数比26.46%,初级职称人员(247人)占职称人数比43.56%。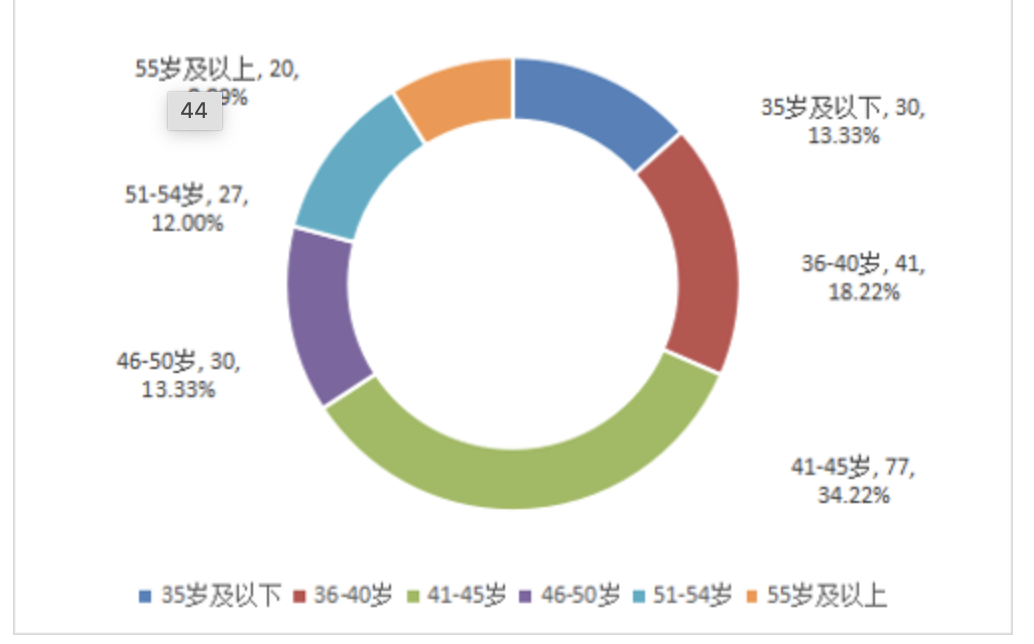
图5 2024年事业单位到岗人员职称情况 单位:人从学历看,大学及以上学历人员占总人数的97.36%。博士研究生71人,硕士研究生316人,大学425人,大专20人,中专1人,高中及以下1人。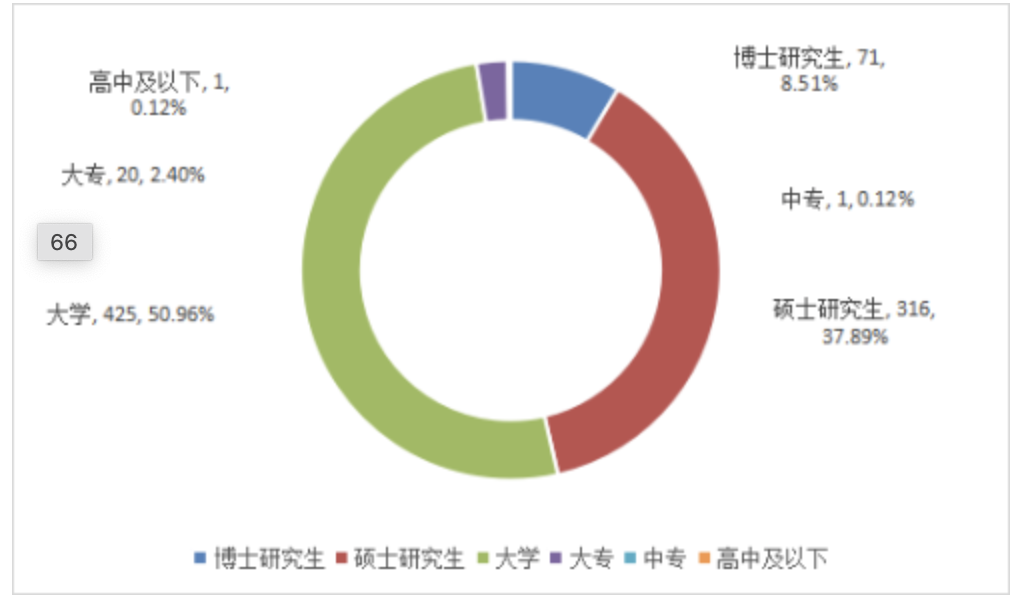
图6 2024年事业单位到岗人员学历情况 单位:人从专业结构看,药学专业人员比例最高,占25.06%。药学专业209人,医学专业78人,食品、公共卫生及相关专业29人,法律专业20人,化学专业66人,管理与经济专业97人,医疗器械及相关专业139人,信息技术及相关专业36人,其他专业160人。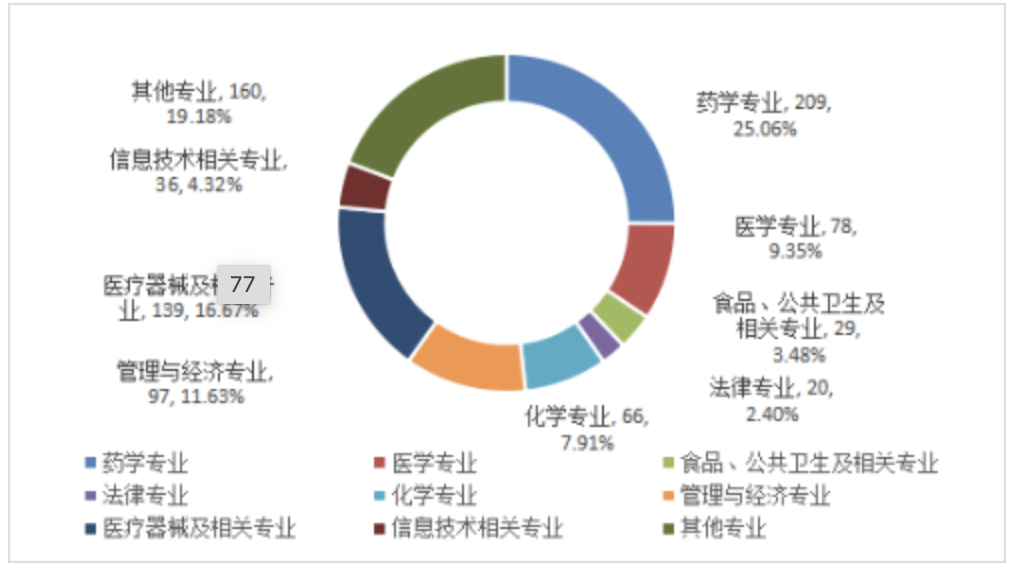
图7 2024年事业单位到岗人员专业情况 单位:人从年龄结构看,45岁以下人员比例为78.42%。35岁以下308人,36-40岁175人,41-45岁171人,46-50岁94人,51-54岁49人,55岁及以上37人。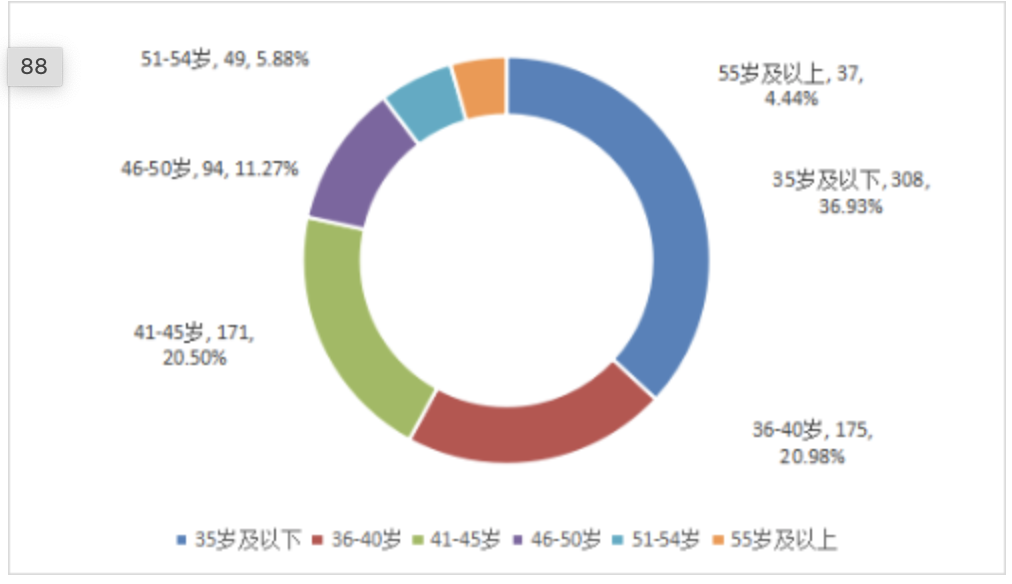
图8 2024年事业单位到岗人员年龄情况 单位:人2024年北京市药品监管系统科技经费总计677.63万元,其中科技项目经费677.63万元,科技项目总计128项,科技成果评价17项。2024年全年受理行政复议案件245件。其中:受理对下级机关进行的行政复议0件,受理被同级政府审理的行政复议245件。受理的复议案件中,药品案件58件,医疗器械案件101件,化妆品案件86件。在复议案件中,中止复议案件0件,申请人撤回终止复议案件80件。2024年共对127件案件作出复议决定。其中:对下级机关的复议作出决定0件,被同级政府审理的复议作出决定127件。127件被同级政府审理的复议决定情况如下:驳回复议申请48件,维持53件,确认违法5件,撤销、部分撤销17件,变更2件,责令限期履行职责2件。2024年法院共受理药品监管行政诉讼案件31件,药品案件10件,医疗器械案件10件,化妆品案件11件。从判决结果看,一审判决14件,其中:驳回诉讼请求9件,确认违法3件,其他2件。二审判决2件,全部维持原判。2024年市局共批准国产药品再注册申请522件,其中:中药天然药物169件、化学药品318件、生物制品35件。2024年市局共批准药品上市后变更备案申请审批事项1070件,未批准0件。2024年全市具有药品GSP检查员资格为330人,其中可从事检查工作的检查员330人。从学历看,大学及以上学历占67.27%。其中:硕士研究生及以上45人,大学177人,大专108人。从职称看,初级职称人数占总职称人数的56.67%,其中:高级职称25人,中级职称118人,初级职称187人。从所在单位看,其他单位占总人数的50.30%,其中:行政机关129人,检查机构35人,其他单位166人。从培训情况看,检查员初次培训9人次,继续培训330人次。截至2024年12月底,全市共检查3860人次。截至2024年12月底,全市共有《药品经营许可证》持证企业5477家。其中:法人批发218家,非法人批发12家,零售连锁企业89家,零售连锁门店2737家,零售药店2421家。2024年全市各级监管机构共检查药品生产企业1546家次,其中:含疫苗生产企业387家次,麻药、精神药品、易制毒化学品生产企业119家次 ,含血液制品、注册剂等高风险品种的生产企业233家次。出动检查人次3943人次,发现违规的生产企业0家。2024年全市各级监管机构共检查批发企业1331家次,发现违法违规的批发经营企业1家次,完成整改6家次。检查零售企业26087家次,发现违法违规的零售经营企业130家次,其中:严重违反GSP的零售企业0家次,涉及假药的零售企业3家次,无照经营0家次,其他零售企业126家次,完成整改124家次,立案查处的经营零售企业128家次。2024年全市共抽验药品4069批次,不合格批次1批。2024年全市共查处药品案件374件。查处药品案件货值金额932.35万元;罚款654.2万元,没收违法所得金额428.79万元。从案值划分来看,以案值10万元以下的案件为主有368件,占药品案件总数的98.40%。案值在10万-20万元的案件共有2件;案值在20万-50万元的案件有2件;案值在50万-1000万元的案件共有2件;案值在1000万元-1亿的案件共有0件。2024年来源于日常监管和专项检查的案件204件,占药品案件总数的54.55%;来源于投诉举报的案件102件,占总数的27.27%;来源于其他部门通报的案件37件,占总数的9.89%;来源于执法检验的案件13件,占总数的3.48%;来源于其他的案件10件,占总数的2.67%;来源于监督抽验的案件8件,占总数的2.14%。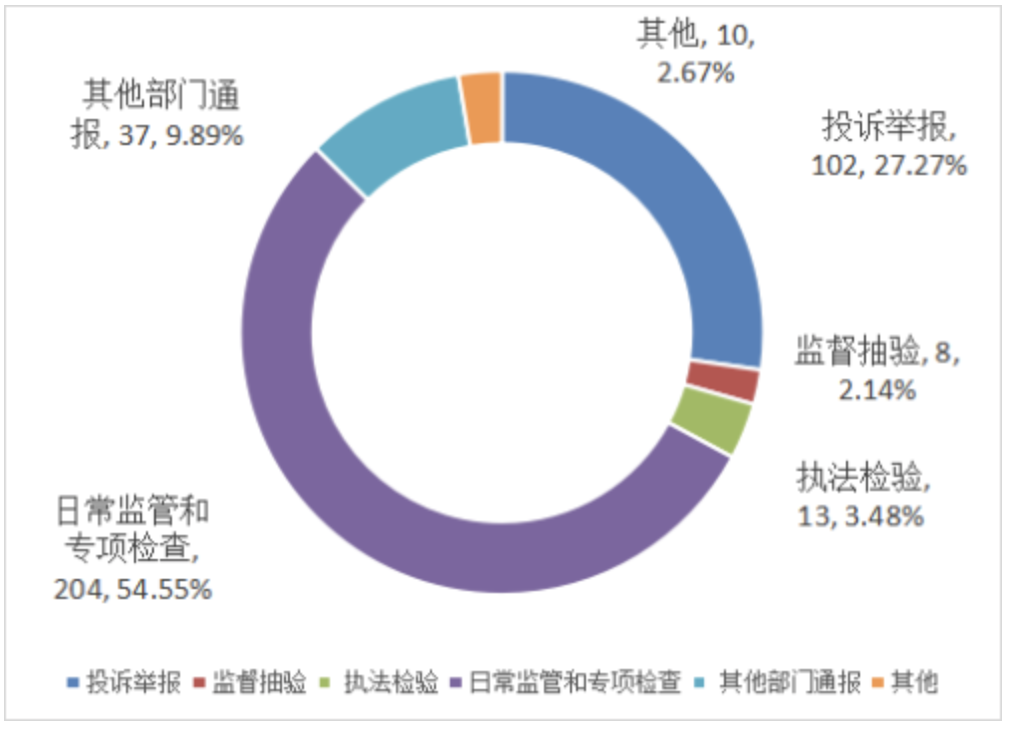
药品案件的违法环节以经营环节为主(308件),占到药品案件总数的82.35%,居第一位;违法环节为医疗机构的案件(43件)占药品案件总数的11.50%,居第二位;违法环节为生产环节的案件(13件)占药品案件总数的3.48%,居第三位;违法环节为其他的案件(10件)占药品案件总数的2.67%,居第四位。2024年生产销售假药案件立案2件,行政处罚案件信息公开0件,生产销售假冒化妆品案件立案3件,行政处罚案件信息公开0件。截至2024年12月底,全市共有互联网药品信息服务机构审批1887家。截至2024年12月底,全市共有麻醉药品定点生产企业4家,其中:含原料药生产企业2家, 含制剂生产企业4家。精神药品定点生产企业9家,其中:第一类精神药品定点生产企业1家,第二类精神药品定点生产企业9家。麻醉药品、精神药品定点生产企业10家。药品类易制毒化学品定点生产企业1家。截至2024年12月底,全市共有麻醉药品和第一类精神药品定点经营区域性批发企业3家。第二类精神药品定点经营企业37家,其中:专门从事第二类精神药品批发企业35家;第二类精神药品定点经营零售连锁企业2家。药品类易制毒化学品原料药定点经营企业1家。2024年全市境内第一类医疗器械备案2591件;境内第二类医疗器械首次注册受理746件、批准671件,延续注册受理1105件、批准1117件,许可事项变更受理1801件、批准2097件,登记事项变更备案651件,注/撤销17件。截至2024年12月底,境内第二类医疗器械注册证7476件。截至2024年12月底,全市实有医疗器械生产企业1002家。可生产一类医疗器械企业数量451家,可生产二类医疗器械企业数量664家,可生产三类医疗器械企业数量334家。重点监管企业134家。截至2024年12月底,全市有仅从事第二类医疗器械经营的企业29723家,仅从事第三类医疗器械经营的企业1116家,同时从事第二、三类医疗器械经营的企业13451家,医疗器械批发企业15690家,医疗器械零售企业16423家,医疗器械批零兼营企11449家,从事无菌或植入性医疗器械经营的企业7640家,从事体外诊断试剂(IVD)经营的企业13144家,专门提供医疗器械运输贮存服务的企业39家,从事医疗器械网络销售的企业5823家。2024年全市各级监管机构共检查医疗器械生产企业2178家次,其中检查含一类医疗器械产品的生产企业461家次,要求停产整改3家次;检查含二类医疗器械产品的生产企业922家次,要求停产整改8家次;检查含三类医疗器械产品的生产企业832家次,要求停产整改10家次;检查含体外诊断试剂医疗器械产品的生产企业327家次,要求停产整改3家次。检查国家重点监管企业328家次。全面检查高风险含无菌或植入性医疗器械生产企业387家次,要求停产整改4家次;检查创新医疗器械生产企业133家次,均通过检查。检查第三类医疗器械的生产企业720家次,要求停产整改6家次。检查委托生产企业注册人制企业168家次,均通过检查;检查受托生产企业160家次,均通过检查。检查国家集中带量采购中选产品生产企业106家次,均通过检查;检查省级和省级联盟集中带量采购中选产品生产企业326家次,要求停产整改1家次。飞行检查医疗器械生产企业232家次,要求停产整改9家次。存在违法违规行为的生产企业11家次,完成整改915家次,立案查处的生产企业2家次。2024年全市各级监管机构共检查医疗器械经营企业、使用单位、医疗器械网络交易服务第三方平台21824家次;飞行检查经营企业530家次;存在违法违规的企业或单位263家次;完成整改的企业或单位265家次,立案查处的企业或单位226家次。其中:检查医疗器械经营企业16684家次,发现存在违法违规行为的经营企业164家次,完成整改166家次,立案查处136家次;检查医疗器械使用单位4969家次,发现存在违法违规行为的使用单位99家次,完成整改98家次,立案查处90家次;检查医疗器械网络交易网服务第三方平台171家次,发现存在违法违规行为的平台0家次,完成整改1家次,立案查处0家次。2024年全市共抽验医疗器械企业519家,按环节分,生产环节抽验385批次,不合格6批次;经营环节抽验200批次,不合格6批次;使用环节抽验349批次,不合格7批次。按器械类别分,一类医疗器械抽验10批次,不合格1批次;二类医疗器械抽验587批次,不合格15批次;三类医疗器械抽验349批次,不合格7批次。2024年查处医疗器械案件689件,货值金额4127.24万元,罚款2121.91万元,没收违法所得68.62万元。从案值划分来看,案值5万元以下的案件667件,占医疗器械案件总数的96.80%。案值在5万-20万元案件共有14件,案值在20万-50万元案件共有7件,案值在1000万元-1亿元案件共有1件。2024年医疗器械案件的主要来源是日常监管和专项检查258件(占49.90%),其他部门通报73件(占14.12%)、其他36件(占6.96%)、投诉举报137件(占36.50%)、监督抽验10件(占1.93%)和执法检验3件(占0.58%)。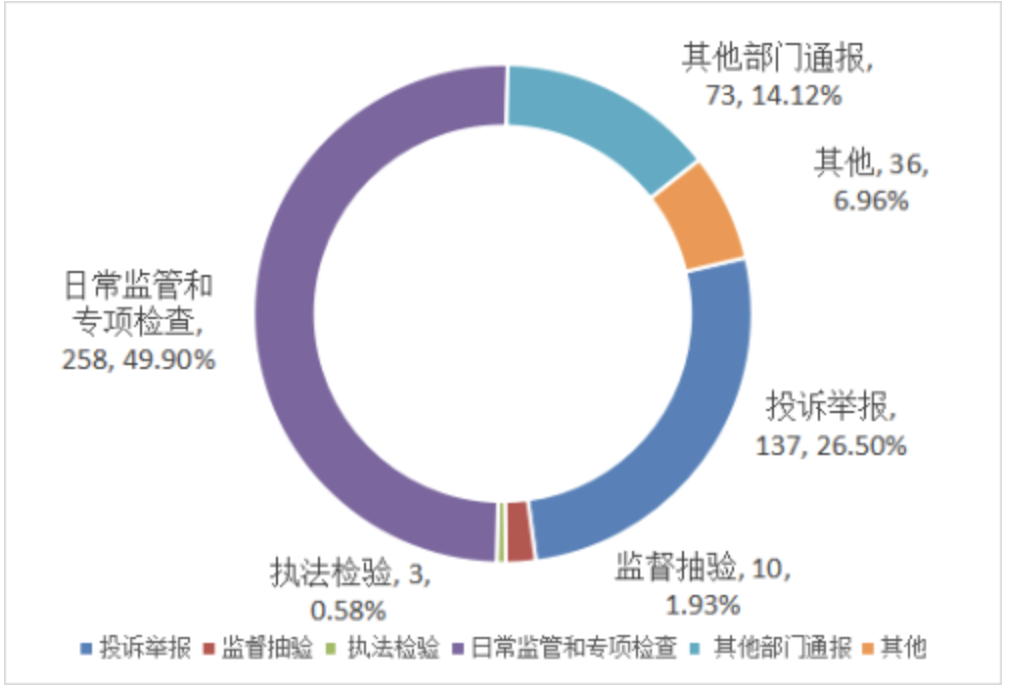
从违法环节来看,违法环节为经营环节的案件共472件,占案件总数的68.50%,居第一位;违法环节为使用单位的案件共177件,占案件总数的25.69%,居第二位;违法环节为生产环节的案件共33件,占案件总数的4.79%,居第三位。2024年生产销售不符合标准的医疗器械案件立案30件,行政处罚案件信息公开8件。2024年全市具有医疗器械GMP检查员资格为306人。从学历看,大学及以上学历占100%,其中:硕士研究生及以上98人,大学197人,大专11人。从职称看,高级职称人数占职称人数的16.01%,其中:高级职称49人,中级职称111人,初级职称146人。从检查经验看,5年以上检查经验占48.69%,其中5年以上检查经验149人,3年到5年检查经验115人,3年以下检查经验42人。从所在单位看,检查机构占31.89%,其中:行政机关107人,检验检测机构82人,审评中心50人,检查机构9人,其他单位58人。截至2024年12月底,全市共检查3772人次。2024年全市各级监管机构共检查化妆品生产企业267家次,出动检查708人次。完成整改企业143家次,飞行检查化妆品生产企业7家次,责令暂停生产企业0家次,完成整改后恢复生产企业0家次。2024年全市具有化妆品检查员资格为542人。从学历看大学及以上学历占100%,其中:硕士研究生及以上69人,大学462人,大专11人。从职称看,初级职称人数占职称人数的50.55%,其中:高级职称68人,中级职称200人,初级职称274人。从检查经验看,5年以上检查经验占40.03%,其中5年以上检查经验217人,3年到5年检查经验246人,3年以下检查经验79人。从所在单位看,行政机关占总检查员人数的28.97%,其中:行政机关157人,检验检测机构15人,审评中心103人,检查机构77人,其他单位190人。截至2024年12月底,全市共检查3420人次。2024年共查处化妆品案件599件,货值金额243.55万元,罚款856.54万元,没收违法所得133.92万元。从案值划分来看,案值在2万元以下的案件585件,占化妆品案件总数的97.66%;案值在2万-20万元的案件12件;20万-50万元的案件1件;50万元-1000万元的案件1件。2024年化妆品案件的主要来源是日常监管和专项检查199件(占33.22%)、投诉举报316件(占52.75%)、其他部门通报27件(占4.51%)、其他18件(占3.01%)、监督抽验31件(占5.18%)、执法检验8件(占1.34%)。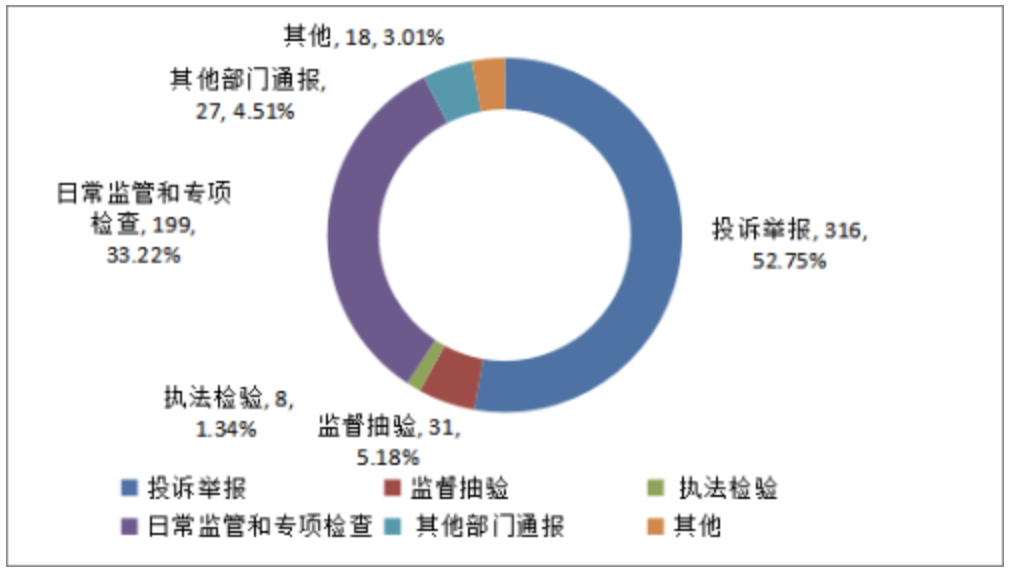
主要违法环节是化妆品经营环节案件567件,占案件总数的94.66%,居第一位;违法环节为其他的案件共18件,占案件总数的3.01%,居第二位;违法环节为生产环节的案件共14件,占案件总数的2.34%,居第三位。2024年生产销售假冒化妆品案件立案3件,行政处罚案件信息公开1件。(二)2024年第四季度北京市药品监督管理统计报告https://yjj.beijing.gov.cn/yjj/zfxxgkzl17/fdzdgknr80/tjxx74/jb29/743554300/index.html
本报告所用数据来源于本局向国家药品监督管理局报送的《药品监督管理2024年定期统计报表制度》中的第四季度报表,数据统计时间为2024年10月1日至2024年12月31日。报告分别对药品、医疗器械、化妆品的相关行政受理、审批、监管等情况进行了汇总分析,供药品监管系统参考使用。截至2024年12月底,全市持有《药品经营许可证》的批发企业319家,其中法人批发218家,非法人批发12家,零售连锁总部89家;全市持有《药品经营许可证》的零售企业5158家,其中零售连锁门店2737家,零售企业2421家,药品网络零售企业2726家。2024年第四季度全市各级监管机构共检查药品生产企业326家次,出动检查871人次,本期未发现违法违规生产企业。2024年第四季度全市各级监管机构共检查药品批发企业、零售连锁企业总部、药品网络交易服务第三方平台289家次,未发现违法违规的企业。检查药品零售经营企业、使用单位7261家次,发现违法违规的经营企业、使用单位58家次,完成整改的经营企业、使用单位56家次,立案查处企业、单位59家次。2024年第四季度本市共抽检药品44批次,有0批次不合格。2024年第四季度全市共查处药品案件86件。查处药品案件货值金额684.12万元,罚款金额82.99万元。从货值划分来看,以货值10万元以下的案件为主,货值10万元以下的案件共84件,占药品案件总数的97.68%;货值20万-50万的案件1件,占药品案件总数的1.16%;货值50万-1000万的案件1件,占药品案件总数的1.16%。2024年第四季度来源于日常监管和专项检查的案件59件(占68.61%)、来源于投诉举报的案件17件(占19.77%)、来源于执法检验的案件1件(占1.16%)、来源于其他部门通报的案件5件(占5.81%)、来源于监督抽验的案件0件(占0.00%)、来源于其他的案件4件(占4.65%)。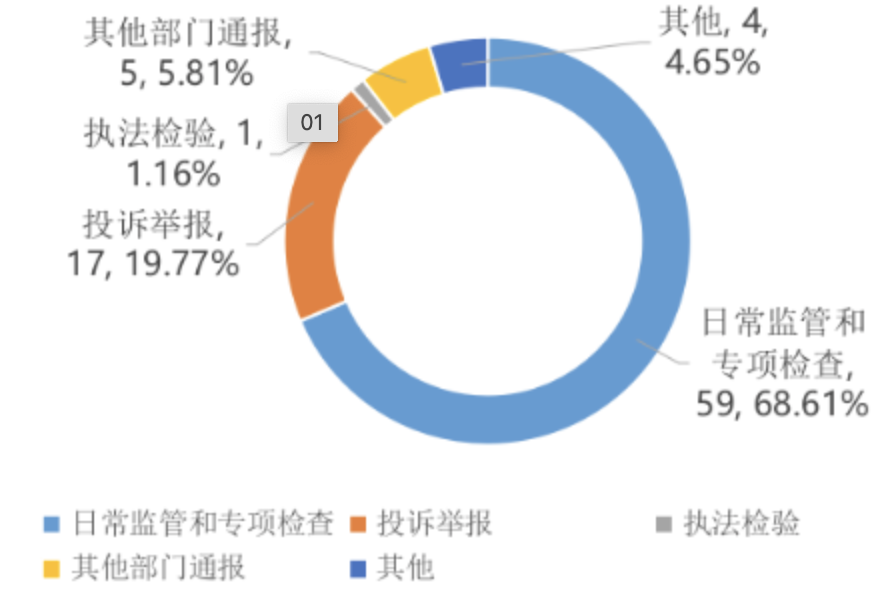
图1 2024年第四季度药品案件来源情况 单位:件药品案件的主要违法环节以经营环节为主,共71件,占案件总数的82.56%;主要违法环节为医疗机构的案件12件,占案件总数的13.95%;主要违法环节为生产环节的案件1件,占案件总数的1.16%;主要违法环节为其他的案件2件,占案件总数的2.33%。2024年第四季度生产销售假药案件立案0件,生产销售劣药案件立案6件,行政处罚案件信息公开31件。截止至2024年12月底,全市药监局互联网药品信息服务机构审批期末实有1887家。药品网络交易服务第三方平台期末实有35家。2024年第四季度境内第一类医疗器械新增备案107件;境内第二类医疗器械首次注册受理260件、批准238件,延续注册受理176件、批准241件,变更注册受理259件、批准350件,登记事项变更备案120件,注/撤销3件。截至2024年12月底,境内第一类医疗器械实有备案2591件,境内第二类医疗器械注册证实有7476件。截止至2024年12月底,全市实有医疗器械生产企业1002家。一类医疗器械产品生产备案凭证451张,仅生产二类医疗器械产品生产许可证468张,仅生产三类医疗器械产品生产许可证138张,同时生产二、三类医疗器械产品生产许可证196张。可生产一类医疗器械企业451家,可生产二类医疗器械企业664家,可生产三类医疗器械企业334家。截止至2024年12月底,全市有仅从事第二类医疗器械经营的企业29723家,仅从事第三类医疗器械经营的企业1116家,同时从事第二、三类医疗器械经营的企业13451家。提供医疗器械网络交易服务第三方平台服务的企业62家。2024年第四季度,全市各级监管机构共检查医疗器械生产企业588家次。全面检查高风险含无菌医疗器械生产企业88家次;检查含植入性医疗器械生产企业53家次;检查创新医疗器械生产企业36家次;检查第三类医疗器械生产企业181家次。飞行检查医疗器械生产企业63家次,停产整改0家次。2024年第四季度全市各级监管机构共检查医疗器械经营企业、使用单位、医疗器械网络交易服务第三方平台5406家次;飞行检查经营企业132家次;存在违法违规的企业或单位106家次;完成整改的企业或单位109家次。2024年第四季度本市共抽检医疗器械254批次,1批次不合格。按类别分,一类医疗器械抽检3批次(其中1批次不合格),二类医疗器械抽检197批次,三类医疗器械抽检54批次。2024年第四季度查处医疗器械案件182件,货值金额3703.93万元,罚款金额274.14万元。从货值划分来看,以货值5万元以下的案件为主,货值在5万元以下的案件有178件,占医疗器械案件总数的97.80%;货值5万—20万元的案件有2件,占医疗器械案件总数的1.10%;货值20万—50万元的案件有1件,占医疗器械案件总数的0.55%;货值1000万—1亿元的案件有1件,占医疗器械案件总数的0.55%。2024年第四季度医疗器械案件的主要来源是日常监管和专项检查94件(占51.65%)、投诉举报41件(占22.52%)、其他部门通报24件(占13.19%)、其他13件(占7.14%)、监督抽验8件(占4.4%)、执法检验2件(占1.1%)。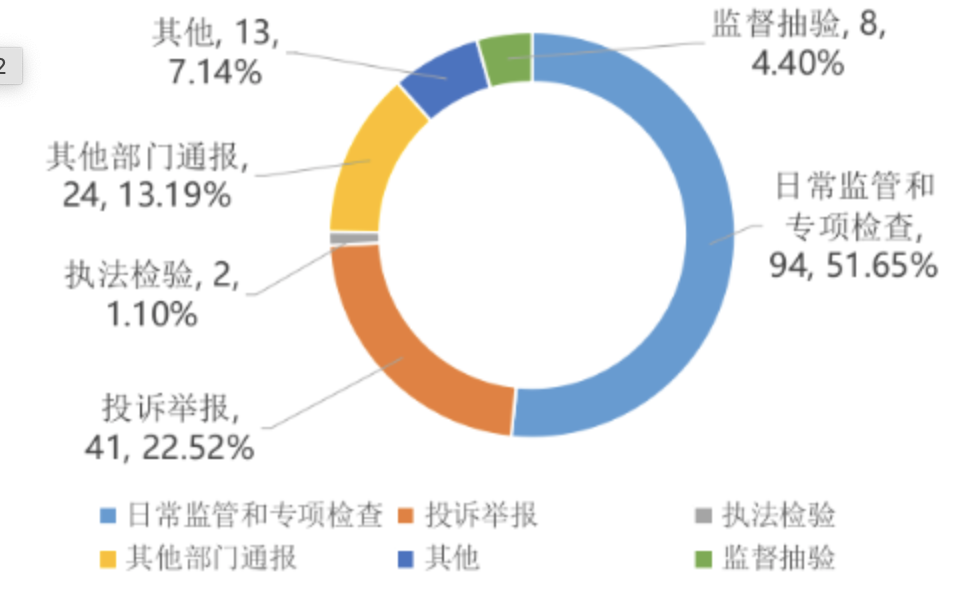
图2 2024年第四季度医疗器械案件来源情况 单位:件从主要违法环节来看,查处主要违法环节为经营环节的案件共125件,占案件总数的68.69%;主要违法环节为使用单位的案件41件,占案件总数的22.52%;主要违法环节为生产环节的案件15件,占案件总数的8.24%;主要违法环节为其他的案件1件,占案件总数的0.55%。2024年第四季度生产销售不符合标准的医疗器械案件立案4件,行政处罚案件信息公开5件。2024年第四季度全市各级监管机构共检查化妆品生产企业36家次,出动检查88人次,完成整改的企业28家次,飞行检查化妆品生产企业0家次。2024年第四季度共查处化妆品案件115件,货值金额19.30万元,罚款金额44.15万元。从货值划分来看,以货值2万元以下的案件为主,货值在2万元以下的案件有111件,占化妆品案件总数的96.52%;货值在2万—20万元的案件有4件,占化妆品案件总数的3.48%。2024年第四季度化妆品案件的主要来源是日常监管和专项检查58件(占50.43%)、投诉举报39件(占33.91%)、其他部门通报8件(占6.96%)、监督抽验4件(占3.48%)、其他4件(占3.48%)、执法检验2件(占1.74%)。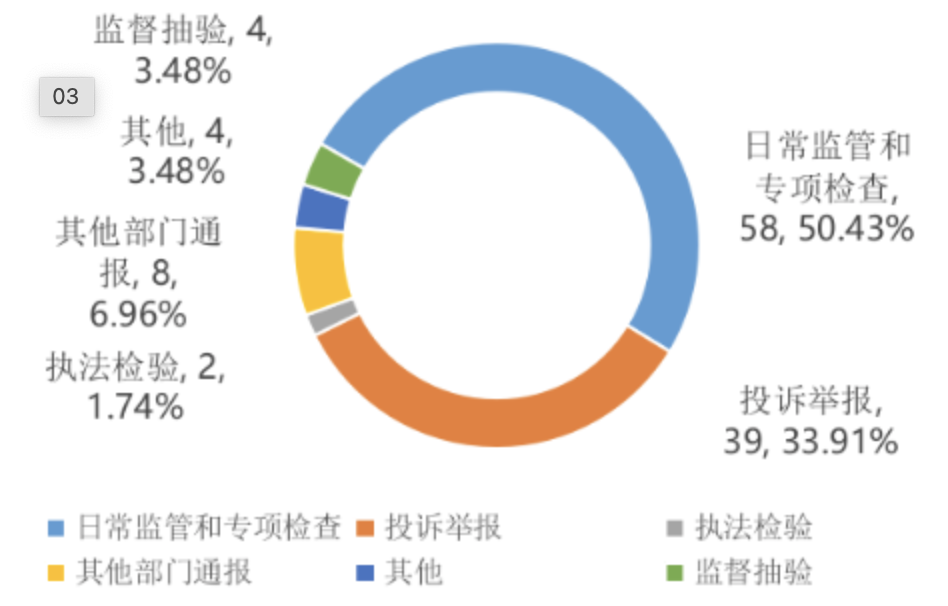
图3 2024年第四季度化妆品案件来源情况 单位:件主要违法环节是经营环节的案件共103件,占案件总数的89.56%;主要违法环节是生产环节的案件共6件,占案件总数的5.22%;其他案件6件,占案件总数的5.22%。2024年第四季度本市共抽检化妆品3批次,不符合规定22批次。按类别分,特殊化妆品抽检2批次,不符合规定13批次;普通化妆品抽验抽检1批次,不符合规定9批次;儿童化妆品抽检0批次。2024年第四季度生产销售假冒化妆品案件立案0件,行政处罚案件信息公开0件。(一)广东省药品监督管理局关于印发《广东省药品监督管理局药品监督管理行政处罚裁量适用规则实施细则》的通知http://mpa.gd.gov.cn/zwgk/gzwj/content/post_4675338.html
各地级以上市市场监督管理局,省药品监管局机关各处室、各药品稽查办公室,有关直属事业单位:为规范广东省各级人民政府承担药品监督管理职责的部门行使行政处罚裁量权,保障公民、法人和其他组织的合法权益,广东省药品监督管理局制定《广东省药品监督管理局药品监督管理行政处罚裁量适用规则实施细则》,经广东省药品监督管理局局务会审议通过,并经广东省司法厅审查通过。现予印发,请遵照执行。第一条 为规范广东省各级人民政府承担药品监督管理职责的部门(以下称药品监督管理部门)行使行政处罚裁量权,保障公民、法人和其他组织的合法权益,细化《药品监督管理行政处罚裁量适用规则》(以下简称《规则》),结合本省实际,制定本实施细则。第二条 全省各级药品监督管理部门办理药品、医疗器械和化妆品违法案件,行使行政处罚裁量权,适用本实施细则。第三条 本实施细则是对《规则》部分条款的细化量化,《规则》中已有明确规定的,本实施细则不再重复。法律、法规、规章以及国家药品监督管理局规范性文件对行政处罚裁量权适用规则另有规定的,从其规定。第四条 行使行政处罚裁量权时,应当坚持合法裁量、程序正当、过罚相当、公平公正、处罚和教育相结合的原则,依据违法事实、性质、情节、社会危害程度和当事人主客观情况等因素,结合本地区经济社会发展状况、药品产业高质量发展和药品安全风险防控需要等情况,对案件进行综合裁量。第五条 行使行政处罚裁量权,应当根据具体案情综合考虑下列情形:本实施细则所规定的各裁量阶次可以考量的因素,非决定行政处罚所适用裁量阶次的唯一因素,不能仅依据单一因素就决定行政处罚所适用的裁量阶次。第六条 当事人的主观过错程度分为无主观过错、主观过失、主观故意。(一)当事人已尽到合理的注意义务和履行法定义务,违法行为仍然发生的,认定为无主观过错,是不予处罚情形可以考量的因素。包括但不限于《规则》第十四、十五条规定。无主观过错的举证责任由当事人承担。法律、行政法规另有规定的,从其规定。(二)当事人明知或应知其需履行的法定义务却未履行的认定为具有主观过失。包括但不限于药品零售企业未按储存要求储存药品,医疗器械经营企业购进医疗器械时未索取注册备案资料。(三)当事人出于获利或避免损失的目的主动实施的认定为主观故意。包括但不限于逃避、抗拒监督检查,转移、隐匿、销毁涉案产品进销存记录,通过非法渠道购进产品价格明显低于市场价格的药品。(一)当事人五年以内第一次实施同一性质违法行为的,是不予处罚情形可以考量的因素;(二)当事人在两年以内实施违法行为三次以上的,或者一年以内因同一性质违法行为受过行政处罚的,是从重情形可以考量的因素;(三)当事人两年以内实施同一性质违法行为三次以上的,是情节严重情形可以考量的因素。第八条 有下列情形之一的,可以认定为违法行为轻微,是不予处罚、减轻或者从轻处罚情形可以考量的因素:(一)没有违法所得或者违法所得较小,货值金额较小;有下列情形之一的,可以认定为违法行为的具体方法或手段恶劣,是从重或者情节严重情形可以考量的因素:(三)通过不履行法定记录义务等隐蔽手段规避监管的;(四)其他可以认定为违法行为的具体方法或手段恶劣的情形。第九条 违法行为轻微并及时改正,有下列情形之一的,可以认定为没有造成危害后果,是不予处罚情形可以考量的因素:(一)经询问当事人,并查询投诉举报系统、不良反应监测系统等方式,未发现相关危害后果的;有下列情形之一的,可以认定为危害后果轻微,是减轻或者从轻处罚情形可以考量的因素:(四)对危害后果采取主动补救、赔偿、履行等义务,及时消除社会影响的;危害后果严重,包括造成人员伤害后果及社会危害程度严重的情形,是从重或情节严重情形可以考量的因素。造成人员伤害后果是指轻伤以上伤害,轻度以上残疾,器官组织损伤导致功能障碍及其他严重危害人体健康的情形。违法行为被新闻媒体、网络曝光造成较大社会影响的,认定为产生严重社会影响,是情节严重情形可以考量的因素。第十条 当事人主动实施召回涉案产品相关措施的,可以认定为已采取补救措施。当事人主动实施召回并有以下情形之一的,可以认定已采取补救措施并消除危害后果:(二)召回大部分涉案产品且有充分证据证明市场上已无涉案产品流通的;(三)其他可以认定已采取补救措施并消除危害后果的情形。主动实施召回,是指当事人在药品监督管理部门尚未立案调查且责令召回之前,已实施召回行为。第十一条 当事人有下列情形之一的,可以依法从轻行政处罚:(一)具有《规则》第十一条(二)或者(五)情形之一的;(七)涉案产品数量较少且货值金额或者违法所得较小;第十二条 当事人有下列情形之一的,可以依法减轻行政处罚:(一)具有《规则》第十一条(一)、(三)、(四)、(六)项等的情形之一;(二)具有《规则》第十五条(一)、(二)、(三)项等的情形之一;(三)具有本实施细则相关规定两项或两项以上可以从轻情形的;减轻行政处罚足以起到惩戒、教育作用,或者从轻行政处罚按照法理情衡量,仍然显失公正的,或明显过罚不当的,可以作出减轻行政处罚的决定。第十三条 除《规则》第九条规定的情形外,当事人有下列情形之一的,可以依法从重行政处罚:(一)造成较大财产损失的,或者造成恶劣影响的,或者引发群体性事件的;(四)生产使用的原料、辅料或者直接接触产品的包装材料来源不合法或者不明的;(五)在药品监督管理部门采取暂停生产、销售等风险控制措施期间,继续生产、销售的;第十四条 除《规则》第十六条规定的情形外,当事人有下列情形之一的,按照“情节严重”给予行政处罚:(三)当事人两年以内实施同一性质违法行为三次以上的;(四)具有《规则》或本实施细则可以从重或应当从重有关规定中两项以上情形的;当事人有《化妆品生产经营监督管理办法》第六十一条第一款规定情形的,应当按照化妆品监督管理法规、规章规定的“情节严重”给予行政处罚。第十五条 给予当事人减轻处罚时,依据法律、法规、规章,《规则》、本实施细则和相关裁量基准中有关减轻处罚规定的情形数量,确定减轻处罚罚款的档次:(一)当事人具有一项应当或可以减轻情形的,可以适用减轻处罚第一档次,罚款超过法定最低处罚金额的70%;(二)当事人具有两项应当或者可以减轻情形,可以适用减轻处罚第二档次,罚款在法定最低处罚金额的30%以上70%以下;(三)当事人具有三项以上应当或者可以减轻情形,可以适用减轻处罚第三档次,罚款低于法定最低处罚金额的30%。按照第十二条第一款第(三)项减轻规则,两项从轻因素可视为一项减轻因素,且不同因素可叠加计算。第十六条 对当事人处以减轻处罚时,选择在法定最低罚款限值以下确定罚款数额、适用更轻的处罚种类、对减轻所适用的档次进行调整或者属于应当并处而不并处情形的,应当经过部门负责人集体讨论予以决定。第十七条 本实施细则所称违法行为持续时间较短、违法区域范围较小、涉案产品数量较少、货值金额较小或者违法所得较小等具体标准由市、县级药品监督管理部门结合工作实际予以合理细化、量化。第十八条 本规则中“以上”“以下”“以内”包括本数,“超过”“低于”不包括本数。第十九条 根据药品、医疗器械和化妆品现行监管常用法律法规的规定,广东省药品监督管理局制订药品、医疗器械和化妆品行政处罚自由裁量权基准作为本实施细则的附件和补充参考。第二十条 本实施细则由广东省药品监督管理局负责解释。本规则自2025年3月1日起实施,有效期五年,原《广东省药品监督管理局规范行政处罚自由裁量权适用规则》(粤药监规执法〔2021〕1号)同时废止。附件1 广东省药品监督管理局药品行政处罚自由裁量权基准.xls附件2 广东省药品监督管理局医疗器械行政处罚自由裁量权基准.xls附件3 广东省药品监督管理局化妆品行政处罚自由裁量权基准.xls(二)《广东省药品监督管理局药品监督管理行政处罚裁量适用规则实施细则》解读http://mpa.gd.gov.cn/zwgk/gzwj/content/post_4676862.html
《中华人民共和国行政处罚法》《中华人民共和国药品管理法》《中华人民共和国疫苗管理法》《医疗器械监督管理条例》《化妆品监督管理条例》《广东省化妆品安全条例》《广东省规范行政处罚自由裁量权规定》《药品监督管理行政处罚裁量适用规则》等。《广东省人民政府办公厅关于推进包容审慎监管的指导意见》(粤府办〔2022〕7号)《国务院关于进一步规范和监督罚款设定与实施的指导意见》(国发〔2024〕5号)等。二、《实施细则》与《药品监督管理行政处罚裁量适用规则》及其他法律法规的关系是如何规定的?《实施细则》是对《药品监督管理行政处罚裁量适用规则》(以下简称《规则》)部分条款的细化量化,结合执法实际进行了规定。《规则》中已有明确规定的,本实施细则不再重复。法律、法规、规章以及国家药品监督管理局规范性文件对行政处罚裁量权适用规则另有规定的,从其规定。全省各级药品监督管理部门办理药品、医疗器械和化妆品违法案件,行使行政处罚裁量权,适用本实施细则。四、《实施细则》正文内容与附件基准文件的关系是如何规定的?《实施细则》中正文内容是总原则,适用于基准中规定的所有违法情形,基准文件作为《实施细则》的附件和补充参考,适用于对应法条所规定的违法情形。《实施细则》正文共二十条,有两大部分内容,第一部分是根据《规则》第八条,结合执法实际对各因素进行了具体规定;第二部分是对从轻、减轻、从重和情节严重的情形进行了详细的列举和说明。其中第四、五条规定了综合裁量考虑因素,第六条至第十条是对第三条的细化,重点规定了裁量因素及其认定标准、相关阶次;第十一条至第十四条,则是在《规则》的基础上梳理增加了可以依法减轻处罚、从轻处罚、从重处罚、情节严重的的具体情形;第十五条至第十九条,规定了减轻处罚的计算方式、处罚程序,同时对持续时间等具体标准的制定做出了授权,明确了减轻处罚的程序和新旧制度的衔接,基准文件作为《实施细则》的附件等。六、药品行政处罚自由裁量基准有哪些主要内容及变化?药品行政处罚自由裁量基准对《中华人民共和国药品管理法》《中华人民共和国疫苗管理法》《药品注册管理办法》等法规规章涉及的违法行为进行逐一梳理,结合本省实际情况归纳《规则》《实施细则》及相关法律法规、部门规章规定以外的特殊裁量因素,作为减轻、从轻、从重处罚和情节严重情形的适用条件。对原有的26条裁量基准内容修订为21条:由于相关项目无特殊裁量因素,无需单独列出,删除原基准序号11、15、18、22-26等8个项目;因对不同处罚对象适用的处罚种类和幅度不一,将原基准序号16的项目拆分为15、16项,加以区分;据执法需要,增加补充序号5和21这2项违法行为。七、医疗器械行政处罚自由裁量基准有哪些主要内容及变化?医疗器械行政处罚自由裁量基准对《医疗器械监督管理条例》《医疗器械生产监督管理办法》《医疗器械经营监督管理办法》等10部法规规章涉及的违法行为进行逐一梳理,共梳理归纳出40种不同类型违法行为,及其对应的处罚条款、种类和幅度。着重围绕重点违法行为、高风险产品、自由裁量空间较大的处罚条款、违法主客观因素等方面,对其中13种违法行为,重点从减轻、从轻、从重三个方面列举了43种对应情形。对处罚条款多为改正、警告,拒不改正后,其罚款额也不大等考虑到其本身不具备更多的裁量基础,则在基准中不进行列举,交由执法人员依据国家《规则》及《实施细则》相关条款进行裁量。八、化妆品行政处罚自由裁量基准有哪些主要内容及变化?化妆品行政处罚自由裁量基准对《化妆品监督管理条例》《化妆品生产经营监督管理办法》《广东省化妆品安全条例》等法规规定的行政处罚裁量标准、条件、种类、幅度等进行细化量化,立足于解决基层执法人员办理化妆品行政处罚案件时遇到的问题。本基准一共有16项,共39个违法行为。原有《化妆品监督管理条例》9个处罚项目全部保留,并在原有内容基础上,设定依据增加《化妆品生产经营监督管理办法》《牙膏监督管理办法》等法规相关条款。序号9、11、12、13、14、15、16是新增的7个处罚项目,其中《化妆品注册备案管理办法》2项,《化妆品生产经营监督管理办法》3项,《中华人民共和国电子商务法》《广东省化妆品安全条例》各新增1项。目前的法律法规对减轻和从轻的情形未作具体划分,《中华人民共和国行政处罚法》和《规则》均使用“减轻或从轻”进行表述,但是在实践中,这两个裁量阶次是完全不同的两个阶次,特别是减轻,适用时甚至可以在规定的处罚种类之外选择更轻的处罚种类种的程度,对当事人合法权益的影响也是截然不同的。《实施细则》进一步细化《规则》要求,对可以从轻和可以减轻的情形分别列举,并按照减轻与从轻的内在逻辑关系,制定“具有本实施细则相关规定两项或两项以上可以从轻情形的”可以减轻这一公式,打通两者之间的适用情形,使可以减轻和可以从轻均有法可依。声明:本文系药方舟转载内容,版权归原作者所有,转载目的在于传递更多信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除内容