
2025-03-27 09:15:03来源:药时空浏览量:1068
2025年3月26日,康希诺发布2024年年度报告:公司实现营业收入8.46亿元,同比增长137.01%,主要得益于流脑结合疫苗的市场推广和全球公共卫生事件影响的减弱;公司归属于上市公司股东的净亏损为3.79亿元,亏损较上一年度大幅收窄74.45%,显示出公司在控制成本和提升运营效率方面的努力和成效。
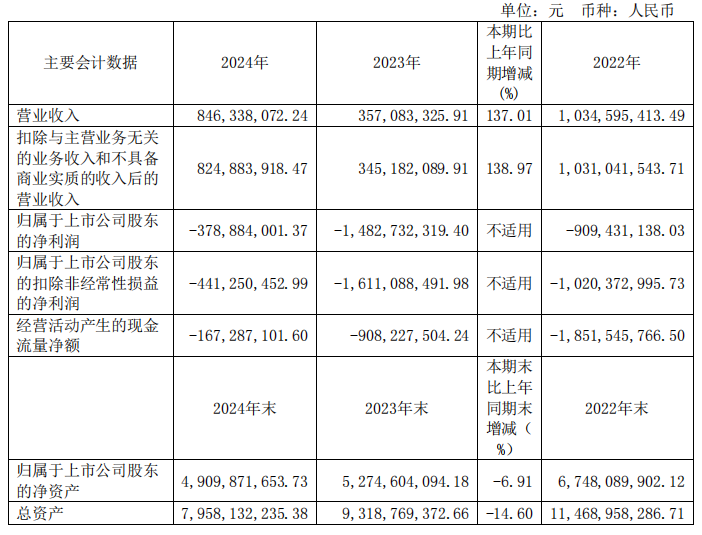
流脑疫苗产品是康希诺主要的商业化产品。随着推广和市场导入,公司的MCV4曼海欣和MCV2美奈喜这两款流脑疫苗产品实现销售收入约7.94亿元,同比增长41.31%。同时,MCV4的药品补充申请已获国家药品监督管理局受理,适用人群年龄范围拟由“3月龄~3周岁(47月龄)儿童”扩大至“3月龄~6周岁(83月龄)儿童”,以期为儿童提供更全面的保护,并进一步提升MCV4曼海欣®的市场渗透率。
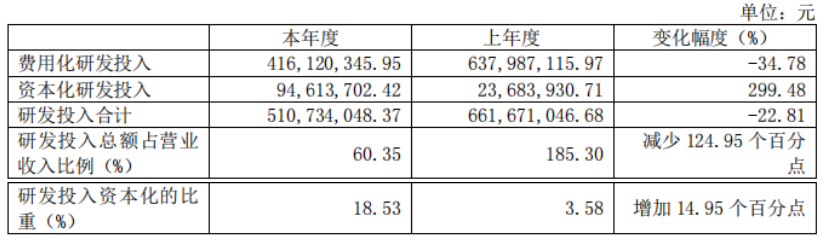
在研发方面,康希诺持续加大投入,全年研发投入达5.11亿元,占营业收入的60.35%,同比减少22.81%。研发投入变化主要系公司研发重心转移,且其他在研产品的研发进展、研发阶段不同所致;报告期内公司将满足相关研发会计政策的13价肺炎结合疫苗PCV13i、婴幼儿组分百白破疫苗DTcP、吸附破伤风疫苗及脑膜炎球菌多糖结合疫苗MCV4曼海欣海外、扩龄研究开发支出予以资本化。
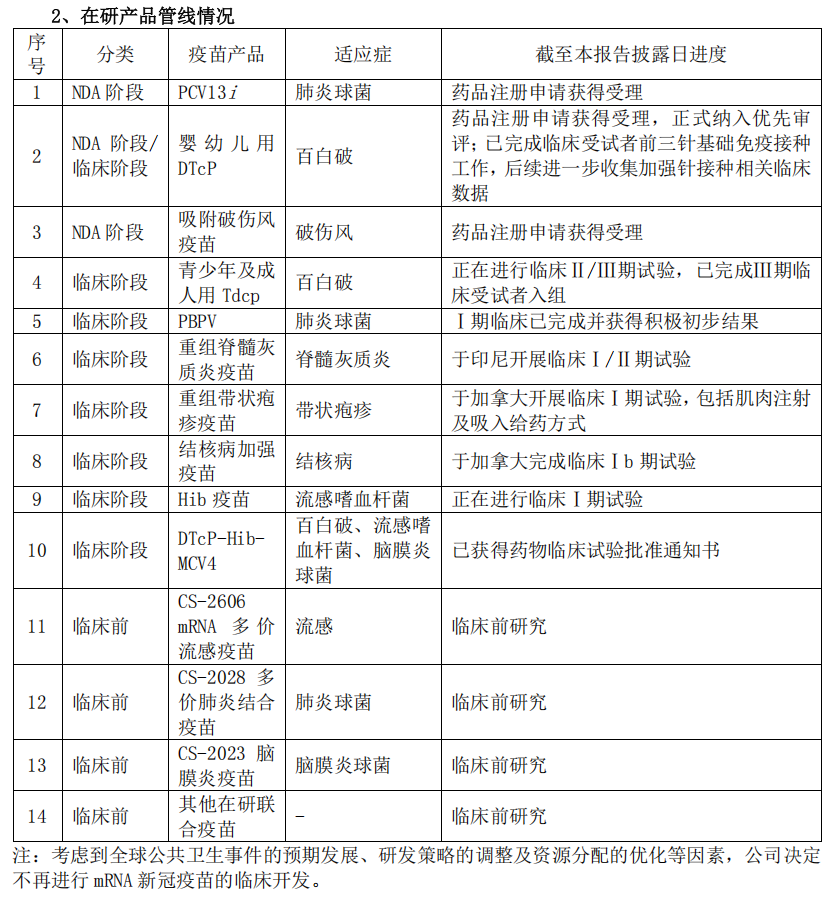
公司构建了五大技术平台,并形成了极具竞争力的产品管线,包括针对预防脑膜炎、肺炎、百白破、新冠肺炎、埃博拉病毒病、带状疱疹、结核病等10余种适应症的多款创新疫苗产品。
13价肺炎结合疫苗PCV13i药品注册申请获受理,目前已完成了临床现场检查及生产现场检查,预期于2025年内获批上市,因与MCV4曼海欣®同样定位为高端自费疫苗,目标消费人群重合,该产品的上市有利于公司丰富商业化产品品种,并提升营销效率。
组分百白破疫苗产品方面,公司的婴幼儿组分百白破疫苗DTcP注册上市许可已获受理,且于2025年2月已被正式纳入优先审评品种;青少年及成人用组分百白破疫苗Tdcp已完成Ⅲ期临床受试者入组。
DTcP-Hib-MCV4联合疫苗已于2025年2月获得药物临床试验批准通知书。同时,Hib疫苗于 2024年11月启动Ⅰ期临床试验并完成首例受试者入组。作为未获批上市的单苗需累积一定的临床数据,以支持未来以组分百白破为基础的联合疫苗的注册申报。
吸附破伤风疫苗已于2025年2月向国家药品监督管理局递交药品注册申请并获得受理。
重组脊髓灰质炎疫苗已于印尼启动于特定年龄婴幼儿中的Ⅰ/Ⅱ期临床试验,并完成Ⅰ期临床首例受试者入组。
重组肺炎球菌蛋白疫苗PBPV获得Ⅰ期临床积极初步结果
重组带状疱疹疫苗于加拿大的Ⅰ期临床正在进行中。
国际化进程方面,公司目前正在开展四价流脑结合疫苗的出海工作,主要以东南亚、中东、北非、南美为目标区域,推动注册和商业化工作。公司也会同步结合未来13价肺炎结合疫苗及组分百白破疫苗组合的海外开拓目标,以公司丰富的产品管线为切入点,与合作方建立长期良好的战略合作关系,持续推进公司国际化进程。
同时,公司也会视产品定位及研发进度,以WHO PQ认证为方向进行前期准备和筹划工作,探索国际组织采购产品的可行性;对于全球创新类产品,也会积极探讨于发达国家准入的可行性。
参考资料:康希诺2024年年度报告.
声明:本文系药方舟转载内容,版权归原作者所有,转载目的在于传递更多信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除内容