2025-11-28 10:27:16来源:鼎泰集团TriApex浏览量:867
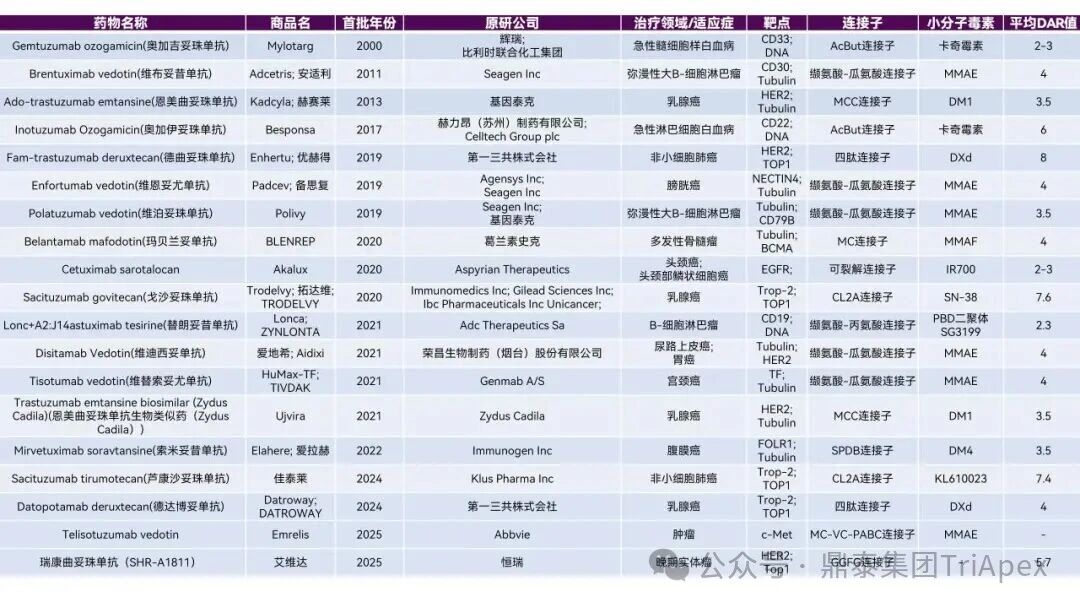
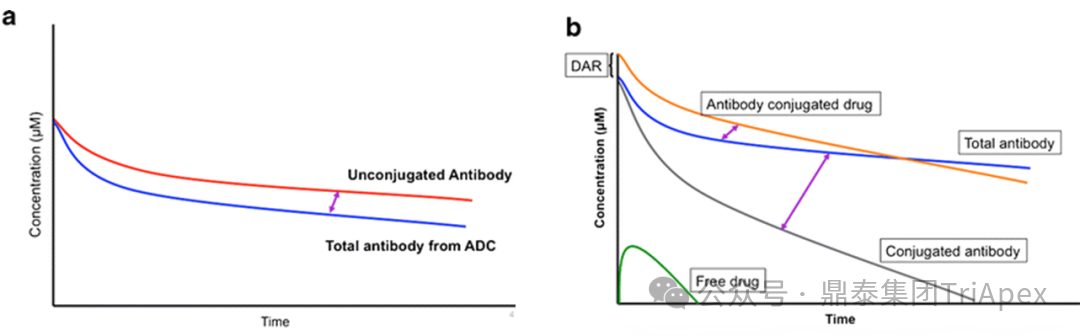
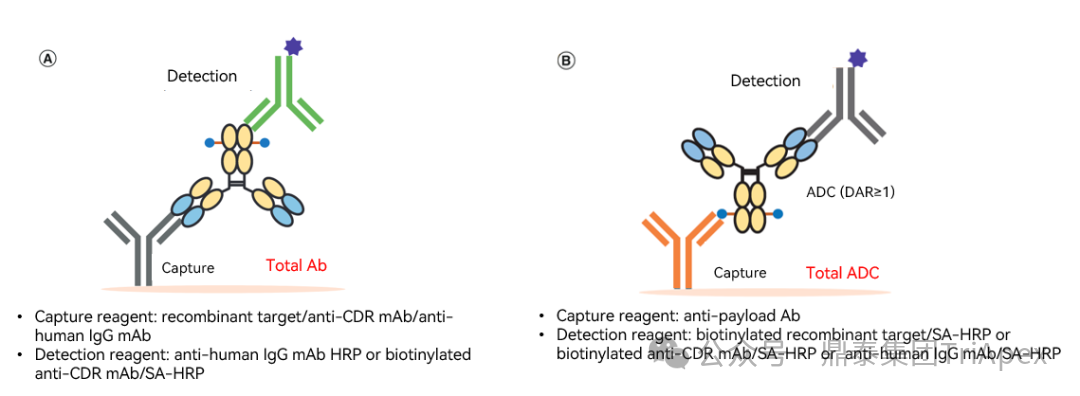
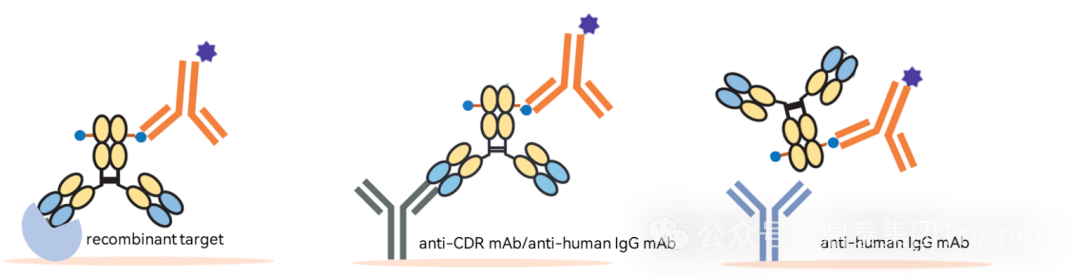
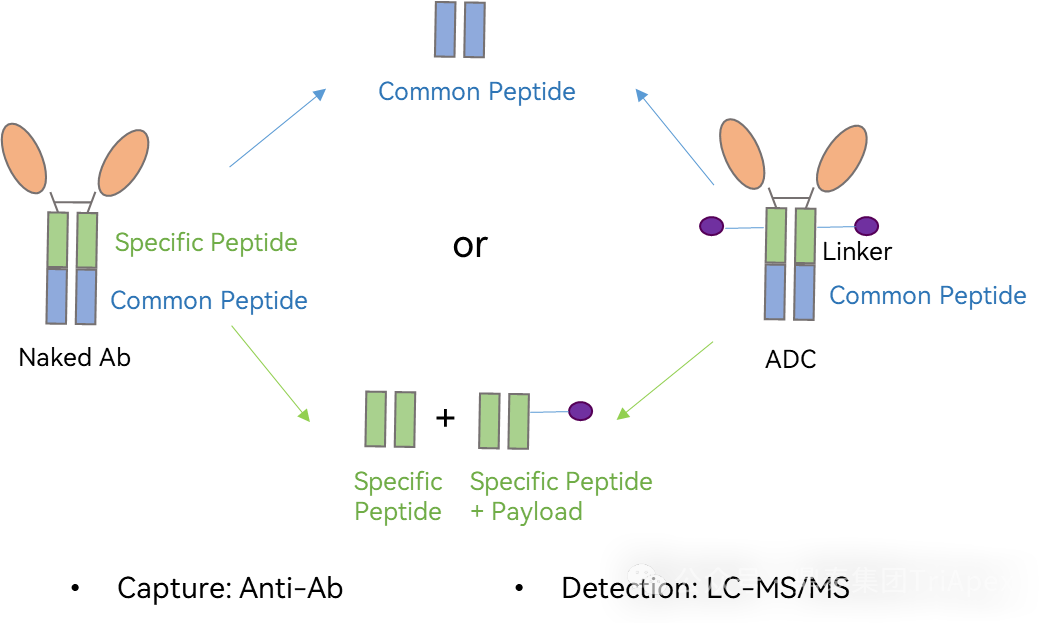
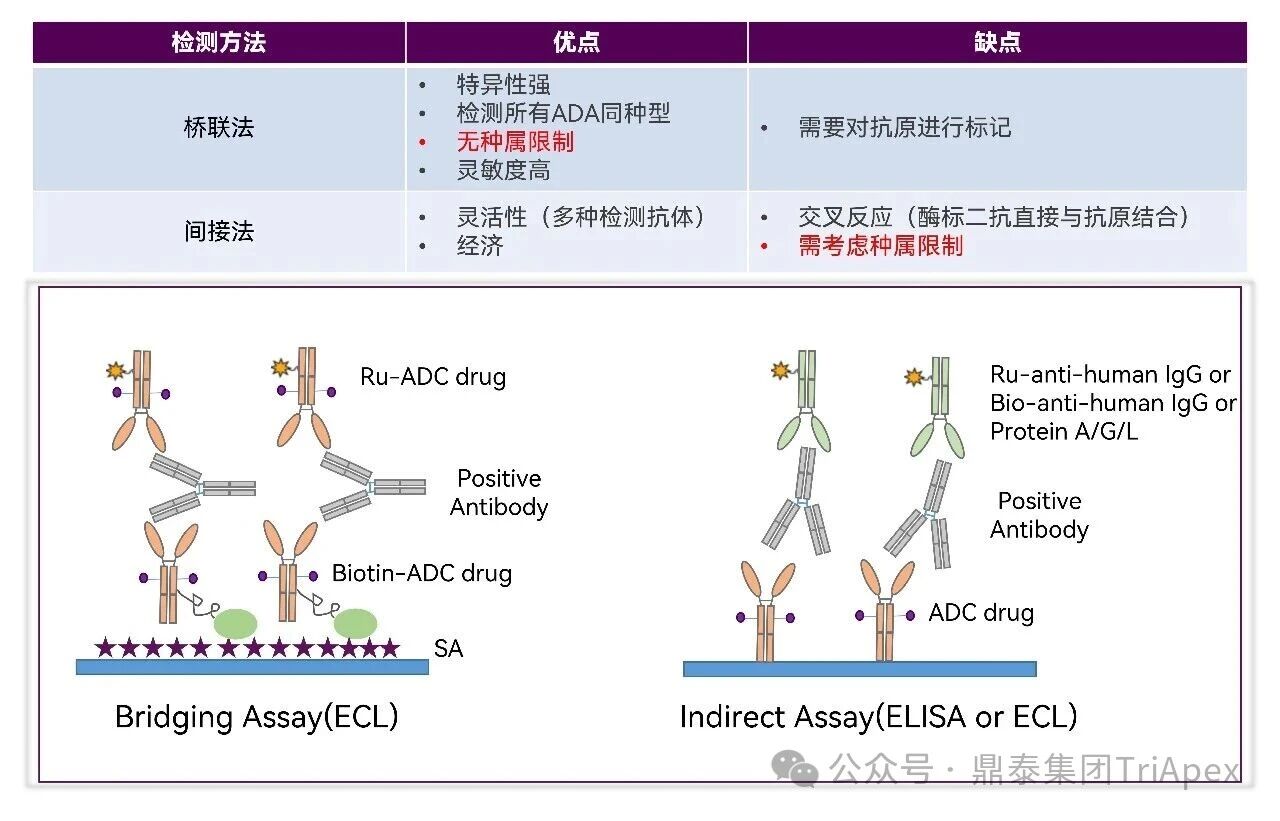
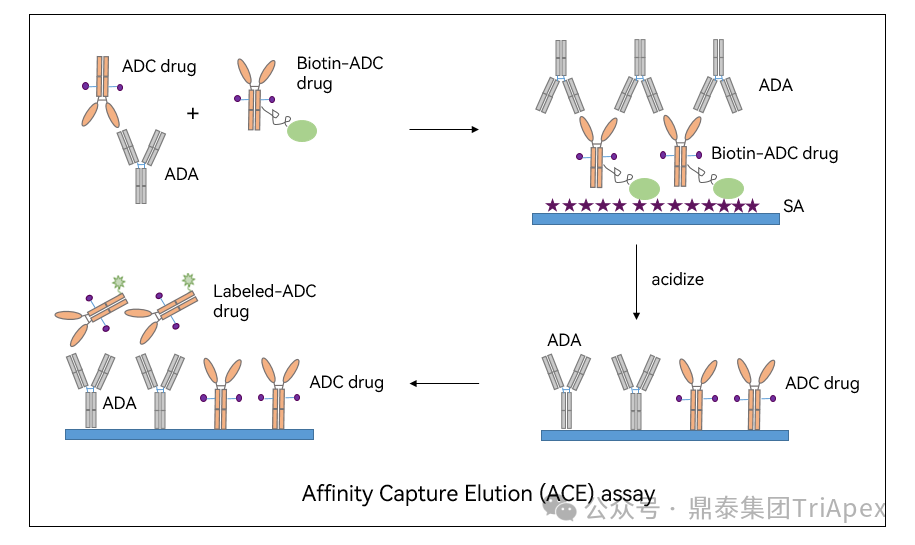
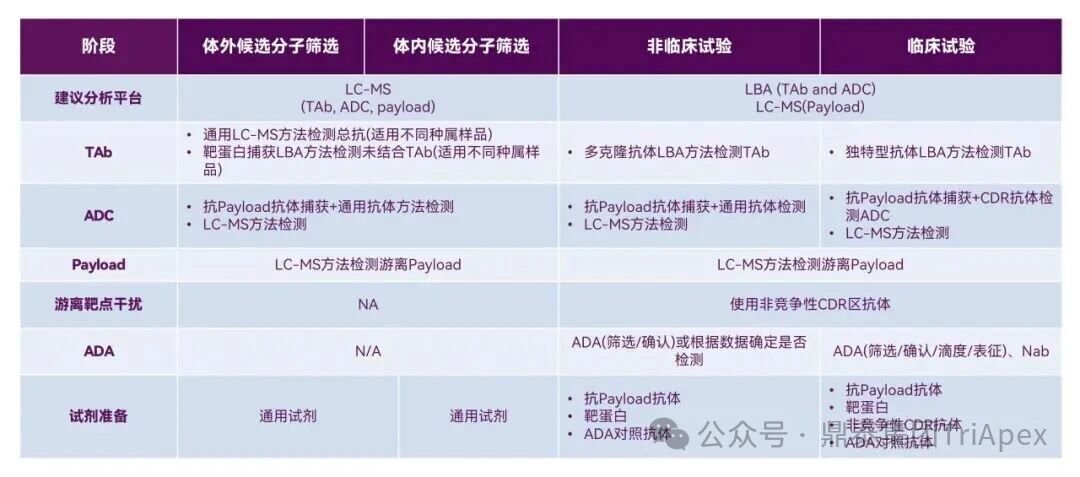
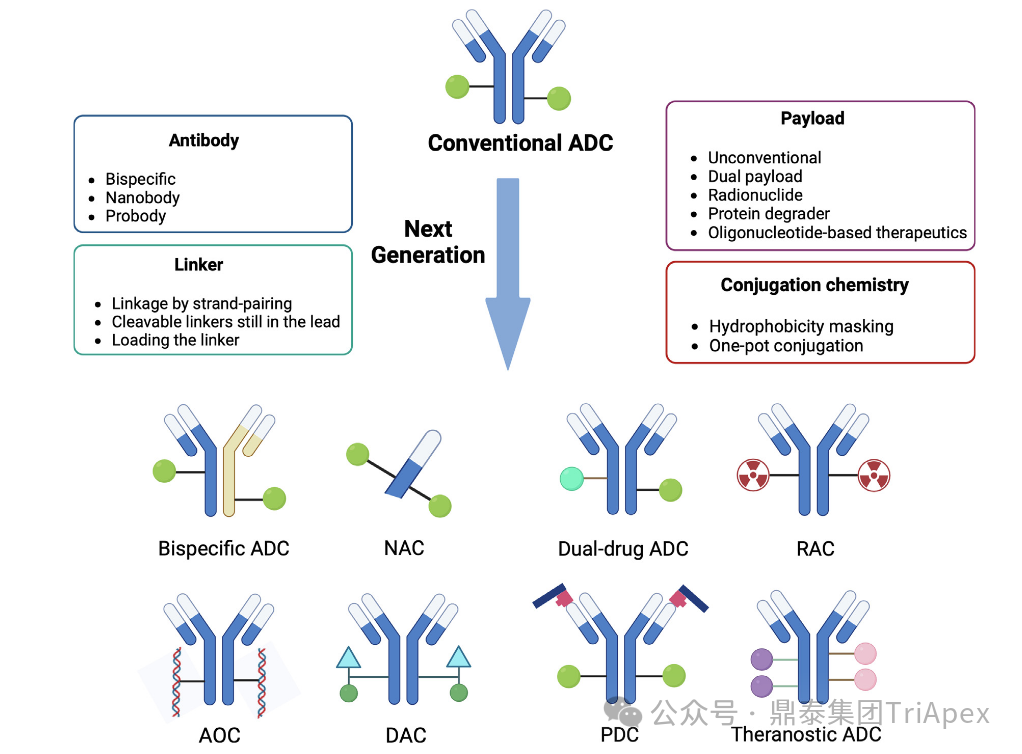
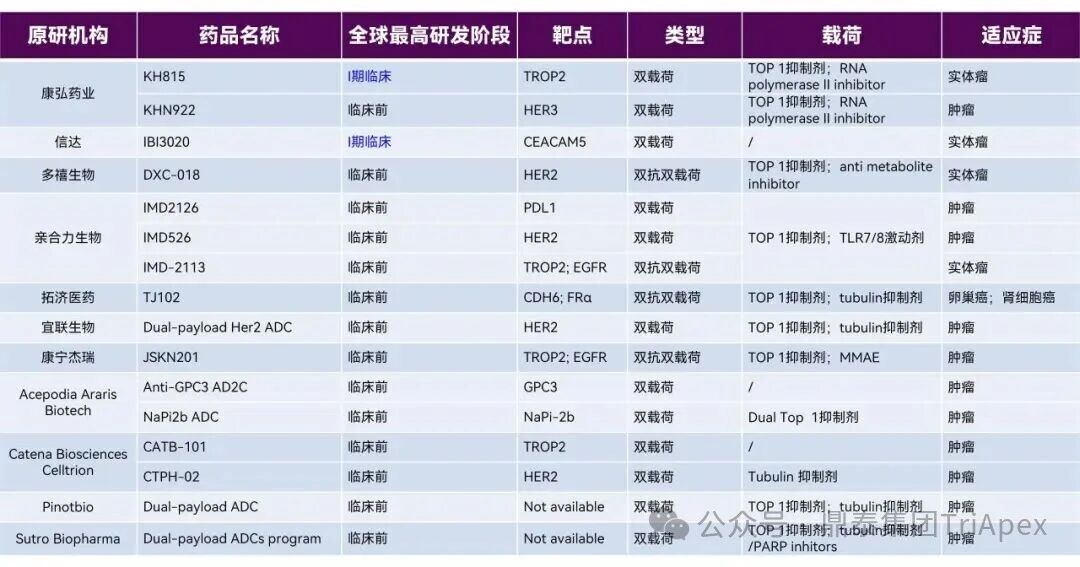
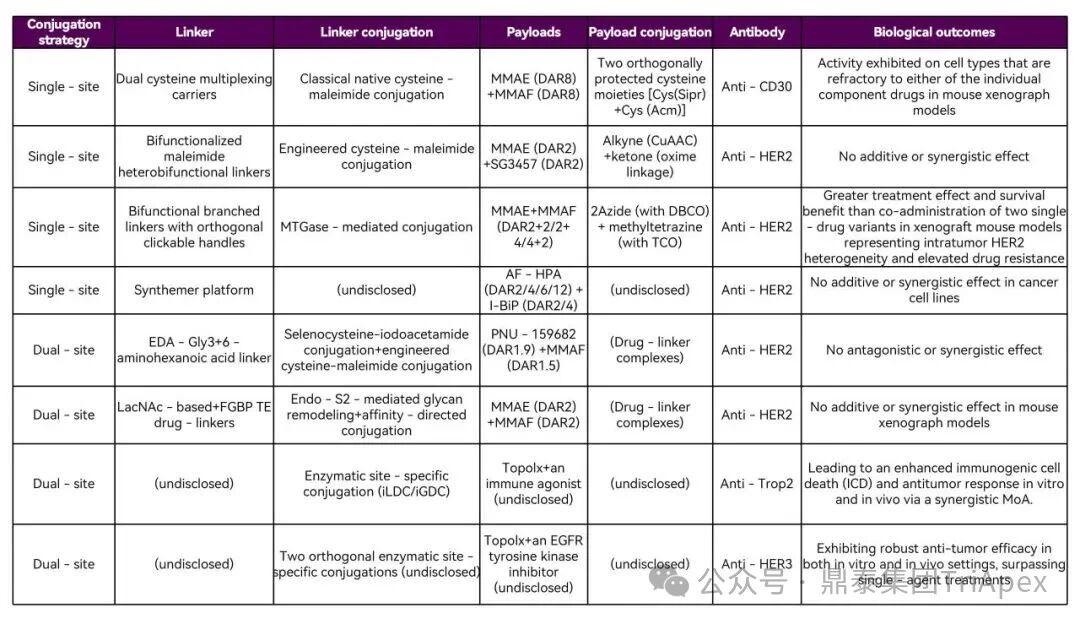
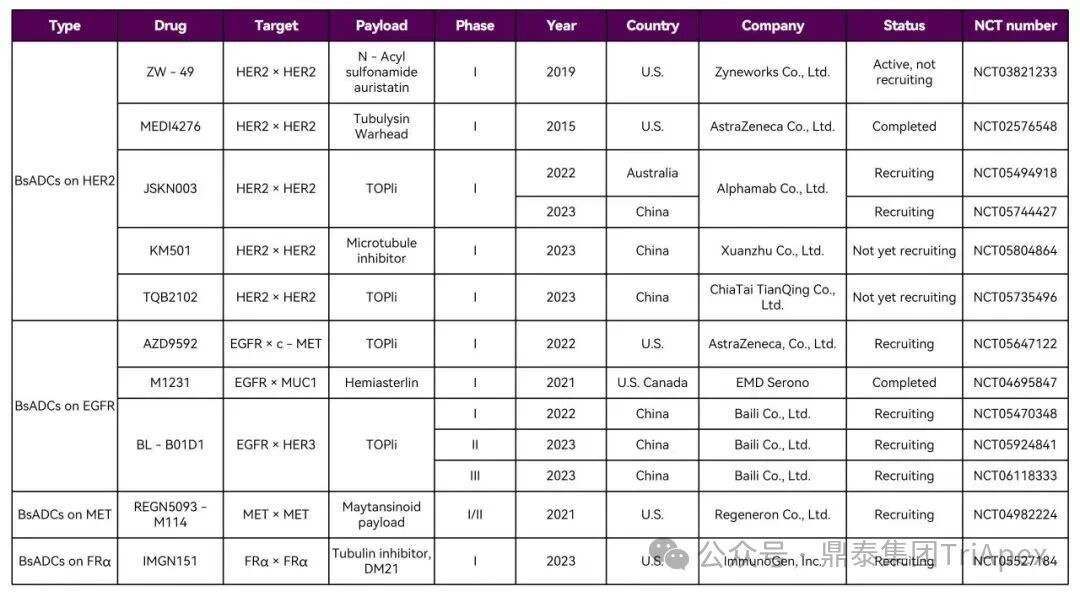
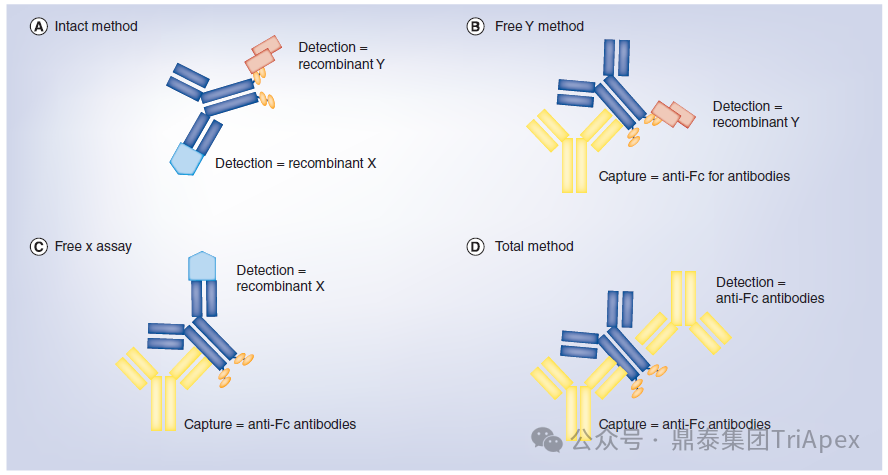
随着双特异性 ADC、双载荷 ADC 等新型结构的突破性进展,ADC 药物已从“单靶点精准打击”迈入“多维度协同作战”的新纪元。这些创新设计极大地拓展了治疗潜力,但同时也使其分子结构、作用机制与体内命运变得空前复杂。 在此背景下,可靠、精准的生物分析已超越其传统辅助角色,成为此类创新药物实现“概念验证”与成功研发的基石与瓶颈。它不仅是连接药物设计与临床疗效的“解码器”,更是评估其治疗窗口、解析耐药机制、并最终决定研发成败的关键。为了持续赋能不断演化的 ADC 药物的研发,鼎泰团队系统梳理了从单靶点到多维突破的 ADC 生物分析策略的演进,为应对新一代 ADC 的复杂挑战提供一份全面的技术路线图。 全文共:7056 字 19 图 预计阅读时长:20 分钟 2025 年美国癌症研究协会(AACR)年会于 4 月 25-30 日在圣地亚哥盛大召开,汇聚全球顶尖癌症研究成果。本届会议中, ADC 领域迎来重大突破,中国创新力量表现尤为瞩目。111 家中国药企携超过 100 款 ADC 新药亮相,在双抗 ADC(Bispecific ADC,BsADCs)和双载荷 ADC 等前沿技术领域占据绝对主导地位:全球披露的 32 项双抗 ADC 研究中,29 项来自中国企业;超过 16 项双载荷 ADC 研究中,超过 10 项源自中国。 然而,双特异性 ADC、双载荷 ADC 等新型结构的涌现,在极大地拓展了 ADC 药物治疗潜力的同时,也使其分子结构与体内行为变得空前复杂。在此背景下,可靠、精准的生物分析已超越其传统辅助角色,成为解析这类复杂创新药物体内命运、实现“概念验证”并最终决定研发成败的基石与瓶颈。鼎泰集团生物分析团队结合 50+ 项 ADC 生物分析项目中积累的一线研发经验,特别是支持 10+ 项双抗/双载荷 ADC 项目的实践,对新型ADC药物生物分析的新格局与核心策略进行了系统梳理,旨在为应对新一代 ADC 的复杂挑战提供一份全面的技术路线图与解决思路。 ★ 文章导览 ★ 01 ADC 介绍及非临床生物分析相关指导原则 02 ADC 药物生物分析策略 03 双抗 ADC、双载荷 ADC 生物分析介绍 04 结语 ADC 介绍及 非临床生物分析相关指导原则 1.1 ADC 介绍 目前,全球共批准了 19 种 ADC 药物(见表 1),针对不同肿瘤靶点的上百种 ADC 正处于不同的临床开发阶段。 因此,建立灵敏、可靠且可重复的生物分析方法,对于精准评估 ADC 药物在体内的药代动力学特征、靶点结合情况、疗效与安全性,乃至加速其临床开发与成功上市,具有至关重要的意义。 表 1. 已批准上市 ADC 药物汇总,数据来自于药渡数据库(截至 2025 年 7 月) 1.2 ADC 药物非临床分析相关指导原则 2023 年 NMPA 发布《抗体偶联药物非临床研究技术指导原则》,2024 年 FDA 发布《Clinical Pharmacology Considerations for Antibody-Drug Conjugates》指导原则,均提及了药代动力学和免疫原性检测相关的内容。对于 ADC 的生物分析及免疫原性的思路及其相关的分析方法建议遵循相关指导原则、参考相关白皮书,如图 1 和图 2。 图 1. ADC 产品指导原则分析思路 图2. ADC 产品生物分析与免疫原性技术性参考文件 ADC 药物生物分析策略 根据 FDA 及 NMPA 指导原则,ADC 的 PK 及 TK 生物分析中均建议检测 ADC、Tab 和游离小分子化合物,如图 3 所示。因此,需要综合的生物分析策略来识别、表征和定量 ADC 体内分解代谢命运(药代动力学,生物转化等)以进行安全性和有效性评估,需要借助的分析技术包括配体结合分析和液相色谱与质谱(LC-MS/MS)分析[3] [4] [5]。 图 3. ADC 药物各组分药时曲线图[2] 以下为 ADC 药物生物分析常用方法概览: 图 4. 基于 LBA 法检测总抗体与 ADC 模式图 2.1 LBA 法检测总抗体 Tab 的检测包含对完全偶联、部分解偶联和完全解偶联的抗体的分析,见图 4A。在 Tab 方法开发过程中,有如下关注点需注意: (1)关键试剂对偶联与非偶联抗体的结合差异 尽管上述包被及检测试剂不直接结合有效载荷,但有效载荷可能通过空间位阻效应间接干扰试剂与 ADC 抗体组分的结合。这种干扰在高 DAR 值 ADC 中尤为显著,因此在方法开发阶段应考察关键试剂对偶联与非偶联抗体的结合差异,避免该测定法无法精准量化体循环中所有预期的 DAR 分子组分的情况。 (2)游离靶点的干扰 游离形式的靶点能够与抗体结合、可能导致体内结合型 Tab 无法被检出。在临床阶段,应考虑健康人群和目标患者人群血液循环中可溶性药物靶点的表达水平,并在方法开发和验证过程中评估药物靶点的存在情况。若在生理或病理相关条件下靶点蛋白严重干扰检测的情况下,应考虑其它可用的检测模式。例如,使用非阻断型抗独特型抗体代替靶点蛋白作为捕获试剂;对于临床前的生物分析,也可以采用通用型的抗体试剂,例如对人源抗体重链或轻链特异性的抗体试剂,或尝试采用合适的试剂将靶点耗竭后进行检测。 2.2 LBA 法检测 ADC ADC 的分析方法一般以抗小分子抗体作为包被试剂,再以标记的靶蛋白或者抗 ADC 药物的独特型抗体或抗人 IgG Fc 抗体作为检测试剂,见图4B。该检测方法体现了等分子检测的原则(即 DAR 不敏感),保证了对药物偶联抗体的准确检测。相反地,如图 5,若以靶蛋白或抗独特型抗体或抗人 IgG 作为包被试剂,以标记的小分子抗体作为检测试剂,这种检测方法受到 ADC 分子中载荷数量的影响,违反了等分子检测的原则,导致检测结果不准确,因此不推荐该检测模式。 另外,在方法开发中应该考虑 ADC 分析方法受不同 DAR 值的影响,测试不同 DAR 值标准品的检测差异,选取合适 DAR 值的标准品及分析模式。 图 5. 基于 LBA 法检测 ADC 模式图(不推荐) 2.3 LC-MS/MS 法检测 LC-MS/MS 是非偶联有效载荷及其代谢物生物分析的首选平台。Hybrid LC-MS/MS 方法结合了 LBA 的高选择性和 LC-MS/MS 方法的选择性和灵敏度,在过去的十年中,尤其是在尚未获得合适的 LBA 试剂的早期发现阶段,Hybrid LC-MS/MS 方法已经代替 LBA 方法用于 Tab 和 ADC 的偶联有效载荷的生物分析。 Hybrid LC-MS/MS 检测模式见图 6。 Tab 定量:首先使用抗独特型抗体或通用捕获试剂(如 Protein A、Protein G 或抗人IgG)对 ADC 的 mAb 组分进行亲和捕获,从生物基质中提取 ADC,然后用胰蛋白酶或其他蛋白酶将 mAb 消化成替代肽/特征肽,最后通过 LC-MS/MS 定量。通常在胰蛋白酶消化步骤中加入稳定同位素标记的特征肽,以实现准确定量。 ADC 定量:通常通过亲和捕获 ADC,然后使用组织蛋白酶 B 和木瓜蛋白酶(用于蛋白酶可切割接头)等蛋白酶切割有效载荷,或用 DTT 或 TCEP(用于二硫键接头)进行还原,然后进行有效载荷的 LC-MS/MS 多反应监测(MRM)分析。 图 6. Hybrid LC-MS/MS 检测 ADC 药物示意图[6] 当然,对于一些特殊情况,需要调整检测体系,例如,如果无法获得抗小分子抗体,且连接小分子的为不可裂解 Linker,但能够获得针对抗体部分的抗体,这种情况下需要特殊考虑检测方式。如图 7 所示,Kcas bio 针对 ADC 药物制备 Specific Peptide 与 Common Peptide,通过 LC-MS/MS 检测,裸抗分析可检测到 Specific Peptide 与 Common Peptide,ADC 分析则可检测到 Common Peptide 与 Specific Peptide+payload,从而对 ADC 与 Tab 进行定量。 图 7. 位点特异的 ADC 和总抗的生物分析方法[12] 2.4 免疫原性检测 与其他生物制品类似,ADC 进入生物体后也可能会引起免疫原性,产生抗药抗体(Antibody Drug Antibody, ADA),包括结合型抗体(Binding Antibody)和中和型抗体(Neutralizing Antibody, Nab)。ADC 的免疫原性评价有助于对药代、药效和安全性结果进行分析,这在临床试验中更为重要。对于 ADC 的 ADA 分析,多采用配体结合检测方式,建议遵循 NMPA 指导原则《药物免疫原性研究技术指导原则》以及 FDA 法规《Immunogenicity Testing of Therapeutic Protein Products —Developing and Validating Assays for Anti-Drug Antibody Detection》进行方法开发、验证以及三层级分析检测策略。 图 8. ADA 常用检测平台与模式 (1)检测平台 ADA 常用的检测平台有 ELISA 与 ECL,如图 8。ECL 平台方法的灵敏度高、定量范围广且重复性高、稳定性好,但在临床前的 ADA 分析中,考虑到经济性,较多采用 ELISA 法。 (2)检测模式 检测模式分为桥联法和间接法,如图 8,在试剂能够获得的情况下,桥联法是优先选择的方法。桥联 ECL 法以生物素化药物作为包被试剂,以钌标记的药物作为检测试剂;桥联 ELISA 法采用药物直接包被,生物素化的药物作为检测试剂。桥联检测模式不受检测样品种属及阳性抗体种属限制,且特异性强;但是,在实际方法开发中,受限于标记药物的可获得性或药物标记后结合活性降低,可考虑采用针对阳性抗体种属和样品种属的混合二抗作为检测试剂,但该方法有可能会出现待测样品假阴性的情况。为了解决上述问题,间接检测模式通常会采用 ProteinA/G/L 作为检测试剂,该检测试剂可用于多个种属的检测,避免假阴性的风险。但是,该方法在实际操作中会比其他方法更容易出现污染、本底信号值升高等不稳定的情况。 (3)提高 ADA 检测的药物耐受水平 由于非临床毒理研究给药剂量相对较高,生物样品中含有高浓度的药物与 ADA 竞争性结合,从而影响 ADA 的检测,表现为方法的药物耐受性差。为了解决上述问题,通常在 ADA 方法开发阶段,根据给药剂量估算药物浓度,尽量提高方法的药物耐受性。目前应用比较多的是 ACE 法,如图 9所示,通过生物素标记的药物富集 ADA,然后通过酸化将 ADA 洗脱后包被于板底,最后采用标记后的药物进行检测。另外,可通过采集受试者体内药物谷浓度时的样本来尽量降低血药浓度过高产生的干扰。 图 9. 亲和捕获洗脱方法(Affinity Capture Elution, ACE) 2.5 ADC 产品分析思路小结 表2. ADC 产品生物分析小结 表 2 系统梳理了 ADC 药物研发不同阶段中,针对不同待测物的分析策略与考量重点。其核心在于根据研发阶段的特点和待测物(Tab、ADC、Payload)的复杂性,选择并优化最适宜的分析方法(LC-MS 或 LBA)。 在早期发现阶段(体外/体内候选分子筛选),分析的重点是快速、通用和高通量。LC-MS 因其高灵敏度和特异性,成为检测小分子 Payload 和进行初步 ADC 表征的首选方法。另外,Tab 及 ADC 的检测,也可采用灵活的 LBA 法来评估其结合活性。此阶段的关键考量是方法开发速度和平台通用性,以支持大量候选分子的快速评估,因此优先采用通用试剂。 进入开发阶段(非临床/临床试验)后,分析的重心转向方法的精确性、可靠性和对复杂生物基质的适应性,检测试剂由通用型抗体向独特性抗体转变。 双抗、双 Payload ADC 药物 传统的 ADC 由三部分组成:抗体、Linker 和有效载荷。根据抗体、Linker、有效载荷和偶联化学试剂的选择,研究者开发出新的 ADC,出现了新术语,如图 10 所示。 双特异性 ADC(Bispecific ADC,BsAb) 纳米抗体-药物偶联物(Nanobody–drug conjugate,NAC) 双载荷抗体偶联药物(Dual-payload ADC) 放射性核素-抗体偶联物(Rradionuclide–antibody conjugate,RAC) 抗体-寡核苷酸偶联物(Antibody–Oligonucleotide Conjugate,AOC) 抗体降解偶联物(Antibody-degrading Conjugate,DAC) 前体-药物偶联物(Probody–drug Conjugate,PDC) 治疗诊断 ADC(Theranostic ADC) 本节主要介绍双特异性 ADC 以及双载荷 ADC 开发给生物分析带来的新挑战和生物分析关注点。 图 10.下一代 ADC 药物示意图[1] 如表 3 所示,在 2025 年的 AACR 会议中,国内多禧生物、康弘药业、康宁杰瑞、亲合力生物等企业均披露布局的双毒素 ADC;多禧生物、康宁杰瑞、亲合力生物、拓济医药布局双靶点双毒素 ADC;康弘药业 KH815 成为全球首个进入临床的双毒素 ADC 药物。除此之外,信达 IBI3020 是一款靶向 CEACAM5 的双毒素 ADC,目前在中国已获批 IND,拟治疗实体瘤。国外企业在双载荷 ADC 的管线目前多处于临床前阶段。 表 3. 2025 AACR 公布的双载荷 ADC,数据来自医药魔方(截至 2025 年 07 月) 3.1 双载荷抗体偶联药物(Dual-payload ADC) (1)Dual-payload ADC 的概念与结构 尽管 ADC 药物显著拓展了治疗选择,但仍面临若干挑战。一个主要问题是:抗体在肿瘤组织内的药物渗透有限,这会限制药物递送并导致疗效欠佳[7]。此外,传统 ADC 疗法中,在治疗压力下耐药性癌细胞群的富集仍是重大障碍:由于依赖单一治疗药物形成的选择性压力,使得不敏感的肿瘤细胞得以存活并增殖,最终导致肿瘤组织内出现获得性耐药。针对以上痛点,双载荷 ADC 应运而生,设计思路如图 11 所示。 图 11. 双载荷 ADC 结构[8] A) 双载荷 ADC 的概念设计和考虑 B) 双载荷 ADC 的双重偶联模式:单一位点偶联(single-site)和双位点偶联(dual-site) (2)已报道 Dual-payload ADC 汇总 表 4 展示了目前已报道的 Dual-payload ADC 设计。 表4. 已报道的 Dual-payload ADC 设计汇总[8] (3)Dual-payload ADC 生物分析检测模式及特殊考虑点 Dual-payload ADC 的抗体分析 Dual-payload ADC 抗体部分的检测策略可以参考单抗 ADC 的 PK 生物策略,详见 02 ADC 药物生物分析策略部分。 Dual-payload ADC 的 ADC 部分分析 建议重点关注检测携带任一或两种 payload 的 ADC 总量。即捕获抗体分别采用两种抗小分子抗体,检测抗体采用靶点或抗独特型抗体。需要关注的是,两种方法检测结果的可比性及解读分析。当使用基于抗体部分(如某段特征肽)的 LC-MS/MS 定量方法测定 ADC 总浓度时,由于该方法测得的是抗体骨架的量,而非载药分子总量,需用平均 DAR 进行校正,得到更接近真实药物分子(即整个ADC)的浓度,对 PK/PD 研究和疗效评估至关重要。 3.2 双特异性抗体(Bispecific ADC,BsADCs) (1)BsADCs 的概念与结构 虽然 ADC 毒性的主要来源为有效载荷或连接子和有效载荷复合物,但是抗体与抗原的结合也对药物作用产生重大影响。解决上述临床挑战的前瞻性方法就是将双特异性抗体与接头有效载荷复合物的偶联,从而产生了双特异性抗体药物偶联物的概念。 BsADCs 是一类能够同时识别并结合两种不同抗原或抗原表位的抗体分子。迄今为止探索的双特异性 ADC 设计可以分为两种类型,根据其结合模式进行分类,包括同时与两种不同抗原结合(双靶点)的 ADC 或与同一抗原上的两个不同表位结合(双表位)ADC,如图 12 所示。 图 12. BsADCs 结构[9] A) BsADCs 的概念设计和考虑;B) 双表位、双靶点 ADC 结合模型;C) 可能的 BsADC 设计的结构类型 (2)BsADCs 的作用机制 BsADCs 具有独特的优势,可通过网格蛋白介导的内吞和非网格蛋白介导的内吞途径促进内化及溶酶体降解,具体过程如图 13。 图 13. BsADCs 的作用机制[10] (3)临床在研 BsADCs 资料汇总 截止 2024 年,有 10 个 BsADC 正在进行临床试验(如表 5),用于治疗各种血液病和某些实体瘤,一些早期临床试验结果在最近的 AACR 和 ESMO 会议上公布。 表5. BsADCs 临床进展[9] (4)BsADCs 生物分析检测模式及考虑点 BsADCs 的 Tab 分析 由于双特异性抗体具有多个不同的结合位点和复杂的作用机制,这些为生物分析方法的设计带来了新的挑战。生物分析方法设计时需要综合考虑药物结构特点、靶点情况、作用机制和特征、技术可行性及监管要求等内容。 如图 14 所示,由于双特异性抗体在结构上具有不同的结合位点,BsAb 在体内可能存在不同的形式,其活性的和非活性形式在方法策略制定时均需要考虑在内,并需要多种生物分析方法来满足不同形式药物的检测需求,包括:完整分子,单靶点游离分子和总药物分子,对不同分子形式的 BsAb 的检测分析需要按照“case by case”原则制定科学的检测策略。其中,游离的完整分子的药物浓度对于 PK 更有意义,总药物分子的药物浓度对于 TK 更有意义,结合型的药物浓度则跟药效更加相关。检测方面往往可以通过分析 format 的设计来达到检测不同形态药物的目的。检测策略如下: □ 游离的完整分子(图 14 A) 使用两个靶点分别作为包被及检测试剂 条件:双特异性抗体药物在体外或体内稳定 目的:测量生物基质中没有任何功能域被靶点或者 ADA 阻断的完整的有活性的双特异性抗体分子 □ 单靶点游离分子(图 14 B和图 14 C) 使用一个靶点蛋白作为捕获试剂,抗人 IgG Fc 抗体作为检测试剂 注意:需考察两个靶点分别包被的方法对检测结果的影响 □ 总药物分子(图 14 D) 使用通用型抗人 IgG Fc 抗体作为包被和检测试剂 特殊处理:酸化的方式使得 bound 型的药物分子与靶点/抗药抗体的连接被打破,从而可以更加灵活地对 total 型药物进行检测。 图 14. BsADCs 抗体部分的检测[11] BsADCs 的 ADC 部分分析 对于 BsADCs 的 ADC 部分,可参考 02 ADC 药物生物分析策略部分所述单抗 ADC 的检测方式。 BsADCs 生物分析考虑点 BsADC 药物的生物分析,与普通 ADC 药物的相比,尤其要注意的是双靶点影响。需评估所建立方法检测样品中 ADC 与 Tab 的一致性,根据鼎泰项目经验,若遇到 ADC 与 Tab 不一致的情况,可以考虑两个靶点混合使用作为包被及检测试剂。 (5)BsADCs 药物的抗药抗体分析 BsADCs 的 ADA 分析可参考本文 02 ADC 药物生物分析策略中常规 ADC 的 ADA 检测,在此不进行赘述。鉴于 BsADCs 能够结合两个抗原结构域,基于风险评估,非临床阶段一般不需要对 ADA 确证为阳性的样本进一步开展结构域特异性分析,临床阶段一般在中后期进行。 结语 随着双抗 ADC、双载荷 ADC 等新型结构的突破性发展,ADC 在肿瘤治疗等领域的地位日益凸显。生物分析作为创新药物开发全链条中的关键环节,承担着评估药代、药效和毒性的重要任务。由于新型 ADC 结构复杂性,涉及双靶点协同作用、双毒素 PK 分离、动态 DAR 异质性等诸多挑战,加之全球监管指南仍处于快速演进阶段,当前生物分析仍面临方法可比性、数据解读标准化等系统性挑战。值得期待的是,随着中国企业在全球 ADC 创新中成果的加速涌现,行业经验与数据资产的持续积累,会进一步推动分析技术体系的深度优化。未来,针对新型 ADC 的成熟化检测标准有望逐步建立,从而为下一代 ADC 的临床转化提供精准、可靠的数据支持。