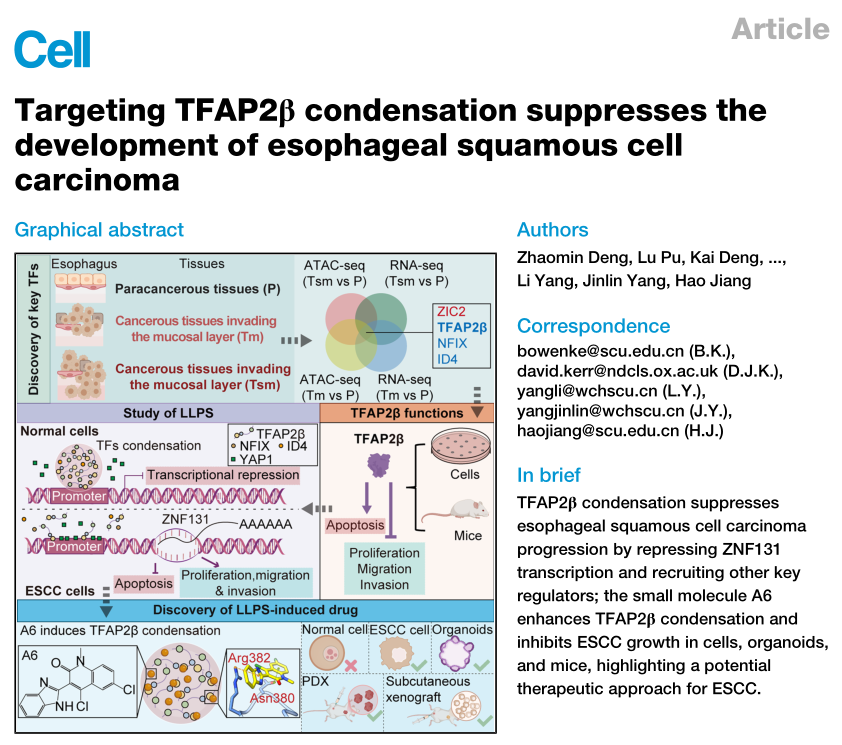
在食管鳞状细胞癌(ESCC)治疗面临困境的背景下,液-液相分离(LLPS)作为一种新兴的生物学机制,其与肿瘤发展的关联逐渐受到重视。先前研究已发现,长链非编码RNA MALR可通过促进ILF3蛋白的相分离驱动ESCC进展。然而,是否存在其他关键转录因子通过相分离主导ESCC的转录失调,以及能否针对此过程开发特异性疗法,仍是领域内悬而未决的核心问题。四川大学华西医院、牛津大学及中国科学技术大学等机构合作团队针对此科学问题展开了系统研究。他们不仅揭示了转录因子TFAP2β在ESCC早期通过形成相分离凝聚体发挥关键抑癌功能,更首创性地开发出首个能够特异性增强该过程的小分子化合物A6,为ESCC的靶向治疗提供了全新策略。中文标题:靶向TFAP2β相分离抑制食管鳞状细胞癌的发展
期刊名称:Cell
影响因子:42.5
发表时间:2026年2月5日(提前在线发表)
01 研究背景
食管鳞状细胞癌(ESCC)是全球范围内一种高致死性的恶性肿瘤,占所有食管癌病例的约90%。尽管内镜切除、放化疗及靶向治疗(如抗血管生成药物、抗HER2疗法及免疫检查点抑制剂)已成为临床标准,但其疗效有限且常伴随显著副作用,导致患者总体生存率仍然不容乐观。因此,深入解析ESCC发生发展的分子机制,并寻找更具特异性和有效性的治疗靶点,是该领域亟待突破的核心问题。
近年来,转录因子(TFs)的功能失调被广泛认为是驱动肿瘤转录组重塑和恶性表型的关键。然而,在ESCC早期阶段,全局性的染色质可及性变化及与之耦合的转录调控网络仍不明确。与此同时,液-液相分离(LLPS)作为一种新兴的生物学原理,在调控基因转录、信号转导等细胞过程中扮演着关键角色。已有研究提示,LLPS与多种胃肠道肿瘤的发展相关。例如,在ESCC中,长链非编码RNA MALR被报道可通过促进ILF3蛋白的相分离来激活HIF1α信号通路,从而加速肿瘤进展。这些发现初步将相分离现象与ESCC联系起来。
尽管如此,关于相分离在ESCC中的普遍性、具体的调控机制,尤其是是否有其他关键转录因子通过形成相分离凝聚体来支配ESCC的转录程序,以及能否针对这一过程开发特异性治疗药物,这两个根本性问题仍然悬而未决,构成了当前研究的空白与挑战。
▏识别早期ESCC的核心下调转录因子TFAP2β
前因:早期ESCC的全局染色质可及性和转录调控网络不明。传统ATAC-seq技术对微量临床样本成功率低。
过程与结果:
技术优化:研究团队首先改进了ATAC-seq建库方法(使用胶原酶和分散酶消化),成功对28例早期ESCC患者的配对样本(癌旁P、黏膜层癌Tm、黏膜下层癌Tsm)进行了染色质可及性分析,成功率超过80%(Fig.1A)。
多组学整合分析:对同一样本进行ATAC-seq和RNA-seq测序。分析发现,与癌旁组织相比,癌组织中染色质可及性增加的区域多位于启动子区,而减少的区域多在远端调控元件(Fig.1C-D)。整合分析染色质开放变化与差异表达基因,并辅以转录因子 motif 分析,最终锁定了一个在癌组织中共同下调的转录因子:TFAP2β(Fig.1F-H)。
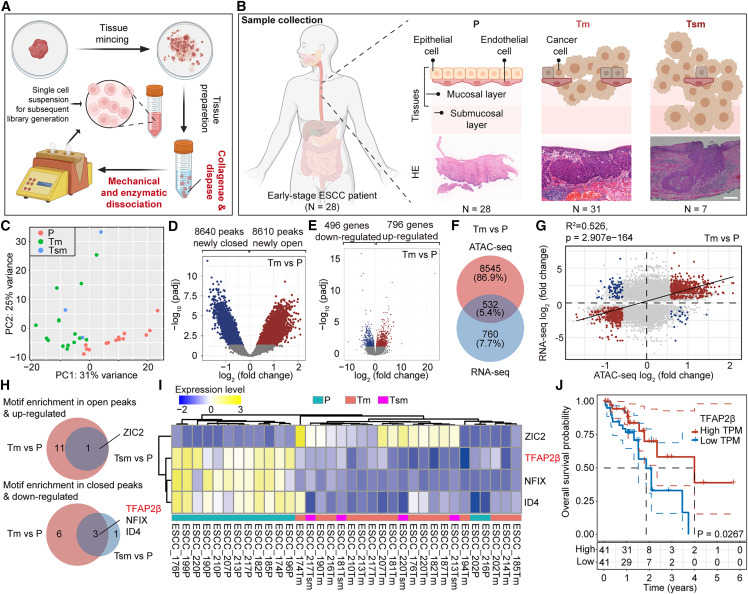
图1 TFAP2β被鉴定为在早期ESCC中下调的关键转录因子
A:用于微量临床样本的优化ATAC-seq建库流程示意图。B:从28例早期ESCC患者中收集多阶段(癌旁P,黏膜层癌Tm,黏膜下层癌Tsm)样本的策略及代表性H&E染色。C:基于ATAC-seq数据的染色质可及性主成分分析,显示P、Tm、Tsm组间的差异。F:Tm vs. P组中,差异可及性峰相关基因与差异表达基因的重叠情况(韦恩图)。G:Tm vs. P组中,染色质可及性变化与基因表达变化的相关性分析。H:通过整合motif富集分析和差异表达数据,鉴定出在Tm vs. P和Tsm vs. P两组比较中共同上调和下调的转录因子(韦恩图)。I:关键转录因子(TFAP2β, ZIC2, NFIX, ID4)在P、Tm、Tsm样本中的表达热图。J:基于TCGA数据的生存分析,显示TFAP2β低表达与ESCC患者不良预后相关。小结:TFAP2β被鉴定为在ESCC发生早期即下调的关键转录因子,其低表达与患者不良预后相关(Fig. 1I-J)。这提示TFAP2β可能是一个重要的抑癌因子,引出了对其功能的深入探索。
▏验证TFAP2β在ESCC中的抑癌功能
前因:TFAP2β在ESCC中下调,但其具体功能未知。
过程:
临床样本验证:在患者组织样本中证实,TFAP2β的mRNA和蛋白水平从癌旁组织到早期癌再到晚期癌逐步降低(Fig.2A-B)。
细胞功能实验:在ESCC细胞系中过表达TFAP2β,可显著抑制细胞增殖、克隆形成、迁移和侵袭,并促进细胞凋亡;敲低TFAP2β则效果相反(Fig.2D-L)。
动物模型验证:在小鼠皮下移植瘤模型中,过表达TFAP2β能抑制肿瘤生长;在尾静脉转移模型中,能显著减少肺和肝的转移灶(Fig.2M-T)。
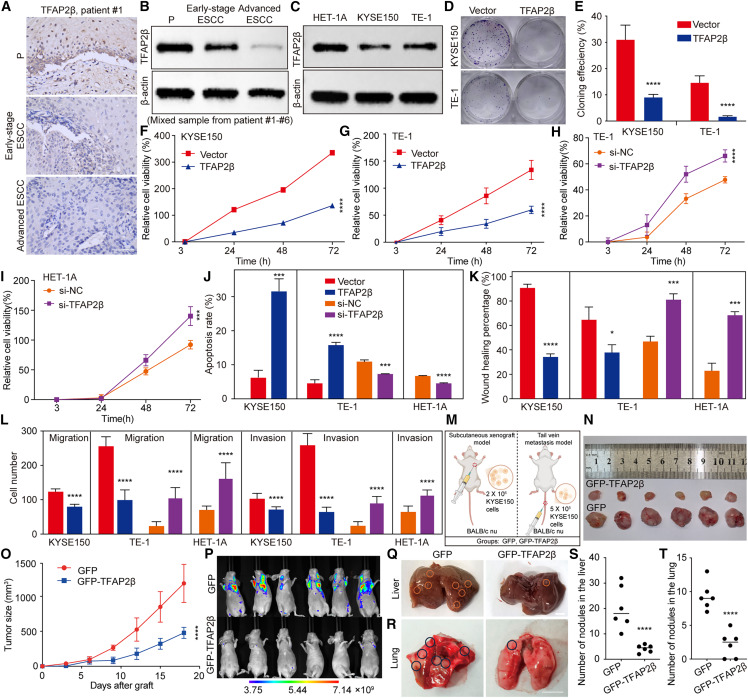
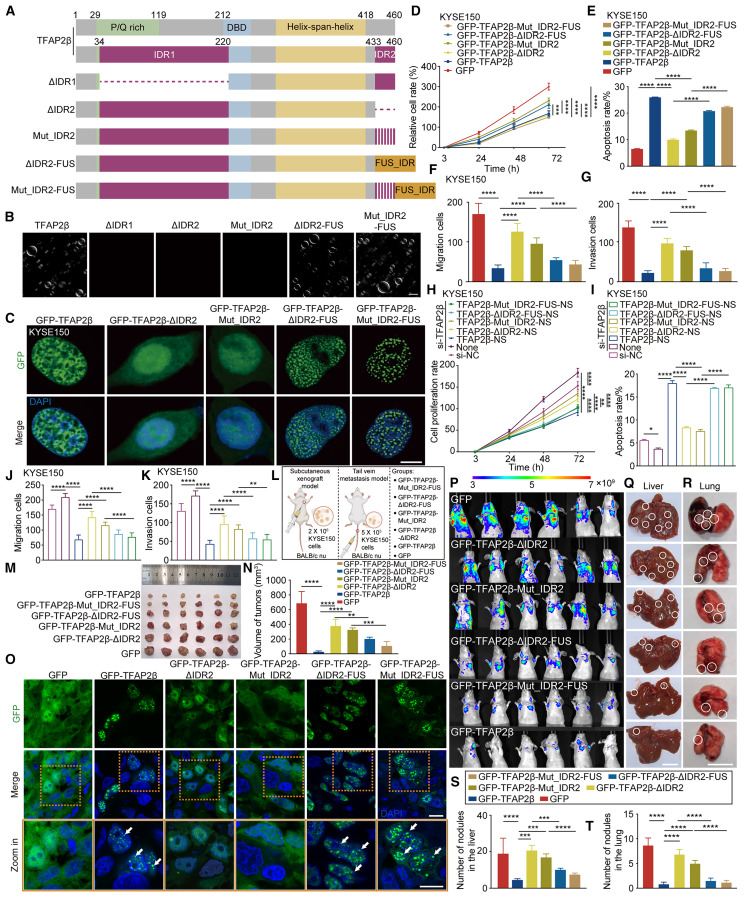
图2 TFAP2β促进细胞凋亡并抑制ESCC细胞增殖、迁移和侵袭
A:患者配对组织(P,早期ESCC,晚期ESCC)的TFAP2β免疫组化染色。
B-C:患者样本和细胞系中TFAP2β蛋白水平的免疫印迹分析。
D-E:过表达TFAP2β对KYSE150和TE-1细胞克隆形成能力的抑制。
F-I:CCK-8实验显示过表达TFAP2β抑制细胞增殖,敲低TFAP2β促进增殖。
J:流式细胞术分析显示TFAP2β促进细胞凋亡。
K-L:伤口愈合和Transwell实验显示TFAP2β抑制细胞迁移和侵袭。
M:皮下移植瘤和尾静脉转移小鼠模型示意图。
N-O:过表达TFAP2β的移植瘤体积更小,生长更慢。
P-T:活体成像及离体器官观察显示,过表达TFAP2β显著减少肺和肝的转移结节数量。
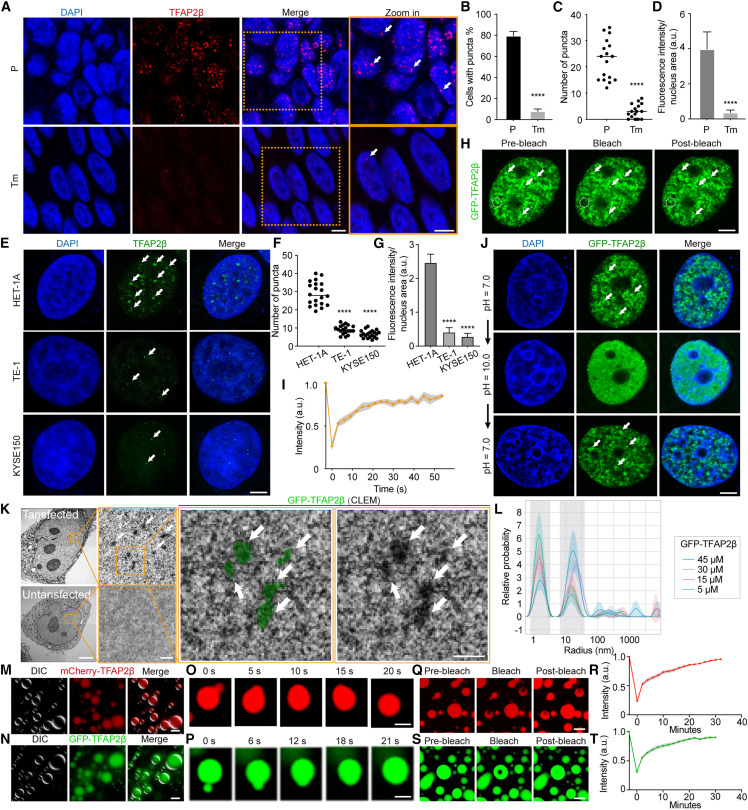
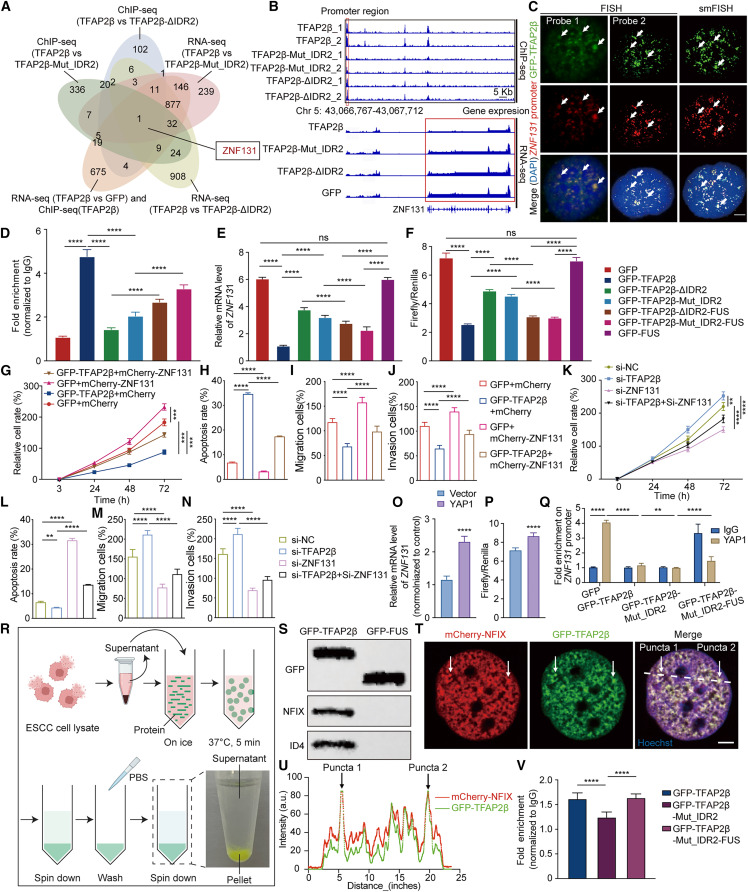
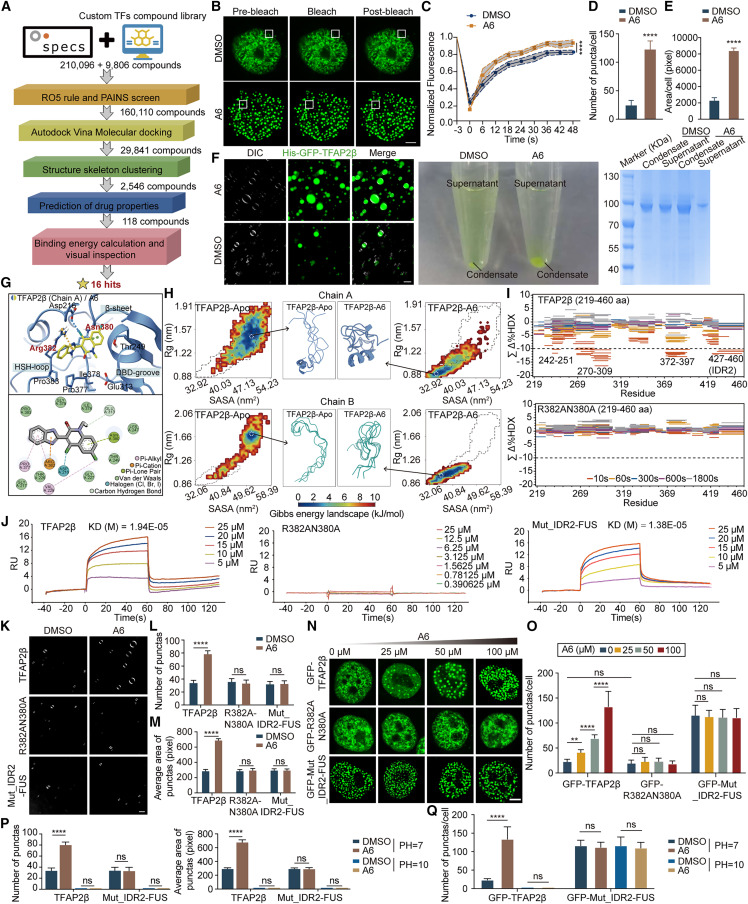
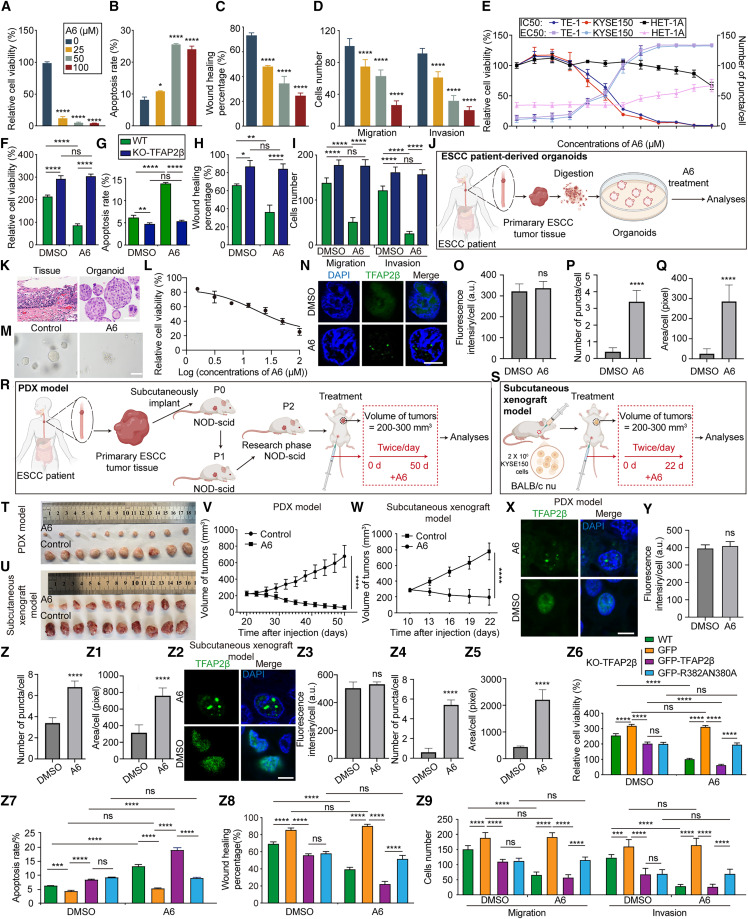
小结:TFAP2β被确认为一个强有力的ESCC抑癌因子,其功能缺失可能驱动ESCC的进展和转移。这自然引出一个关键问题:TFAP2β通过什么分子机制发挥这些抑癌作用?▏发现TFAP2β通过液-液相分离行使其功能前因:TFAP2β等被鉴定出的关键TF均含有可能介导相分离的内在无序区(IDR)。相分离现象观察:免疫荧光显示,TFAP2β在正常/癌旁食管细胞核内形成明显的点状凝聚体,而在ESCC细胞中这种凝聚现象减弱(Fig. 3A-G)。体内动态性:荧光漂白恢复实验表明,TFAP2β核内凝聚体具有高度流动性(Fig. 3H-I)。可逆性:改变pH值可逆地溶解和重建凝聚体(Fig. 3J)。无膜结构:相关光镜-电镜联用显示其为无膜的电子致密结构(Fig. 3K)。体外重建:纯化的TFAP2β蛋白在体外能形成液滴,并表现出融合、动态等典型相分离特征(Fig. 3L-T)。图3 TFAP2β在细胞核内和体外均表现出相分离性质A-G:TFAP2β在癌旁组织、癌细胞系(HET-1A, TE-1, KYSE150)的细胞核内形成点状凝聚体,并在ESCC中减弱。H-I:荧光漂白恢复实验证明GFP-TFAP2β核内凝聚体具有高度动态性。J:pH值变化可逆地溶解和重组GFP-TFAP2β凝聚体。K:相关光镜-电镜图像显示GFP-TFAP2β凝聚体为无膜的电子致密结构。L:动态光散射显示GFP-TFAP2β蛋白形成液滴。M-T:纯化的mCherry/GFP/His标签TFAP2β蛋白在体外形成液滴,表现出融合和动态特性。关键结构域定位:鉴定出TFAP2β的C端IDR2(含6个保守正电荷残基)对其相分离至关重要。突变这些残基会破坏相分离(Fig. 4A-C)。功能回补实验:在细胞和小鼠模型中,丧失相分离能力的TFAP2β突变体其抑癌功能显著削弱;而通过融合异源相分离域(FUS-IDR)恢复其凝聚能力后,抑癌功能也得以恢复(Fig. 4D-T)。图4 TFAP2β的相分离介导其在ESCC细胞增殖、凋亡和迁移中的功能B:体外液滴形成实验显示,IDR缺失或突变体丧失相分离能力,融合FUS-IDR后可恢复。C:细胞中过表达不同TFAP2β变体,观察其核内凝聚体形成情况。D-K:细胞功能实验证明,丧失相分离能力的突变体(ΔIDR2, Mut_IDR2)其抑制增殖/迁移/侵袭和促进凋亡的功能减弱;恢复相分离后(融合FUS-IDR),功能也得以恢复。M-O:小鼠皮下移植瘤实验证实,TFAP2β的相分离能力是其抑制肿瘤生长所必需的。P-T:小鼠尾静脉转移模型证实,TFAP2β的相分离能力是其抑制肿瘤转移所必需的。小结:TFAP2β的抑癌功能严格依赖于其发生液-液相分离的能力。这突破了将TFAP2β仅视为传统转录因子的认知,将其功能与生物分子凝聚体这一新范式联系起来。前因:需要明确TFAP2β凝聚体如何调控转录以抑制癌症。下游靶点筛选:结合ChIP-seq和RNA-seq数据,发现ZNF131是唯一受TFAP2β相分离直接调控的基因(Fig. 5A)。结合与抑制机制:TFAP2β凝聚体直接结合在ZNF131启动子区(Fig. 5B-C),其相分离能力越强,结合与抑制效果越强(Fig. 5D-F)。机制上,TFAP2β通过“占据”启动子,阻断了转录激活因子YAP1对ZNF131的激活(Fig. 5O-Q)。功能性验证:ZNF131过表达可逆转TFAP2β的抑癌效应,而敲低ZNF131则可模拟TFAP2β过表达的效果(Fig. 5G-N)。平台功能发现:TFAP2β凝聚体还能作为分子平台,招募另外两个关键下调TF(NFIX和ID4),增强它们与各自靶基因DNA的结合(Fig. 5R-V)。图5 TFAP2β凝聚体抑制ZNF131转录并招募其他转录因子A:通过多数据集交叉分析,鉴定出TFAP2β相分离的直接下游靶基因ZNF131(韦恩图)。B:基因组浏览器视图展示TFAP2β结合在ZNF131启动子区域。C:FISH/smFISH实验显示GFP-TFAP2β凝聚体与ZNF131启动子位点共定位。D-F:ChIP-qPCR、RT-qPCR和荧光素酶报告基因实验证实,TFAP2β的相分离能力增强其与ZNF131启动子的结合并抑制其转录。G-N:功能回复实验证明,过表达ZNF131能逆转TFAP2β的抑癌效应;敲低ZNF131能逆转TFAP2β敲低促癌效应。O-Q:机制探究发现,TFAP2β通过其凝聚体竞争性抑制转录激活因子YAP1与ZNF131启动子的结合。R-V:液滴沉降实验和活细胞成像显示,TFAP2β凝聚体能招募NFIX和ID4;ChIP-qPCR证实TFAP2β凝聚体增强NFIX与其靶基因Meis1增强子的结合。小结:揭示了TFAP2β相分离的双重功能:一方面,作为转录抑制器,直接抑制致癌基因ZNF131;另一方面,作为分子平台,协同调控其他关键转录因子的活性。这解释了其强大的抑癌效果。前因:TFAP2β相分离是明确的抑癌机制,但尚无靶向此过程的ESCC治疗药物。虚拟筛选与发现:建立针对TFAP2β的虚拟筛选流程,从数万化合物中筛选出能增强其相分离的候选分子A6(Fig. 6A)。机制验证:A6能直接结合TFAP2β的DNA结合域,通过变构效应稳定其IDR2构象,增强静电相互作用,从而特异性促进TFAP2β的相分离(Fig. 6G-Q)。图6 化合物A6在体内外诱导TFAP2β发生相分离B-C:FRAP实验显示A6处理增强了GFP-TFAP2β核内凝聚体的动态恢复速度。D-E:A6处理增加了KYSE150细胞中TFAP2β核内凝聚体的数量和面积。F:体外液滴沉降实验显示A6促进His-GFP-TFAP2β形成更多的凝聚体。G:分子动力学模拟显示A6与TFAP2β DBD沟槽区的Arg382和Asn380残基相互作用。H:自由能景观图显示A6结合使TFAP2β的IDR2区域构象更稳定、更有序。I:氢氘交换质谱分析显示A6结合降低了TFAP2β多个区域(包括IDR2)的构象动态性。J:表面等离子共振实验测定A6与不同TFAP2β变体的结合亲和力。K-Q:一系列体外和细胞内实验证明,A6促进TFAP2β相分离的作用依赖于其IDR2中的关键正电荷残基以及生理pH环境。体外:A6以剂量依赖性方式抑制ESCC细胞增殖、迁移和侵袭,并促进凋亡,且该效应依赖于TFAP2β的存在(Fig. 7A-I)。类器官模型:在患者来源的ESCC类器官中,A6同样能抑制生长并增强TFAP2β的核内凝聚(Fig. 7J-Q)。体内模型:在PDX模型和细胞系移植瘤模型中,A6治疗能显著抑制肿瘤生长,且未引起明显毒性。肿瘤组织分析证实A6增强了瘤内TFAP2β的凝聚,但不影响其蛋白总量(Fig. 7R-Z5)。图7 化合物A6通过靶向并促进TFAP2β相分离来抑制ESCC进展A-D:A6以剂量依赖的方式抑制KYSE150细胞活力、促进凋亡、抑制迁移和侵袭。E:不同细胞系(KYSE150, TE-1, HET-1A)对A6的敏感度与其TFAP2β凝聚体形成能力相关。F-I:在TFAP2β敲除或敲低的细胞中,A6的抗肿瘤效应显著减弱,证明其作用依赖于TFAP2β。J-Q:在患者来源的ESCC类器官中,A6处理降低类器官活力、减小其尺寸,并增强TFAP2β的核内凝聚。R-W:在PDX模型和皮下移植瘤模型中,A6治疗显著抑制肿瘤生长,且未明显影响小鼠体重。X-Z5:免疫荧光显示,A6治疗增加了肿瘤细胞内TFAP2β的核内凝聚,但不改变其总蛋白水平。Z6-Z9:功能挽救实验证明,A6的抗肿瘤效应依赖于其与TFAP2β的直接相互作用(R382A/N380A突变使其失效)。小结:成功发现了首个通过增强抑癌蛋白相分离来发挥抗肿瘤作用的候选药物A6,完成了从机制研究到潜在疗法开发的转化闭环,为ESCC提供了全新的治疗策略。1、技术方法创新:建立了适用于微量临床样本的ATAC-seq建库方法,推动早期癌症表观遗传研究。2、机制新颖性:首次揭示TFAP2β通过相分离调控ESCC转录程序,提出“相分离介导的转录抑制”新机制。3、药物发现创新:发现首个针对ESCC的相分离诱导型化合物A6,具备肿瘤细胞特异性。4、研究维度完整:从临床样本→机制研究→药物开发→类器官/动物模型验证,形成闭环研究体系。本研究发现TFAP2β通过形成相分离凝聚体,发挥抑制食管鳞癌的关键作用,并成功开发出首个能够特异性增强该过程的小分子化合物A6,在临床前模型中验证了其治疗潜力。该工作不仅揭示了相分离调控肿瘤转录的新机制,也为ESCC的靶向治疗提供了新策略。展望未来,研究团队指出需进一步探索:ZNF131的下游作用机制;其他关键转录因子(如NFIX、ID4)的相分离行为及其与TFAP2β的协同关系;TFAP2β凝聚体对ESCC细胞染色质三维结构的影响;以及推进A6的临床转化研究,包括药代动力学优化和安全性评估。Deng, Z., Pu, L., Deng, K., Liu, W., Zhang, J., Zhang, L., Meng, Q., Zhou, W., Jin, H., Xu, D., Qi, S., Wu, Z., Ma, Y., Liu, X., Yao, X., Ke, B., Kerr, D. J., Yang, L., Yang, J., & Jiang, H. (2025). Targeting TFAP2β condensation suppresses the development of esophageal squamous cell carcinoma. Cell. https://doi.org/10.1016/j.cell.2025.11.019
声明:本文系药方舟转载内容,版权归原作者所有,转载目的在于传递更多信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除内容