
2024-08-20 11:20:08来源:夏建川教授团队浏览量:956
8月8日,在美国临床肿瘤学会突破性峰会 (ASCO Breakthrough) 2024上,一项来自中国、聚焦于B7H3特异性同种异体CAR-T细胞疗法的研究得到了重点介绍,还获得了摘要奖(全球共40项)。
为什么这项研究能得到国际医学界的高度赞誉?跟着本文,一起来了解吧!
现货型同种异体CAR-T 细胞疗法MT027安全可控,1年生存率高达84.6%
这是一项由研究者发起的探索性试验,涉及鞘内或脑室内给药 B7H3 特异性同种异体 CAR-T 细胞(MT027),用于治疗复发性高级别神经胶质瘤。
MT027是用健康供者T细胞制备的同种异体嵌合抗原受体T细胞注射液,通过基因修饰技术将靶向B7-H3的嵌合抗原受体(CAR)表达于基因编辑T细胞表面制备而成,用于治疗复发性胶质母细胞瘤和其他实体瘤。
截至2024年3月7日,共纳入50例B7H3阳性、KPS≥40的成年复发性高级别胶质瘤患者,其中32例接受了至少3剂(PPS1)治疗,15例接受了≥3剂治疗,至少1次疗效随访(PPS2)。
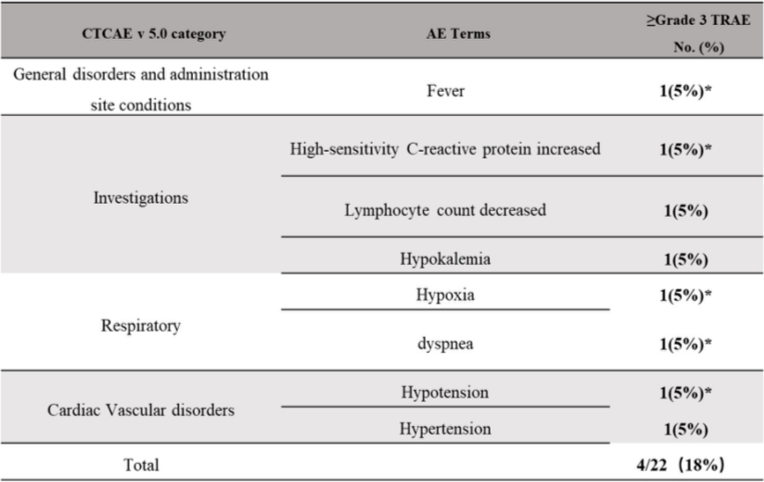
MT027 治疗的患者安全性数据(来自讲者幻灯片)
数据显示,最常见不良事件为发烧和头痛,未发生细胞因子释放综合征(CRS)、免疫效应细胞相关神经毒性综合征(ICANS)、移植物抗宿主病(GvHD)或药物相关死亡。4例(8%)患者发生≥3级不良事件,3例(6%)发生严重不良事件。
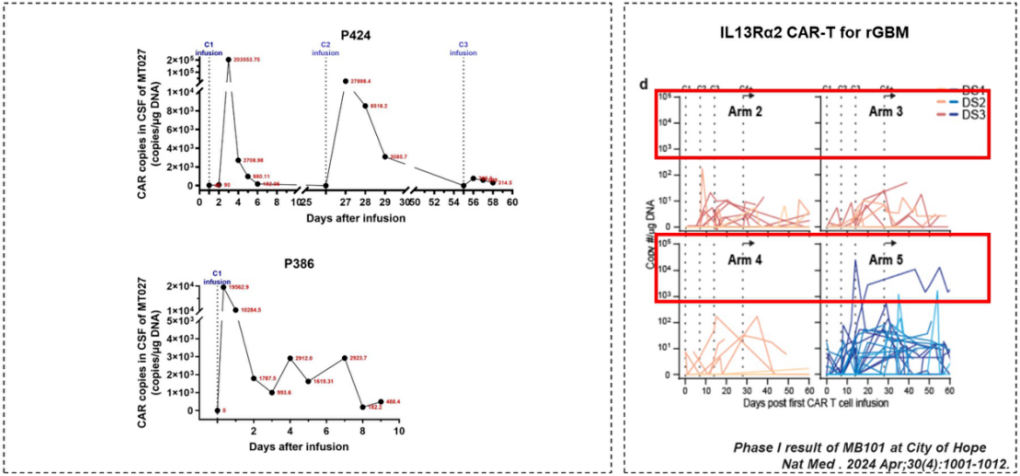
MT027 输注后展现出强大的扩增能力和长期持久性(来自讲者幻灯片)
各组CAR-T细胞拷贝数均达到10000~100000拷贝/μg,单次给药后持续时间>60天。多次给药后,患者体内CAR-T细胞数量长期维持在较高水平(中位数为8850拷贝/μg)。此外,脑脊液中关键细胞因子水平(如 IL-6、TNF-α 和 IFN-γ)显著升高和持续表达。
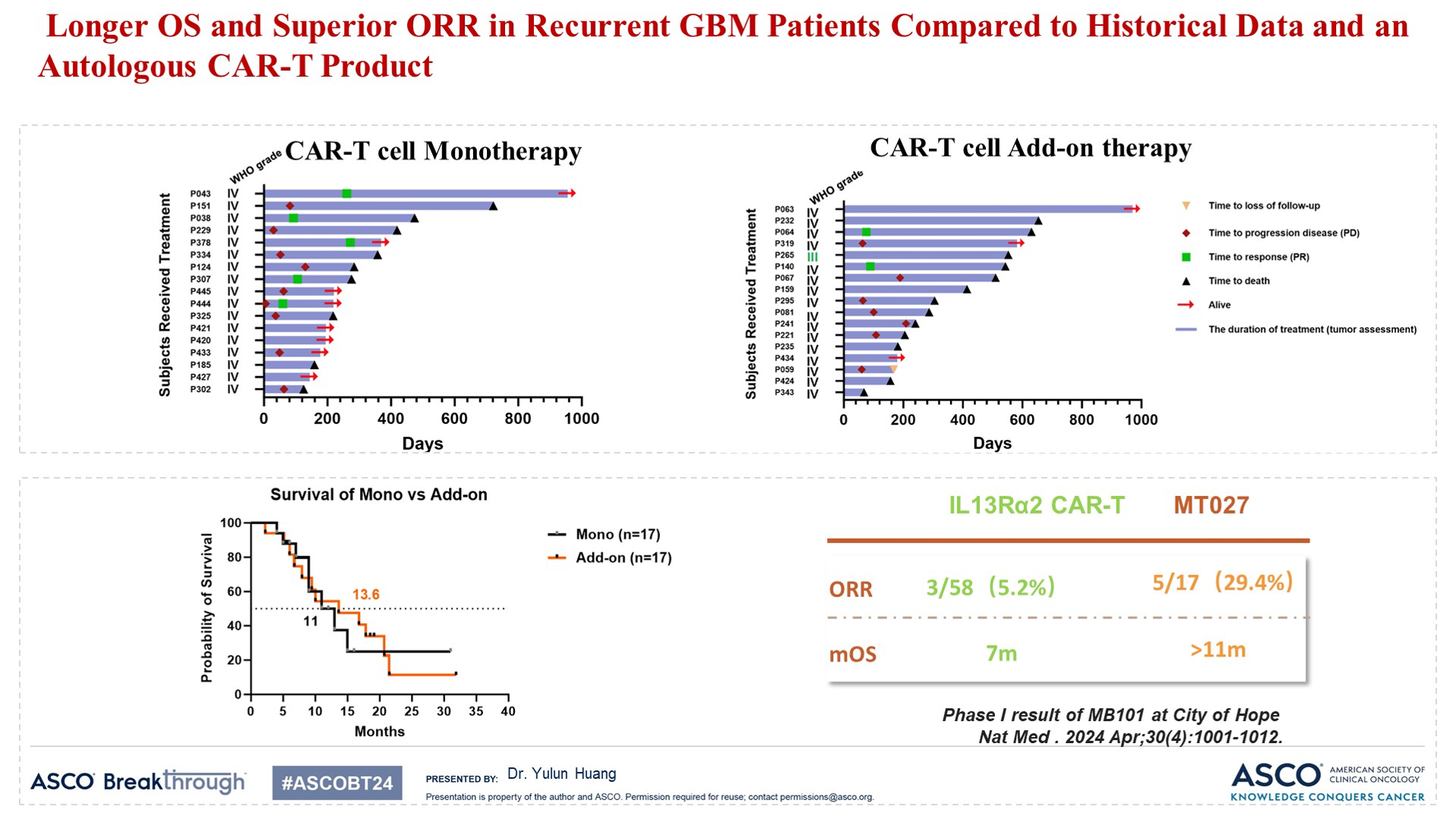
与历史数据和自体CAR-T产品相比,复发性GBM(胶质母细胞瘤)患者的OS延长和ORR优异
PPS1和PPS2组的中位OS分别为13.54个月和20.73个月,12个月OS率分别为53.30%和84.60%。
此外,MT027与历史数据和类似产品数据相比,总生存期(OS)显著延长(超过11个月),客观缓解率(ORR)更高(29.4%)。这提示通用型CAR-T治疗有望突破晚期实体瘤治疗的瓶颈。
MT027研究的3大亮点:通用、避开血脑屏障、激活冷肿瘤
这种同种异体CAR-T疗法(MT027)具有以下亮点:
“通用型”CAR T细胞产品
目前,大多数临床试验都集中在使用自体T细胞的CAR-T细胞疗法上,其生产过程既耗时又昂贵,还有制造失败的风险,且患者自身T细胞供应不足(如晚期癌症患者的T细胞耗竭和数量减少)等情况,使治疗的及时实施进一步复杂化。
来自健康供体的T细胞(同种异体 T 细胞)数量丰富且功能齐全,可以制造“现成的”CAR-T细胞产品,属于通用型 CAR-T 疗法(UCAR-T)。这种方法不仅克服了自体T细胞疗法的局限性,而且为更广泛的患者使用提供了更大的可扩展性和可用性,即促进了其大规模生产和重复使用。
避开血脑屏障
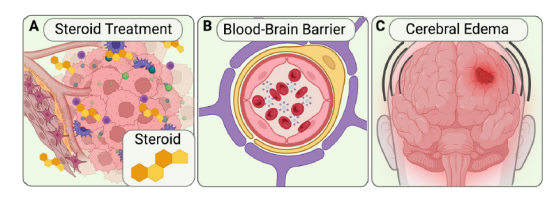
CAR-T细胞治疗脑肿瘤的障碍
通过鞘内或脑室内直接注射,相较于传统静脉注射,在脑胶质瘤治疗中展现出了显著优势。这一给药方式巧妙地避开了脑胶质瘤特有的「血脑屏障」挑战,确保了 CAR-T 细胞能够直接且精确地到达病灶,显著增强了治疗的「靶向性」,并有效减少了全身副作用的发生。
激活冷肿瘤
针对脑胶质瘤这一「冷肿瘤」的免疫特性,UCAR-T疗法通过直接注入高活性的 CAR-T 细胞,成功激活了局部强烈的免疫反应,有效抑制了肿瘤的生长。
小结
免疫细胞疗法是实体肿瘤最具前景的治疗方法之一。目前,CAR-T疗法正逐步攻克靶点选择与免疫抑制等难题,有望成为胶质母细胞瘤等实体瘤患者更有效的治疗选择,带来更理想的预后。
近年来,中国肿瘤研究在ASCO、AACR等国际舞台上的崛起不容忽视。尤其在细胞治疗领域,中国科研团队以卓越的研发实力,不仅缩短了与西方的技术差距,更在部分领域实现领跑,在临床研究的质和量两方面都有很大的进步。相信,未来将有更多的中国原研药物、创新疗法进入全球市场,为全球抗肿瘤事业贡献更多的中国力量。
声明:本文系药方舟转载内容,版权归原作者所有,转载目的在于传递更多信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除内容